[ Deutsch ] [ English ] [ Русский ]
Herzlich willkommen!
molekulartherapie.de
Theorie und modelltheoretische Therapieansätze zentralnervöser Erkrankungen
Kausale Theorie
Die Sonne scheint, in meinem Herzen ist es dunkel.
- Anton Tschechow -
1. Affektive Störungen - eine kausaltheoretische Betrachtung
1.1 Was ist eine Depression?▲
Kernsymptome und Begriffsinflation
Informationen über Depressionserkrankungen sind allgegenwärtig, spätestens seitdem sie durch Aufnahme in die Gruppe der „Volkserkrankungen“ geadelt wurden. Trotz zahlreicher Medienberichte und einer unübersichtlichen Menge von Veröffentlichungen in der Fach- und Ratgeberliteratur hat sich am mangelnden Verständnis ihrer Ursachen und Charakteristika nichts geändert.
Für die meisten Erkrankungen existieren klare Fachbezeichnungen. Eigentlich müsste das auch für die Depression und bipolare Störungen gelten, denn im Kern beruhen sie auf drei pathologischen Veränderungen affektiver Zustände:
- Pathologisch gedämpfte Affekte (Depression)
- Pathologisch gesteigerte Affekte (Manie)
- Psychosen (Wahnvorstellungen oder Halluzinationen)
Trotzdem entstand im Laufe der Zeit eine Fülle verschiedenster Begriffe für die Erkrankung, wie die nachfolgenden Beispiele eindrucksvoll zeigen. Dabei handelt es sich nicht um eine vollständige Liste, denn immer wieder tauchen neue „Fachbegriffe“ auf. Die Bezeichnungen sind zum Teil missverständlich, unklar, mehrdeutig, strittig oder redundant:
Agitierte Depression, Altersdepression, Anaklitische Depression, Angst-Depression, Anhedonische Depression, Anpassungsdepression, Apathische Depression, Asaisonale Depression, Atypische Depression, Beziehungskrisen-Depression, Bipolare Depression, Burnout-bedingte Depression, Chronisch‑depressive Störung, Depression, Depression mit somatischem Syndrom, Depressive Abwehr, Depressive Neurose, Depressive Position, Depressiver Rückzug, Depressives Irresein, Depressive Verstimmung, Digital-Burnout-Depression, Doomscrolling-Depression, Double Depression, Dysphorie, Dysthymische Depression bzw. Dysthymie, Endogene Depression, Endoreaktive Depression, Entlastungsdepression, Erschöpfungsdepression, Exogene Depression, Exogen-reaktive Depression, Funktionale Depression, Gehemmte Depression, Hidden Depression, High-Masking-Depression, Hochfunktionale Depression, Hormonelle Depression, Hypersensitive Depression, Hypersomnie-Depression, Hypoarousale Depression, Hypochondrische Melancholie, Instagram-Depression, Introjektive Depression, Involutionsdepression, Irritable Depression, Kardiovaskuläre Depression, Klinische Depression, Kognitive Depression, Kortisolassoziierte Depression, Larvierte Depression, Lichtmangeldepression, Lebenskrisen-Depression, Major Depression, Medikamentenentzugsdepression, Manisch‑depressive Störung, Manisch-melancholische Psychose, Maskierte Depression, Melancholie, Melancholische Depression, Melancholische Episode, Midlife-Depression, Minor Depression, Monopolare Depression, Narzisstische Depression, Neuroinflammatorische Depression, Neurotische Depression, Pandemie-Depression, Objektverlust-Depression, Organische Depression, Overachiever-Depression, Periodische Depression, Persistierende depressive Störung, Pharmakogene Depression, Phasische Depression, Post-Covid-Depression, Postinfektiöse Depression, Postnatale Depression, Postpartale Stimmungskrise, Posttraumatische Depression, Prämenstruelle Depression, Primäre Depression, Prüfungsdepression, Pubertätsdepression, Psychasthenische Depression, Psychogene Depression, Psychoreaktive Depression, Psychotische Depression, Rapid-Cycling-Depression, Reaktive Depression, Reine Melancholie, Rezidivierende Depression, Saisonal abhängige Depression (SAD), Schilddrüsenassoziierte Depression, Schulddepression, Schwangerschaftsdepression, Schwermut, Sekundäre Depression, Serotoninmangel-Depression, Silent Depression, Smiling Depression, Somatische Depression, Somatisches Syndrom, Somatisierte Depression, Somatogene Depression, Spätdepression, Stressinduzierte Depression, Subklinische Depression, Symptomatische Depression, Therapieresistente Depression, Trauerreaktive Depression, Trennungsdepression, Unipolare Depression, Vegetativ-affektive Depression, Vegetative Depression, Versteckte Depression, Vitaldepression, Winterdepression, Walking Depression, Wochenbettdepression, Zirkuläre Melancholie, Zyklothymia, Zyklothymische Depression, Zyklothymie.
Klassifikation der Weltgesundheitsorganisation
Ein wesentlicher Grund für die Begriffsinflation liegt in den unzureichenden Versuchen, affektive Erkrankungen global einheitlich und klar zu definieren.
Gemäß der Fassung der internationalen statistischen Klassifikation ICD‑10 der Weltgesundheitsorganisation WHO aus dem Jahr 1990 werden mehrere Hauptdiagnosegruppen (F30 ‑ F34, F38 und F39) und Unterkategorien bei Affektiven Störungen unterschieden.
ICD-10 unterscheidet sieben Kategorien affektiver Erkrankungen:
- F30 – Manische Episode
- F31 – Bipolare affektive Störung
- F32 – Depressive Episode
- F33 – Rezidivierende depressive Störung
- F34 – Anhaltende affektive Störung
- F38 – Andere affektive Störungen
- F39 – Nicht näher bezeichnete affektive Störung
Es werden ausschließlich in den Gruppen F31, F32 und F33 jeweils vier Schweregrade unterschieden, ohne diese exakt voneinander abzugrenzen:
- Leicht
- Mittelgradig
- Schwer ohne psychotische Symptome
- Schwer mit psychotischen Symptomen
Die Dauer einer Erkrankung wird nur unsystematisch berücksichtigt. Es werden die eigenständigen Kategorien F33 für eine rezidivierende (= wiederkehrende) Depression und F34 für eine anhaltende Affektstörung verwendet. Letztere wird auch als Dysthymie bezeichnet, für die es keine Differenzierung unterschiedlicher Schweregrade gibt. Erkrankungsursachen werden in den Kategorien nicht berücksichtigt.
Die Klassifikation ist unsystematisch und ein mit fachlich-methodischen Schwachstellen behafteter misslungener Versuch, verschiedene Krankheitsformen voneinander abzugrenzen.
Die sieben Kategorien sind stark voneinander getrennt und berücksichtigen nicht den kontinuierlichen Verlauf affektiver Dysregulationen. Sie sind darüber hinaus straff gebündelt, obwohl voneinander abweichende Krankheitsverläufe vorliegen können. Mittlerweile gibt es eine Überarbeitung, die 2022 als ICD‑11 in Kraft trat. ICD‑11 stellt zwar eine strukturelle Verbesserung dar, doch viele der grundlegenden Probleme bleiben bestehen.
Präzise Diagnosen sind anhand der ICD-Kategorien kaum möglich und als logische Konsequenz daraus entstehen immer neue „Fachbezeichnungen“ und Fantasiebegriffe. Ein gutes Beispiel für die Probleme, die der begriffliche Wildwuchs zur Folge hat, ist die Modediagnose „Hochfunktionale Depression“.
Die „Hochfunktionale Depression“
Häufig ist eine Depression für Betroffene erheblich belastender, als es der äußere Anschein vermuten lässt. Je höher der soziale Druck ist, funktionieren zu müssen, desto größer kann diese Diskrepanz sein. So schleppen sich viele täglich zur Arbeit und erledigen auch sonstige Verpflichtungen, obwohl sie aufgrund ihrer Gemütsverfassung dazu eigentlich nicht mehr in der Lage sind. Das hat nicht nur zur Folge, dass die Erkrankung dem persönlichen Umfeld verborgen bleiben kann, es stellt auch eine erhebliche Stressbelastung dar und birgt die Gefahr einer Intensivierung der Depression.
Für diesen Sachverhalt wurde die missverständliche Bezeichnung „Hochfunktionale Depression“ geprägt. Damit soll auf sprachliche Weise zum Ausdruck gebracht werden, dass an einer Depression Erkrankte im Alltag trotzdem „funktionieren“.
Der Begriff wird häufig so missverstanden, als handele es sich um eine besondere Form der Depression. Es gibt aber keine „hochfunktionale Depression“, es gibt ausschließlich eine Depression.
Den Unterschied macht der Umgang Betroffener mit der Erkrankung. Diese Personen könnten im wörtlichen Sinne als „hochfunktional“ bezeichnet werden, doch der Begriff bleibt technisch und ist auch für diese Umschreibung ungeeignet. Er suggeriert darüber hinaus eine feste Kategorie, obwohl es zahlreiche Zwischenformen gibt. Dadurch wird auch eine differenzierte Betrachtung der Ursachen erschwert ‑ etwa der Rolle von Resilienz, Willensstärke, Perfektionismus, der subjektiv empfundenen Intensität der Depression oder der Existenz einer inneren Rangfolge von Tätigkeiten, nach der Erkrankte ihre Aktivitäten bewältigen.
Befragungen als diagnostisches Instrument
Sämtliche Klassifikations- und Definitionschwierigkeiten erschweren Therapeuten die Erstellung einer verlässlichen Diagnose. Könnten hier alleinige Befragungen eine hilfreiche Alternative sein?
Die Frage muss leider klar mit „nein“ beantwortet werden. Die Diagnose einer Depression mit Hilfe von Fragetests ist aufgrund methodischer Probleme unsicher. Ebenfalls konterkarieren die individuell‑subjektiven Bewertungen eine exakte Messung.
Meist wird die Stärke der Erkrankung von der Anzahl der ausgewählten Symptome abhängig gemacht. Eine Begründung für diese problematische Vorgehensweise gibt es nicht. Darüber hinaus existieren unterschiedliche Testverfahren. Ein besonders häufig genutzter Fragebogen ist der Depressionstest nach I. K. Goldberg, der das Likert-Skalierungsverfahren verwendet. Es werden 18 Fragen mit sechs Antwortmöglichkeiten gestellt. Der Test ist hier zu finden: https://www.netdoktor.de/selbsttests/.
Einschränkungen der Tagesbewältigung als Hauptsymptom
Eine Differenzierung nach dem Ausmaß der Einschränkungen in der Tagesbewältigung ist eine praktikable und aussagekräftige Alternative zur ICD-Klassifizierung oder der Summierung einzelner Symptome.
Es sind vier Kategorien mit fließenden Übergängen sinnvoll:
- 1. Kategorie - Leichte Depression
Der Patient ist in seinen privaten und beruflichen Aktivitäten noch nicht oder nur leicht eingeschränkt.
- 2. Kategorie - Mittelgradige Depression
Hier werden die Alltagsaktivitäten nur unter Schwierigkeiten gemeistert. Sie reicht von mittelschweren Einschränkungen bis zu Fällen, bei denen der Tagesablauf nur unter Mühe gestaltet werden kann. Bei dieser Kategorie ist deshalb eine Differenzierung in mehrere Unterstufen sinnvoll. Die Arbeitsfähigkeit wird zunehmend vermindert, so dass eine Reduzierung der Arbeitszeit oder ein Wechsel in eine als leichter empfundene Beschäftigungsart notwendig wird, zum Beispiel ein Wechsel vom Schichtdienst in den Tagesdienst oder von Reisetätigkeit in den Innendienst. Auch eine vollständige berufliche Veränderung kann notwendig werden.
- 3. Kategorie - Schwere Depression
Private und berufliche Tätigkeiten kommen größtenteils zum Erliegen bis zum kompletten sozialen Rückzug bzw. zur Arbeitsunfähigkeit, oft verbunden mit ausgeprägten Suizidwünschen, die aufgrund bestehender Antriebsstörungen meist nicht realisiert werden. Leichte Psychosen, beispielsweise Verarmungs- oder Schuldwahn, können auftreten.
- 4. Kategorie - Schwerste Depression
Ausgeprägte psychomotorische Störungen, oft verbunden mit Bettlägerigkeit. In Extremfällen tritt ein Stupor ein, der Patient ist nicht mehr in der Lage, sich alleine anzukleiden, Nahrung aufzunehmen oder die Körperpflege zu betreiben. Psychotische Symptome, wie Wahn oder Halluzinationen, können auftreten, meist auch stärker ausgeprägt, sind jedoch nicht zwangsläufig.
Eine Ergänzung durch eine Liste einzelner Symptome ist notwendig, zum Beispiel aus der Denken-Fühlen-Verhalten-Körper-Merkmalsliste oben, wobei deren Anzahl bei der Bewertung nur eine untergeordnete Rolle spielen sollte: Hauptmerkmal für die Differenzierung ist die Qualität der Tagesbewältigung.
Die Fähigkeit zur Tagesbewältigung ist aber auch vom Umgang Betroffener mit ihrer Erkrankung abhängig und bei der Diagnose zu berücksichtigen. Der persönlich empfundene Leidensdruck wäre mit einer ausschließlichen Bewertung auf Grundlage der Bewältigung des Tagesablaufs nicht zuverlässig erkennbar. Erkrankte, die trotz der Depression „funktionieren“, würden nämlich fälschlicherweise einer niedrigeren Kategorie zugeordnet (→ Die „Hochfunktionale Depression“). Die Einschätzung des individuellen Umgangs mit der Erkrankung ist zwecks Diagnosebereinigung daher notwendig, beispielsweise durch eine subjektive Einschätzung der Befindlichkeiten.
Monopolare, bipolare und reaktive Depression vs. depressive Verstimmung
Im Schwerpunkt geht es hier um die monopolare Depression, die auf inneren (= endogenen) oder nicht eindeutig identifizierbaren Faktoren beruht und durch pathologisch gedämpfte Affekte und Aktivitäten gekennzeichnet ist. Sie ist sowohl von der bipolaren Depression als auch von der reaktiven Depression abzugrenzen.
Die auch manisch-depressive Erkrankung genannte bipolare Depression ist durch den Wechsel pathologisch übersteigerter Aktivitätsphasen (Manie) bzw. gedämpfter Aktivitätsphasen (Depression) charakterisiert und beruht ebenfalls ‑ wie die monoplare Depression ‑ auf inneren oder nicht eindeutig zu benennenden Faktoren. Fast alle Kernaussagen und Hypothesen, die hier gemacht werden, treffen auch auf die bipolare Depression zu.
Eine weitere Form wird reaktive Depression genannt, die nachweislich durch schwere psychische Stresssituationen ausgelöst wird. Die Differenzierung zwischen der auf endogenen Faktoren beruhenden monopolaren Depression und reaktiver Depression ist in der Praxis oftmals eine Herausforderung. Es ist nämlich nicht immer eindeutig erkennbar, ob eine bestimmte Stresserfahrung tatsächlich als krankheitsfördernd einzustufen ist oder deren Anteil an der Erkrankungsgenese zu bestimmen.
Alle drei genannten Depressionsformen sind grundsätzlich medizinisch behandlungsbedürftig. Häufig wird dafür die Bezeichnung klinische Depression verwendet. Dieser Begriff ist für die vorliegende Darstellung nicht relevant, da die Behandlungsbedürftigkeit allen drei Erkrankungsformen schon impliziert ist.
Entscheidend aber ist, was keine Depression ist, denn gerade hier gibt es die meisten Missverständnisse. Eine milde oder kurzfristige Reaktion auf ungünstige Lebensumstände wird als depressive Verstimmung bezeichnet. Die Symptome sind hauptsächlich schlechte Laune, Trauer oder Traurigkeit nach dem Verlust einer nahestehenden Person, nachvollziehbare Frustrationsgefühle, vorübergehendes oder begründetes Grübeln, sich Sorgen machen, keine Lust auf etwas haben oder sporadische bzw. begründete Schlafstörungen. Gerade Frustrationsgefühle oder Übellaunigkeit werden im Volksmund häufig fahrlässig und fälschlicherweise als Depression bezeichnet. Nach Beseitigung der externen Auslöser oder Beendigung einer Trauerphase verschwindet auch die depressive Verstimmung. Sie hat keinen Erkrankungscharakter und ist nicht ärztlich behandlungsbedürftig. In bestimmten Fällen ist eine psychologische Begleitung sinnvoll. Auch die depressive Verstimmung birgt Gefahrenpotential, denn unbewältigt kann sie sich zu einer reaktiven Depression entwickeln.
Sowohl die monopolare als auch die bipolare Depression gehören ab der mittelgradigen Ausprägung zusammen mit der Schizophrenie zu den schwersten psychiatrischen Erkrankungen. Oftmals unterbleiben therapeutische Maßnahmen, da weder Erkrankte noch Außenstehende den behandlungsbedürftigen Zustand erkennen. Schätzungen gehen von ca. vier Millionen betroffenen Menschen in Deutschland aus. Depressionserkrankungen erhöhen die Suizidrate auf das 30fache. Es wird geschätzt, dass 40 bis 70 Prozent aller Suizide in Deutschland durch sie verursacht werden.
Symptome einer Depression
Im Wesentlichen ist eine Depression oder die gedämpfte Phase einer bipolaren Störung gekennzeichnet durch Stimmungstiefs, Freudlosigkeit, emotionale Erstarrung oder Antriebsblockaden, die länger als drei Wochen andauern und nicht willentlich korrigierbar sind.
Die gesamte Symptomatik lässt sich vier zentralen Bereichen zuordnen: Denken, Emotionalität, Verhalten und Körper:
- Denken
- Störungen der Konzentrations- und Merkfähigkeit
- Gedankenkreisen (Rumination)
- Grübelzwang
- Denkhemmung und verlangsamtes Denken
- Übertriebener Pessimismus
- Überwiegend negative Gedankeninhalte
- Vermindertes Selbstvertrauen
- In schweren Fällen psychotische Symptomatik mit Wahnvorstellungen, Halluzinationen oder Realitätsverlust
- Emotionalität
- Unbegründete Stimmungstiefs
- Emotionale Verflachung bzw. Erstarrung
- Gefühl innerer Leere
- Unbegründete und nicht willentlich korrigierbare Freudlosigkeit oder Traurigkeit
- Ständige, übertriebene Sorge
- Gefühle der Hoffnungslosigkeit
- Innere Unruhe
- Angststörungen und Panikattacken
- Reizbarkeit und Aggressivität
- Gestörtes Selbstwertgefühl
- Libidostörungen (Libidoverlust, sexuelle Gleichgültigkeit)
- Unbegründete Schuldgefühle, bis hin zum Schuldwahn
- Verhalten
- Antriebsstörungen und Antriebsblockaden
- Innere Getriebenheit (Agitiertheit)
- Entscheidungsschwäche
- Prokrastination
- Sozialer Rückzug
- Gehemmtes Auftreten
- Mangelnde Fähigkeit, sich abzugrenzen („nicht nein sagen können“)
- Interessenverlust
- Suizidgedanken und Suizidversuche
- Essstörungen (Heißhungerattacken, Magersucht)
- Körper (somatoforme Störungen)
- Ein- und Durchschlafstörungen
- Frühes Erwachen
- Hohes Schlafbedürfnis
- Tagesmüdigkeit
- Allgemeine Müdigkeit
- Schnelle Erschöpfung
- Veränderter Gesichtsausdruck (zum Beispiel erstarrte oder traurige Mimik)
- Energie- und Kraftlosigkeit
- Leistungseinbruch
- Kreislaufbeschwerden
- Veränderungen der visuellen Wahrnehmung (Helligkeit, Kontrast, Farbwahrnehmung)
- Störungen des Verdauungssystems
- Hauterkrankungen
- Appetitlosigkeit oder Appetitsteigerung
- Auffällige Gewichtsveränderungen ohne primäre Essstörungen
- Sexualstörungen
- Muskelverspannungen
- Schmerzen
Das Narrativ von der „guten Behandelbarkeit“
Glaubt man den Verlautbarungen von Pharmakologen und Nervenärzten, ist eine Depression medikamentös in Kombination mit Psychotherapie ohne Abstriche an Lebensqualität gut behandelbar. Es wird darüber hinweggesehen, dass die Erfolge konservativer Behandlungsmethoden ernüchternd sind, was sich in den ungünstigen Krankheitsverläufen widerspiegelt, die in zahlreichen Studien dokumentiert sind (→ Härter/Bermejo/Niebling, Praxismanual Depression, Deutscher Ärzte-Verlag, Köln 2007, www.lbib.de/...).
Die Erfolgsaussichten klassischer Kombinationstherapien (Psychotherapie + Medikamente) sind ungünstig:
- Bei etwa 1/3 der Erkrankten verschwindet die Depression, unabhängig davon, welche Maßnahmen eingesetzt wurden. In der Regel ist die Gesundung nicht auf bestimmte (Einzel-)Maßnahmen zurückzuführen, die damit auch wirkungslos gewesen sein könnten. Das Verschwinden der Symptome hätte in diesen Fällen andere Gründe.
- Etwa 1/3 der mit Antidepressiva und psychotherapeutisch Behandelten bekommen ihre Symptome nur unzulänglich in den Griff – mit Nebenwirkungen bzw. deutlichen Abstrichen an Lebensqualität, sodass von einer Heilung im eigentlichen Sinne nicht mehr die Rede sein kann. Auch hier ist die Wirkung der Maßnahmen nicht verifizierbar.
- Beim letzten Drittel wirken Medikamente und Psychotherapie nicht und die Präparate verschlechtern die Situation in manchen Fällen noch durch Nebenwirkungen. Das gilt insbesondere für Patienten mit schwerer oder schwerster Depression. Ihnen bleiben noch die restlichen Behandlungsmethoden, beispielsweise Elektrokrampftherapie, Schlafentzug oder die Magnetfeldtherapie, die in der Regel ebenfalls längerfristig nicht zum Erfolg führen.
Diese Verteilung wird als Drittel-Faustregel bezeichnet und Vergleichbares gibt es auch bei anderen neurologisch-psychiatrischen Erkrankungen.
Die Fehleinschätzung einer „guten Behandelbarkeit“ passt auch zu den vielen gut gemeinten Medienbeiträgen, die den Betroffenen Mut machen sollen, aber kontraproduktiv sind und das Gegenteil erreichen. Dort erhalten sie „Tipps“ wie „verbessern Sie Ihre Stimmung durch positive Aktivitäten, treiben Sie Sport, denken Sie positiv, gehen Sie Ihren Hobbys nach, steigern Sie Ihre Wertschätzung“ etc. Jeder, der eine Depression oder bipolare Erkrankung aus eigener Erfahrung kennt, spürt die Ratlosigkeit hinter derartig floskelhaften, gut gemeinten Ratschlägen. Diese sind darüber hinaus geeignet, die Erkrankung zu verharmlosen, erwecken den falschen Eindruck einfacher Behandlungsstrategien und unterstellen indirekt eigene Verfehlungen und damit eine Mit- oder sogar Hauptschuld an der Erkrankung.
Der ungünstige Erkrankungsverlauf resultiert vor allem aus der unzulänglichen Wirksamkeit von Antidepressiva. So wurde im Rahmen von Initiativen zur Verbesserung der Qualität pharmazeutischer Produkte festgestellt, dass eine der gängigsten Behandlungsstrategien gegen Depressionserkrankungen, nämlich der Einsatz selektiver Serotonin-Wiederaufnahmehemmer (SSRI), bei 38% der Behandlungen keinerlei nachweisbare Wirkungen zeigte, wobei es über den Behandlungserfolg der restlichen 62 % keine Erkenntnisse gab. Vergleichbare Bewertungen liegen auch für Behandlungsstrategien gegen andere neurologische Erkrankungen vor. Bei Medikamenten gegen Morbus Alzheimer lag die Quote der Unwirksamkeit sogar bei 70% (Quelle: Spear/Heath-Chiozzi/Huff, Clinical application of pharmacogenetics, in: Trends in Molecular Medicine, Vol. 7/No. 5, Mai 2001).
Die Ergebnisse einer Metastudie von Irving Kirsch über die Wirkung von SSRI und SSNRI (SSNRI = Serotonin‑Noradrenalin-Wiederaufnahmehemmer) aus dem Jahre 2008, die nach ihrer Veröffentlichung eine breite mediale Aufmerksamkeit bekamen und auf der Auswertung von etwa 50 Einzelstudien beruhten, waren noch ernüchternder: Sie ergaben klare Beweise, dass die Medikamente nicht wirksamer sind als die Scheinpräparate (Quelle: Kirsch, Deacon, Scoboria et al., Initial Severity and Antidepressant Benefits: A Meta-Analysis of Data Submitted to the FDA, Public Library of Science/PLOS Medicine, Bd. 5.2, e45, San Francisco, 2008). Nur bei schweren Erkrankungsfällen wurde ein kleiner und unbedeutender Unterschied zum Placebo festgestellt. Die Untersuchung zielte auf Studien über die Wirkstoffe Fluoxetin, Venlafaxin, Nefazodone und Paroxetin, so dass die Aussagen nicht auf alle Medikamente dieser Wirkmechanismen übertragen werden können. Die Resultate sind jedoch repräsentativ und werden durch vergleichbare Untersuchungen bestätigt. Mit interessanten Details zu Paroxetin beschäftigt sich auch der folgende Abschnitt (→ Die Studie 329 des Paroxetin-Herstellers GlaxoSmithKline).
Die Studienergebnisse wurden nach ihrer Publikation von Pharmaherstellern und Fachärzten sogleich kritisiert. Ulrich Hegerl vom Universitätsklinikum Leipzig entgegnete, dass „(...) die Schlussfolgerung dieser Übersichtsstudie aber auf mehreren Fehlern beruht. Klinische Studien wie die, die Kirsch und sein Team von der University of Hull überprüft haben, sollten die prinzipielle Wirksamkeit der Antidepressiva überprüfen. In solchen Untersuchungen werden die Patienten umsorgt, aktiviert, sie erhalten Zuspruch, es wird ihnen Hoffnung vermittelt. Dabei kommt es zu einem riesigen Placebo-Effekt. Deshalb ist der Unterschied zwischen der Wirkung der Scheinmedikamente, die da verabreicht werden, und den echten Mitteln, so gering, wie Kirsch jetzt kritisiert. Denn diese Versorgung hilft zwar auch den Patienten, die das echte Medikament erhalten, die Wirkung der Maßnahmen addiert sich aber nicht.“ (Quelle: Markus C. Schulte von Drach im Interview mit Ulrich Hegerl am 17.5.2010, Studie zu Antidepressiva - „Diese Berichte werden Menschenleben kosten“, SZ.de, Süddeutscher Verlag, München 2010, http://www.sueddeutsche.de/wissen/...).
Sind diese Einwände berechtigt? Zunächst ist es nicht möglich, die ca. 50 Einzelstudien hinsichtlich der Aussagen von Ulrich Hegerl zu prüfen, beispielsweise bezüglich der „Umsorgung“ der Teilnehmer. Ebenso plausibel ist ein standardisierter, wenig umsorgender Studienablauf. Und selbst wenn es so wäre: Ist eine medizinische Behandlung außerhalb von Studien denn in der Regel nicht ebenso „umsorgend“? Bei genauer Betrachtung macht gerade dieser Einwand deutlich, dass die Medikamente und die Scheinmedikamente sich von ihrer Pharmakodynamik nicht oder kaum unterscheiden. Denn es müsste doch wenigstens ein ausreichend signifikanter Unterschied zwischen Placebo und einem Medikament feststellbar sein.
Es ist natürlich viel von überzeugten SSRI‑ und SSNRI‑Anwendern verlangt, sich kritisch über die Wirksamkeit der Substanzen zu äußern. Denn das bedeutet, die eigene auf diesen Präparaten beruhenden Behandlungsstrategien zumindest teilweise in Frage stellen zu müssen. Dabei liegt das Problem vor allem im beschränkten Angebot medikamentöser Behandlungen gegen Affektstörungen, die fast ausschließlich auf der Manipulation von Monoaminen ‑ zum Beispiel Serotonin oder Noradrenalin ‑ beruhen. Denn was sollten Psychiater auch sagen, wenn ihnen die Industrie kaum eine andere Möglichkeit bietet, ihre Patienten zu behandeln?
Die Herstellerfinanzierung der meisten Antidepressivastudien ist methodisch problematisch. In verschiedenen Beiträgen wird berichtet, dass Pharmaunternehmen ihre eigenen Medikamente durchweg besser beurteilen als Vergleichspräparate und darüber hinaus zahlreiche Studien unveröffentlicht lassen, die keinen Wirksamkeitsnachweis erbringen (Quellen: Hansen RA et al., Internal Med, 9/2005; Whittington CJ et al., Lancet 2004, Artikel im New England Journal of Medicine vom 17.1.2008). Eine Übersicht über den Themenkomplex enthält folgende Web-Seite: www.adfd.org/Manipulation bei Antidepressiva-Studien.
Die Studie 329 des Paroxetin-Herstellers GlaxoSmithKline
Ein gutes Beispiel, dass bei nicht herstellerunabhängig erstellten Studien Misstrauen berechtigt ist, betrifft eine zwischen den Jahren 1994 und 1998 durchgeführte Studie über die Wirksamkeit und Verträglichkeit der SSRI-Substanz Paroxetin an Heranwachsenden mit einer unipolaren Depression (Quelle: Paroxetin bei Jugendlichen unwirksam, Pharmazeutische Zeitung online, 17.9.2015, Govi-Verlag Pharmazeutischer Verlag GmbH, Eschborn 2015, http://www.pharmazeutische‑zeitung.de/...).
Im Juli 2001 veröffentlichte ein 21-köpfiges Team um den Psychiater Martin Keller von der Brown University School of Psychiatry and Human Behavior, Providence/USA, die besagte Untersuchung über Produkte des damaligen Pharmaherstellers SmithKline Beecham (heute: GlaxoSmithKline) in der renommierten Fachzeitschrift Journal of the American Academy of Child and Adolescent Psychiatry (M. Keller et al., Efficacy of Paroxetine in the Treatment of Adolescent Major Depression: A Randomized, Controlled Trial, http://www.jaacap.com/...).
Die Zusammenfassung der damaligen Studienergebnisse belegte eine gute Wirksamkeit und Verträglichkeit der Paroxetin-Präparate von SmithKline Beecham ‑ Handelsnamen Paxil bzw. Seroxat ‑ bei Kindern und Jugendlichen. Originalzitat aus dem Abstract: „Paroxetine is generally well tolerated and effective for major depression in adolescents.“.
Diese positiven Schlussfolgerungen der Autoren wurden jedoch von Beginn an in Zweifel gezogen, da sie der ausführlichen Studiendokumentation völlig widersprachen. Die Studie wurde erstmals im Jahre 2002 von einem Mitarbeiter der amerikanischen Aufsichtsbehörde für Arzneimittel U. S. Food and Drug Association (FDA) bis ins Detail überprüft. Dieser stellte fest, dass Paroxetin gegenüber dem Placebo keine signifikante Überlegenheit zeigte. Das gilt auch für das in der Studie zum Vergleich herangezogene trizyklische Antidepressivum Imipramin. Die jeweils achtwöchigen Verabreichungen bewirkten auf der 66 Punkte umfassenden Hamilton-Skala eine Verbesserung um 10,7 Punkte (Paroxetin), 9,0 Punkte (Imipramin) beziehungsweise 9,1 Punkte (Placebo). Die Abweichungen zum Placebo waren somit minimal und weit jenseits eines Wertes, der als brauchbar anzusehen ist. Signifikant hingegen waren die Nebenwirkungen: Paroxetin erhöhte beispielsweise die Suizid-Gefahr erheblich, Imipramin ging mit einem erhöhten kardiovaskulären Risiko einher.
All das hat den Markt für Paroxetin bei Jugendlichen zunächst nicht beeinflusst. Alleine in den USA wurde 2002, also im Jahr der ersten Überprüfung durch die US-amerikanische FDA, über zwei Millionen mal Paroxetin für Kinder und Jugendliche verordnet.
Erst aufgrund von Nachforschungen britischer Journalisten und ihrer Veröffentlichungen in verschiedenen Reportagen des BBC wurden die britische Zulassungs- und Aufsichtsbehörde für Arzneimittel Medicines and Healtcare Products Regulatory Agency (MHRA) und auch nochmals ihr US-amerikanisches Pendant FDA ‑ die FDA nun schon zum zweiten Mal nach 2002 ‑ auf den Fall aufmerksam. Im Juni 2003 informierten beide Behörden Fachkreise und Ärzte und wiesen diese an, Paroxetin nicht mehr an Jugendliche unter 18 Jahren zu verschreiben.
Die Verfehlungen im Zusammenhang mit dieser Studie waren sehr komplex und gingen über bewusst falsche Formulierungen im Studien-Abstract weit hinaus. Es wurden nicht nur Ergebnisse manipuliert und zurückgehalten. Die Namen einiger Studienteilnehmer hatte man sich ausgedacht und mindestens drei Jugendliche wurden nach Suizidversuchen mit der Begründung aus der laufenden (!) Studie ausgeschlossen, sie seien ungeeignet für eine Teilnahme, obwohl gerade diese Ereignisse für die Bewertung der Sicherheit relevant gewesen wären.
Auch die Vermutung eines Herausgebers des British Medical Journals, die Textentwürfe der Studiendokumentation seien von Ghostwritern des Herstellers geschrieben worden, ließ sich später nachweisen. SmithKline Beecham beauftragte die auf Pharmaprodukte spezialisierte PR-Agentur Scientific Therapeutics Information mit der Erstellung des Fachartikels, der später unter dem Namen von Martin Keller veröffentlicht wurde (Quelle: Controversial Paxil paper still under fire 13 years later, 2.4.2014, The Brown Daily Herald, Providence, Rhode Island/USA, 2014, http://www.browndailyherald.com/...).
Das passt zu dem Fakt, dass die 21 angegebenen „Mitautoren/-innen“, allesamt die Crème de la Crème der amerikanischen Kinderpsychiatrie, überhaupt nicht direkt an der Durchführung der Untersuchung beteiligt waren.
Darüber hinaus arbeiteten damals der Studienleiter Martin Keller und mindestens einer der „Mitautoren“, James P. McCafferty, für SmithKline Beecham. Einen Hinweis auf Interessenkonflikte sucht man im Studiendokument jedoch vergeblich.
Es stellte sich heraus, dass SmithKline Beecham bzw. GlaxoSmithKline Studien im Zusammenhang mit Paroxetin-Präparaten schon immer manipulierte und diesen niemals eine über die Placebowirkung hinausgehende Wirksamkeit hätte attestiert werden dürfen.
Die Verfehlungen des Herstellers führten zum größten Strafverfahren in der Geschichte der Pharmazie. Im Jahre 2012 akzeptierte GlaxoSmithKline eine Strafe in Höhe von 3 Milliarden US‑Dollar ‑ die bis heute höchste Strafe in der Geschichte der pharmazeutischen Industrie ‑ wegen verschiedener Manipulationen, hauptsächlich jedoch im Zusammenhang mit der Studie 329.
Dennoch hält die Diskussion um das Medikament und die Veröffentlichung an. Trotz mehrfacher Aufforderung in den Jahren 2003, 2005 und 2009, die Studie nachträglich zurückzuziehen, weigern sich die Herausgeber des Journal of the American Academy of Child and Adolescent Psychiatry bis heute (Stand März 2023). Im Jahre 2013 wurde dieses Anliegen erfolglos dem Hersteller GlaxoSmithKline vorgetragen.
Dass die Studie 2015 nochmals begutachtet und der Skandal damit weiter ein Thema bleibt, ist der Initiative der Forschergruppe Restoring Invisible and Abandoned Trials/RIAT und dem British Medical Journal zu verdanken.
Bis heute (Stand März 2023) sind Paroxetin-Präparate auf dem Markt und werden gegen verschiedene psychiatrische Erkrankungen verschrieben.
Multifaktorielle Ätiopathogenese
Ein Zusammenspiel genetischer, biologischer und psychosozialer Faktoren kann eine Depression auslösen ‑ diese Ursachenhypothese wird als multifaktorielle Ätiopathogenese bezeichnet. Es existiert bis heute kein wissenschaftlich anerkanntes Modell, das alle potentiellen Ursachen integriert.
Eine biologische Erklärung als Teil der multifaktoriellen Ätiopathogenese ist die Monoaminhypothese, auf der u. a. die Anwendung von SSRI- oder SSNRI-Medikamenten beruht. Alternative Hypothesen betreffen polygenetisch-vererbte Dispositionen oder verschiedene Stressfaktoren.
Die Monoaminhypothese und die monoaminen Botenstoffe
Die pharmazeutisch-medizinische Forschung konzentriert sich aufgrund der dominanten Monoaminhypothese vor allem auf die monoaminen Botenstoffe Noradrenalin und Serotonin, da beide in einem ursächlichen Zusammenhang mit depressiven Symptomen stehen sollen, und ihnen stimmungsaufhellende bzw. antriebsfördernde Wirkungen unterstellt werden. Es werden Versorgungsmängel oder Störungen der Botenstoffübertragung an den Kontaktstellen zwischen den Nervenzellen vermutet. Die meisten der sich auf dem Markt befindlichen Medikamente manipulieren die Reizübertragung dieser beiden Substanzen zwischen den Nervenzellen. Die Frage nach den genauen Kausalitäten zwischen Störungen im Noradrenalin- und Serotoninstoffwechsel und einer Affekterkrankung bleibt unbeantwortet.
Eindeutige Aussagen und schlüssige Erklärungen über Ursache-Wirkungs-Beziehungen gibt es nicht und es bleibt unklar, ob beobachtete Veränderungen Ursachen, Folgen oder Begleiterscheinungen der Erkrankung sind. Es wird nichts darüber ausgesagt, ob angebliche Serotonin- oder Noradrenalinprobleme eine Depression verursachen, ob der Zusammenhang umgekehrt ist oder ein anderer Zusammenhang besteht. Niedrige Serotoninwerte von bis zu ‑50% sind bei vielen Depressiven in verschiedenen Körperflüssigkeiten (Blutserum, Urin, Speichel oder Liquor) messbar, allerdings gibt es auch Untersuchungen, die zu gegenteiligen Ergebnissen kommen. Die Höhe des Serotoninspiegels ist nur bedingt aussagekräftig, denn die Werte in verschiedenen Körperflüssigkeiten sagen nichts aus über die unmittelbaren Vorgänge an den Kontaktstellen der Nervenzellen im Gehirn.
Die Monoaminhypothese wird von vielen Forschern in Zweifel gezogen, da die mehrwöchige Wirkungsverzögerung der Medikamente eher für andere Ursachen spricht. Sie wirken nach der Einnahme an den Übertragungsstellen der Nervenzellen sofort, während die eigentliche depressionsmindernde Wirkung ‑ sofern überhaupt eine eintritt, siehe oben ‑ in den meisten Fällen erst nach mehreren Wochen einsetzt. Viele Wissenschaftler gehen davon aus, dass eher nachgelagerte bzw. sekundäre neurobiologische Anpassungsprozesse für die Minderung der Symptome verantwortlich sind (Quelle u. a.: Köhler 2005). Darüber hinaus werden die langen Wirkungsverzögerungszeiten auch mit Placebo-Effekten in Zusammenhang gebracht.
Viele Mediziner sehen ein weiteres Problem im breiten Wirkungsspektrum der Antidepressiva und vermuten daher eher eine beruhigende oder angstlösende Wirkung anstatt einer Senkung der depressiven Symptomatik (Quelle: Moncrieff/Kirsch 2005).
Ein Artikel des Magazins Zeit Wissen aus dem Jahr 2008 fasst die Kontroverse prägnant zusammen: „Der Botenstoff Serotonin hat eine erstaunliche Karriere als Glückshormon hingelegt. Maßgeblich beteiligt daran waren Werbemaßnahmen für Medikamente. Seit 1965 verdächtigen Ärzte einen niedrigen Serotonin-Spiegel im Gehirn, für Depressionen verantwortlich zu sein. Doch die große Zeit des Botenstoffs begann in den 80er Jahren. Damals wurde eine neue Art von Antidepressiva entwickelt, die Selektiven Serotonin-Wiederaufnahme-Hemmer (SSRI, berühmt wurde vor allem Prozac, in Deutschland unter dem Namen Fluctin im Handel). Diese sollen verhindern, dass die Nervenzellen im Gehirn das ausgeschüttete Serotonin zu schnell wieder aufnehmen. Auf der deutschen Internetseite des Pharmaherstellers Pfizer steht nach wie vor: «Bei einer Depression besteht ein Mangel an Serotonin.» Doch dies konnte bis heute keine Studie nachweisen. Manche Depressive haben sogar einen höheren Serotonin-Spiegel als Gesunde. Was ein normaler Wert ist, weiß ohnehin niemand. Außerdem dauert es in der Regel mehrere Wochen, bis die SSRI bei Patienten Wirkung zeigen, obwohl die Wiederaufnahme-Hemmung schon nach den ersten Tabletten einsetzt. Viele Forscher vermuten inzwischen, dass Serotonin nur indirekt mit der Depression zu tun hat. Die irische Medikamenten-Aufsichtsbehörde jedenfalls untersagte 2003 einem Pharmahersteller, in Informationsbroschüren zu behaupten, das Antidepressivum korrigiere ein chemisches Ungleichgewicht im Gehirn.“ (Quelle: Eva‑Maria Schnurr, Gefährliche Helfer, Zeit Wissen 2/2008, Zeitverlag Gerd Bucerius, Hamburg).
Aufgrund der zunehmenden Skepsis gegenüber Serotonin- und Noradrenalinmodellen wird derzeit verstärkt nach Möglichkeiten geforscht, andere monoamine Neurotransmitter zu beeinflussen. So soll der relativ neue Wirkstoff Bupropion (Handelsname Elontril) u. a. die Dopaminübertragung modulieren. Andere Forschungsaktivitäten beschäftigen sich mit Manipulationen des Neurotransmitters Gamma-Aminobuttersäure (GABA).
1.2 Ursachen einer Depression auf Zellebene (Mikrosicht) ▲
Die Fokussierung der Industrie auf wenige monoamine Substanzen, deren systemische Rollen im Nervensystem nur fragmentarisch verstanden sind, führte in eine therapeutische Sackgasse. Sie ist ungeeignet, erfolgversprechende Behandlungsstrategien gegen multifaktorielle neurologisch-psychiatrische Erkrankungen mit einer großen Bandbreite von Symptomen zu entwickeln. Gerade die Symptomvielfalt verweist auf einen komplexen Ursachenmix. Eine Erklärung, die sich auf Ungleichgewichte weniger Botenstoffe beschränkt, wird dieser Komplexität nicht gerecht.
Die Kenntnisse über an affektiven Vorgängen beteiligten Neurotransmittern und deren genaue Wirkungmechanismen sind nur rudimentär - und das betrifft nicht nur Serotonin oder Noradrenalin. Es wurden schon Ende der 1990er Jahre etwa 1.000 Substanzen identifiziert, die bei der Übertragung von Nervenreizen alleine für Gefühlsregungen eine Bedeutung haben (Quelle: C. Eberhard‑Metzger, Glück ist, wenn die Chemie stimmt, in: Bild der Wissenschaft, Konradin Medien GmbH, Leinfelden-Echterdingen 1999, www.wissenschaft.de/.../65655/). Die tatsächliche Zahl dürfte heute eher höher liegen.
Inzwischen wurden weitere Neurotransmitter identifiziert, die hier eine Rolle spielen könnten, beispielsweise Dopamin, Acetylcholin, Aspartat, Dimethyltryptamin, Histamin oder die Gamma-Aminobuttersäure (GABA). Neurotransmitter sind ebenfalls auf sekundäre Botenstoffe (Second Messenger) im Zellinneren angewiesen.
Auch eine Vielzahl von Endorphinen bzw. Neuropeptiden ist in die neuronale Signalübertragung involviert. Die Existenz unbekannter Botenstoffe ist ebenso wahrscheinlich. Weiter gibt es zahlreiche Neuromodulatoren wie Spurenamine, die Gefühle und Empfindungen im Nervensystem steuern und in ihrer Wirkung die Nervennetzdynamik wesentlich stärker bestimmen als Neurotransmitter. Viele Nervenzellen setzen zusätzlich Kotransmitter frei, die als Neuromodulatoren wirken und emotionale Prozesse stark beeinflussen. Ihre Wirkmechanismen sind weitgehend ungeklärt.
Andere wichtige Substanzen sind Neurotrophine oder Nervenwachstumsfaktoren, die als Neurostimulatoren für die Entwicklung und Funktionsfähigkeit von Nervenzellen und die Neuroplastizität eine große Bedeutung haben. Der wichtige Nervenwachstumsfaktor BDNF (Brain-derived neurotrophic factor) wird derzeit intensiv erforscht. Ein BDNF-Mangel wird mit verschiedenen Nervenerkrankungen in Verbindung gebracht, unter anderem auch mit Affektstörungen.
12 Argumente gegen den Einsatz von Monoaminmanipulatoren
Mit vielen der gängigen Medikamenten ist man derzeit lediglich in der Lage, die Übertragung oder den Abbau monoaminer Neurotransmitter zu manipulieren ‑ ohne dass die genauen Wirkmechanismen der Präparate verstanden werden. Die Wiederaufnahmehemmung bewirkt lediglich, dass die Botenstoffe länger im synaptischen Spalt verbleiben. Auf die Reizweiterleitung in den Axonen haben diese Medikamente keinen direkten Einfluss.
Das betrifft mindestens vier Klassen von Antidpressiva: SSRI, SSNRI, NDRI und MAO-Hemmer. SSRI blockieren selektiv den Serotonintransport (z. B. Fluoxetin, Paroxetin, Sertralin, Citalopram oder Escitalopram), SSNRI zusätzlich den für Noradrenalin (z. B. Venlafaxin). NDRI blockieren den Transport von Dopamin und Noradrenalin (Bupropion). Alle drei erhöhen selektiv den jeweiligen Monoaminspiegel im synaptischen Spalt. MAO‑Hemmer blockieren dagegen das Abbauenzym Monoaminooxidase und erhöhen damit breit sämtliche Monoamine (z. B. Moclobemid).
Der Einsatz der früher gebräuchlichen trizyklischen Antidepressiva (z. B Amitriptylin, Imipramin, Clomipramin, Doxepin) ist wegen ihrer hohen Rate an Nebenwirkungen rückläufig. Da sie neben einer Hemmung der Wiederaufnahme von Serotonin und Noradrenalin zusätzlich noch Rezeptoren mehrerer Botenstoffe blockieren, treffen die nachfolgenden Überlegungen auch auf sie zu.
Eine direkte Erhöhung der Botenstoffe in der Nervenzelle ist pharmakologisch nicht möglich und würde mit hoher Wahrscheinlichkeit unerwünschte Gegenreaktionen auslösen. Eine industrielle Produktion von Serotonin gilt als technisch ausgeschlossen. Serotonin ist zudem nicht oral bioverfügbar und kann die Blut‑Hirn‑Schranke nicht überwinden. Selbst wenn es hypothetisch die Nervenzellen erreichen würde, wäre eine Gegenregulation zu erwarten: serotonerge Neurone würden ihre Eigenproduktion drosseln (negative Feedbackmechanismen), und die Zahl der Serotoninrezeptoren könnte durch Downregulation bzw. Rezeptorinternalisierung sinken.
Die zentrale Frage lautet: Ist die Monoaminhypothese plausibel und sind die Wirkungsmechanismen darauf beruhender Antidepressiva geeignet, eine Depression erfolgreich zu therapieren? Zur Beantwortung müssen die Wirkungsmechanismen der Medikamente und die Konsequenzen ihrer Anwendung umfassend bewertet werden, woraus 12 Einwände resultieren:
- Oberflächliche Wirkung
Monoaminwiederaufnahmehemmer verlängern lediglich die Verweildauer weniger Botenstoffe im synaptischen Spalt, ohne tiefer in die neuronalen Prozesse einzugreifen.
- Biologische Unterkomplexität
Die Medikamente adressieren nur Monoamine, obwohl affektive Prozesse durch hunderte Neurotransmitter, Neuropeptide, Neuromodulatoren, Spurenamine und Kotransmitter hochkomplex gesteuert werden.
- Fehlende Evidenz
Es gibt keinen belastbaren Nachweis, dass Monoaminkonzentrationen Affekte ursächlich steuern.
- Unvollständige Zielerfassung
Zentrale Mechanismen der neuronalen Signalübertragung wie Plastizität, Genexpression, Second Messenger und Rezeptordynamik bleiben unberührt.
- Keine intrazelluläre Wirkung
Es findet keine Erhöhung der Botenstoffe in den Nervenzellen statt.
- Gegenreaktionen
Botenstoffmanipulationen bergen die Gefahr unkalkulierbarer Gegenreaktionen (Downregulation, Rezeptorverlust oder verminderte Eigenproduktion).
- Netzwerkstörungen
Die künstlich erzeugten Ungleichgewichte einzelner Botenstoffkonzentrationen destabilisieren neuronale Systeme.
- Zelluläre Nebenwirkungen
Monoamine haben vielfältige Funktionen außerhalb der Affektregulation, und Manipulationen können andere Zellfunktionen beeinträchtigen.
- Unspezifische Hirnwirkung
Die Medikamente wirken breit und ungesteuert im gesamten Gehirn und beeinflussen auch nicht betroffene Nervenzellen und andere zelluläre Prozesse.
- Fehlende Beeinflussung der Reizweiterleitung
Die Vorgänge in den Nervenfasern (Axonen) bleiben unverändert.
- Statischer Prozess
Der Medikamentenrhythmus ist statisch (tägliche Einnahme, Retard-Präparate), während neuronale Prozesse hochdynamisch sind und sich sekundenschnell anpassen.
- Multifaktorieller Krankheitscharakter
Die Symptomvielfalt einer Depression weist auf eine entsprechende Ursachenvielfalt auf Zell‑, Netzwerk‑ und Organebene hin; monoaminzentrierte Therapien lassen diese Faktoren unberücksichtigt.
Ableitung der ersten Hypothese
Bedingt durch ihren unvollständigen und manipulativen Ansatz sind die auf der Monoaminhypothese beruhenden Antidepressiva nicht in der Lage, den Anforderungen einer ursächlichen Therapie gerecht zu werden. Dieses Urteil wird sowohl von der hohen Unzufriedenheit Betroffener gerechtfertigt als auch von der fachlichen Kritik, denn etwa 2/3 der Patienten profitieren nicht oder nur bedingt von den Medikamenten, was die Grenzen des Ansatzes klinisch belegt.
- Hypothese: Eine Depression beruht auf komplexen Störungen neuronaler Funktionen, die weit über Veränderungen im Stoffwechsel monoaminer Botenstoffe hinausgehen.
Reizübertragungsfehler aufgrund eines fehlerhaften Stoffwechsels monoaminer Botenstoffe ist nur eine mögliche Ursache. Ebenso kommen Störungen bei der Reizentstehung, der Reizübertragung im Allgemeinen oder der Reizweiterleitung der Neuronen in Betracht. Darüber hinaus sind neuronale Funktionsstörungen denkbar, die einen völlig anderen Charakter haben.
Ableitung der zweiten Hypothese
Die Gliazellen wurden lange Zeit kaum beachtet, obwohl ihre Anzahl im menschlichen Gehirn mit bis zu 100 Milliarden mit denen der Neuronen vergleichbar ist. In manchen Arealen hat das Gehirn eines Menschen sogar bis zu dreimal mehr Gliazellen als Neuronen. Der Begriff Hirnzellen schließt daher, neben den verschiedenen Neuronenarten, die Gliazellen ein.
Zunächst wurde den Gliazellen nach ihrer Entdeckung im 19. Jahrhundert durch Rudolf Virchow nur eine Funktion als „Nervenkitt“ zur Stützung der Neuronen zugeschrieben.
Nach und nach hat sich das Wissen über ihre Funktionen erhöht und seit einigen Jahren ist bekannt, dass eine bestimmte Sorte von Gliazellen, die Astrozyten, sogar den Informationsaustausch an den Synapsen der Neuronen modulieren, indem sie eigenständig Neurotransmitter ausschütten. Weiter sind Astrozyten für die Regulation des Flüssigkeitshaushalts im Gehirn zuständig und nehmen überschüssige Kalium‑Ionen während der Reizweiterleitung auf. Bestimmte Typen von Astrozyten sind in der Lage, an der Neurogenese mitzuwirken, das heißt sich in Neuronen umzuwandeln, um Lücken aufzufüllen. Neueste Forschungen weisen darauf hin, dass Astrozyten auch aktiv den Glukosetransport ins Gehirn steuern (Quelle: Pharmazeutische Zeitung online, Gliazellen regulieren aktiven Zuckertransport ins Gehirn, Avoxa-Mediengruppe Deutscher Apotheker GmbH, 12.8.2016, http://www.pharmazeutische-zeitung.de/...).
Darüber hinaus stellen die Mikrogliazellen das Immunsystem des Gehirns dar und sind für den Abtransport schädlicher Stoffe, beispielsweise von Teilen abgestorbener Zellen, zuständig. Sie fungieren als Immunzellen und sind für Phagozytose und Entzündungsregulation verantwortlich.
Andere Typen von Gliazellen bilden die weiße Myelinschicht, die Axone isolieren und für eine schnelle Nervenreizweiterleitung unerlässlich sind. Diese Gliazellen werden im Gegensatz zur „grauen Substanz“, den eigentlichen Nervenzellkörpern, als „weiße Substanz“ bezeichnet. Im Rückenmark und Gehirn sind das die Oligodendrozyten und außerhalb davon im peripheren Nervensystem die Schwann'schen Gliazellen.
Forscher der Stanford University konnten zeigen, dass Gliazellen die Anzahl synaptischer Verbindungen beeinflussen und an regenerativen Prozessen im Gehirn beteiligt sind (Quelle: Barres et al. 2005).
Diese Funktionen sind aber nur ein kleiner Teil dessen, was Gliazellen im Nervensystem leisten. Quintessenz: Die Qualität der Informationsverarbeitung und der Gesundheitszustand des Gehirns hängen wesentlich von funktionstüchtigen Gliazellen ab.
- Hypothese: Störungen der Gliazellfunktionen beeinträchtigen neuronale Aktivitäten und können eigenständige oder mitverursachende Faktoren einer Depression sein.
Gliazellen übernehmen zentrale Aufgaben in der Versorgung, Regulation und Isolation von Nervenzellen und beteiligen sich aktiv an neuronaler Kommunikation und Neurogenese. Werden diese Funktionen nicht korrekt durchgeführt, können daraus affektive Symptome entstehen oder sich verstärken.
1.3 Gehirnlandkarte (Makrosicht) ▲
Für ein umfassendes Verständnis affektiver Erkrankungen reicht eine ausschließlich auf Funktionen einzelner Zellen reduzierte Betrachtung nicht aus. Bei der Diskussion der Schwachstellen gängiger Antidepressiva wurde deutlich, dass diese auch in nicht betroffenen Hirnarealen unerwünschte Aktivitäten entfalten können oder andere hirnorganische Ursachen unberücksichtigt lassen. Einer dieser Gründe könnte in der ausschließlichen bzw. überwiegenden Erkrankung bestimmter Hirnareale liegen, die funktionell mit Affekten in direktem oder indirektem Zusammenhang stehen.
1.3.1 Gehirnareale und ihre Funktionen
Das Gehirn eines Menschen hat ungefähr 100 Milliarden Neuronen mit einer hochgradigen Vernetzung untereinander. Jede davon kann bis zu 10.000 Verbindungen zu anderen Nervenzellen unterhalten. Dazu kommt noch eine etwa gleichgroße Anzahl von Gliazellen, die je nach Hirnareal die Neuronen um bis zum Dreifachen übertreffen kann. Einige Wissenschaftler und Philosophen bezeichnen das Gehirn als die „komplexeste Struktur des Universums“, was jedoch ziemlich vermessen ist, da bisher fast ausschließlich nur irdische Strukturen bekannt sind.
Der Mythos vom komplexesten Gebilde im Universum
Dass es sich beim Gehirn um ein hochkompliziertes Organ handelt, steht außer Zweifel. Es ist jedoch wenig hilfreich, sich von dieser Zuschreibung einschüchtern zu lassen, denn es besteht hauptsächlich aus zwei Zellarten ‑ Neuronen und Gliazellen ‑, die letztlich Reize korrekt zu verabeiten haben. Auch weitere Aspekte des Nervensystems sind ‑ wie bei jeder ganzheitlichen Betrachtung ‑ zu beachten, beispielsweise die Blutgefäßzellen des Gehirns, die mit ihrer Versorgungsfunktion aber indirekt bzw. sekundär ebenfalls zur Reizverarbeitung beitragen. Die primären Hauptakteure des Gehirns sind aber Nerven- und Gliazellen.
Warum sind die Erfolge im Verständnis und in der Behandlung neurologisch-psychiatrischer Erkrankungen so dünn gesät? Liegt ein Teil der Schwierigkeiten vielleicht darin, dass die Komplexität des Gehirns überschätzt wird und dadurch unnötige Hemmungen entstehen? Die Vorstellung vom „komplexesten Gebilde des Universums“ kann den Blick auf grundlegende Funktionsprinzipien verstellen.
Aber wie sieht die Realität abseits vom Mythos des „komplexesten Gebildes des Universums“ aus? Betrachtet man Hirnpräparate, beispielsweise Hirngewebeschnitte, fällt die Uniformität der „grau-weißen Masse“ sofort auf (→ Abbildung 1). Die strukturelle Uniformität des Gehirngewebes steht im deutlichen Kontrast zu den hunderten Klassifikationen neurologisch‑psychiatrischer Erkrankungen. Es stellt sich doch sofort folgende Frage: Wie sollen so viele verschiedene Erkrankungen und Ursachenhypothesen plausibel sein, wenn das zugrunde liegende Gewebe in Aufbau und Funktion doch weitgehend uniform ist?
ABBILDUNG 1: EIN HIRNSCHNITT (LATERAL)
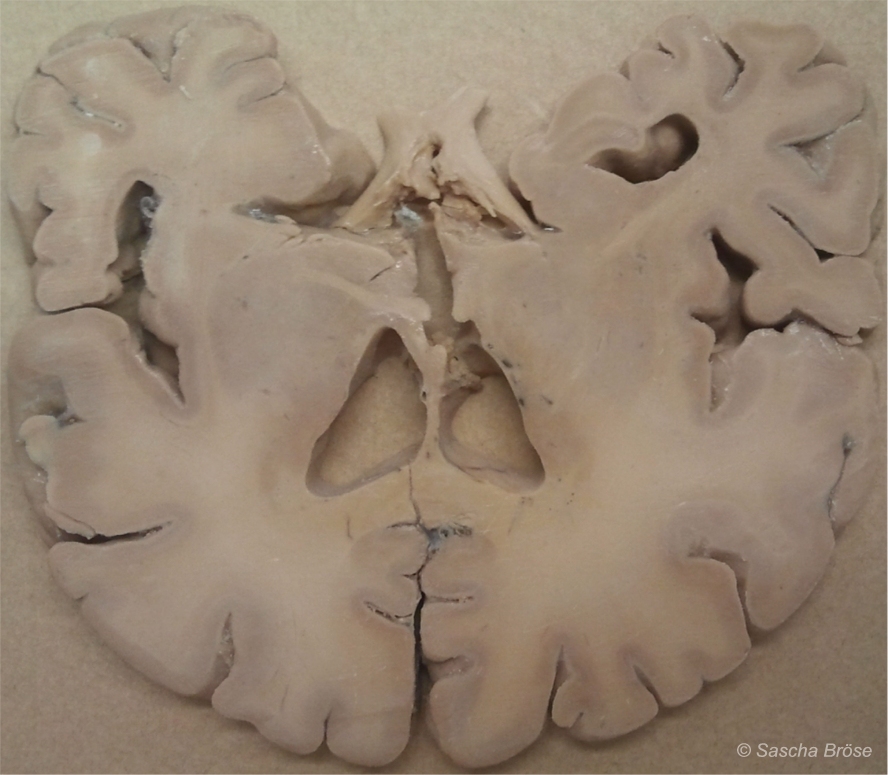
Abbildung 1: Ein Schnitt durch das menschliche Gehirn. Deutlich zu erkennen sind die Hirnwindungen mit den außenliegenden, grauen Bereichen der Nervenzellen. Zwar gibt es eine Menge verschiedener Subtypen von Nervenzellen, in Aufbau und Funktion sind sie grundsätzlich jedoch alle fast identisch. Davon zu unterscheiden ist die innere Substanz der Nervenleitungen (Axone) mit ihren myelinbildenden Gliazellen, die wesentlich heller ist und deshalb „weiße Substanz“ genannt wird. Verglichen mit anderen Organen, beispielsweise einer Niere oder einem Lungenflügel, sieht das zentrale Nervensystem klar strukturiert und geordnet aus, die zerfurchte Struktur entsteht nur aus Platzgründen, denn auf diese Weise konnte die Natur sehr viele Nerven- und Gliazellen auf kleinstem Raum unterbringen. Der ICD-10-Katalog unterscheidet in zwei Kapiteln dennoch knapp 200 Grobkategorien von Erkrankungen mit zahlreichen Unterkategorien, die fast alle das Gehirn betreffen. Sollte man daraus den Schluss ziehen, dass es auch ebenso zahlreiche Erkrankungsursachen auf der primären Organebene gibt? Die Uniformität des Gehirngewebes zeigt: Die Gründe können nur auf relativ wenigen grundsätzlichen Fehlfunktionen beruhen, so dass auch die unterschiedlichen Hirnregionen ausschlaggebend sein müssen, welche Symptome sich manifestieren. Das ist vergleichbar mit einem Multiplikatoreffekt, der leider unzählige Erkrankungsursachen auf der (primären) Organebene suggeriert, die es aber nicht gibt. So gerät man schnell auf eine falsche Fährte.
Übertriebene Ehrfurcht vor dem Gehirn ist kontraproduktiv. Sie behindert, zu neuen Erkenntnissen zu gelangen und macht blind für wesentliche Zusammenhänge. Es ist daher sinnvoll, das Gehirn bewusst als einen „großen Zellhaufen“ zu betrachten, um grundlegende Fehlentwicklungen besser erkennen zu können. Und könnte das Übersehen solcher grundlegenden Fehlentwicklungen nicht eine Ursache dafür sein, dass die medizinische Standardbehandlung vieler neurologisch‑psychiatrischer Erkrankungen kaum Fortschritte macht?
Obwohl Menschen bereits Ende der 1960er Jahre auf dem Mond landeten und heute Milliarden elektronischer Bauteile auf einem winzigen Siliziumchip unterbringen können, scheint die Behandlung von Nervenerkrankungen immer noch in den Kinderschuhen zu stecken. Im Grunde wird das Gehirn immer noch als „Black‑Box“ betrachtet. Die Raumfahrt hätte es wahrscheinlich nicht weit gebracht, wenn dort ebenso vorgegangen wäre: Man muss nicht die Rückseite des Mondes im Maßstab 1:1000 kartografieren, um auf der Vorderseite zu landen.
Hirnstrukturen in der Übersicht
Sinnvoll ist ein komprimiertes Modell des Zentralnervensystems, das eine übersichtliche Zuweisung der Funktionen einzelner Hirnareale ermöglicht und erkennen lässt, welche Regionen für die Entstehung oder den Verlauf bestimmter Nervenerkrankungen entscheidend sein könnten. Im Laufe der Zeit konnte die Hirnforschung verschiedenen Hirnbereichen Funktionen zuordnen, obwohl aufgrund der Verschaltung der Regionen untereinander eine eindeutige funktionelle Abgrenzung nicht immer möglich ist. Dennoch lassen sich zahlreiche Funktionen relativ zuverlässig neurologisch lokalisieren.
Das Gehirn lässt sich in folgende Regionen und Strukturen differenzieren:
- Großhirnhemisphären
- Äußerer Cortex mit den primären und sekundären (Sinnes-)Arealen und dem Assoziationsareal
- Innerer Cortex mit Gyrus cinguli und Gyrus parahippocampalis
- Großhirnkerne (Hippocampus mit Fornix, Mandelkern, Mamillarkörper und Basalganglien)
- Zwischenhirn
- Thalamus
- Hypothalamus
- Hypophyse
- Zirbeldrüse (Epiphyse)
- Stammhirn
- Mittelhirn (Mesencephalon bzw. Oberes Stammhirn)
- Verlängertes Mark (Medulla oblongata bzw. Unteres Stammhirn)
- Kleinhirn
- Cerebellum (Kleinhirn im engeren Sinne)
- Pons (Brücke)
- Aufsteigendes retikuläres Aktivierungssystem/ARAS
- ARAS, ein Teil der Formatio reticularis, ist eine entscheidende Hirnzellenstruktur des Stamm- und Zwischenhirns mit Nervenbahnverzweigungen in viele Hirnregionen
Die Funktionalität bezüglich Sensorik, Motorik, Kognition, Emotionalität, Motivation und Gedächtnis/Lernen lässt sich grob zuordnen, wie die nachfolgenden Ausführungen zeigen.
Großhirnhemisphären
Das Großhirn ist die funktionell vielfältigste Hirnregion und nimmt ca. 80% des Hirnvolumens eines Menschen ein. Zwei funktionelle Teilbereiche werden unterschieden: die stammesgeschichtlich jüngere äußere und die innere Großhirnrinde (auch „Cortex“ genannt) und die älteren Großhirnkerne, die unterhalb der Großhirnrinde angeordnet sind. Diese beiden als „graue“ Substanz bezeichneten Bereiche der Nervenzellkörper bilden zusammen mit der „weißen“ Substanz der Nervenfasern die Großhirnhemisphären.
Die äußere Großhirnrinde steuert die höheren kognitiven Funktionen, beispielsweise Sinnesreizverarbeitung, Intellekt oder Persönlichkeitsmerkmale. Teile der inneren Großhirnrinde und verschiedene Großhirnkerne bilden zentrale Anteile des emotionalen Systems, welches vor allem für Gefühle, Angst, Stressverarbeitung, Antrieb und Gedächtnis zuständig ist. Großhirnkerne übernehmen teilweise ebenfalls Funktionen der Motorik oder sind an der Steuerung von Körperfunktionen beteiligt.
Äußere und innere Großhirnrinde (Cortex) als Bestandteile der Großhirnhemisphären
In der äußeren Großhirnrinde werden Aktivitäten gesteuert, die den ersten großen Funktionsbereich des Gehirns repräsentieren, der hauptsächlich für bewusstes Erleben, Intellekt und Persönlichkeit zuständig ist.
- Primäres sensorisches Sinnesareal:
Zuständig für die erste Verarbeitung von Tast-, Geruchs- und Geschmacksempfindungen.
- Primäres motorisches Areal:
Zuständig für das willentliche Ausführen von Bewegungen des gesamten Körpers ohne den feinmotorischen Anteil.
- Primäres visuelles Sinnesareal:
Zuständig für die erste Verarbeitung der visuellen Wahrnehmung von Formen und Farben.
- Primäres auditives Sinnesareal:
Zuständig für die erste Verarbeitung akustischer Wahrnehmungen von Tönen bzw. Geräuschen.
- Sekundäre sensorische, motorische, visuelle und auditive (Sinnes-)Areale:
Die Informationen der primären Areale werden hier weiterverarbeitet und bewusstgemacht. Zu jedem der vier primären Areale gibt es parallel ein sekundäres Areal.
- Präfrontaler Cortex/Assoziationsareal:
Hier werden weitere hochkomplexe Fähigkeiten (mit-)gesteuert, zum Beispiel Persönlichkeit, Bewusstsein, Kreativität, soziales Verhalten etc. Die Bereiche des präfrontalen Cortex und der Frontallappen sind eng mit Bereichen der Basalganglien und den emotionsverarbeitenden Großhirnbereichen verbunden. Daher ist die Wahrscheinlichkeit einer Beteiligung an emotionalen Prozessen hoch. Vermutlich werden Signale aus dem Zwischenhirn und den tiefer liegenden Großhirnarealen im Assoziationsareal bewusstgemacht, bewertet und intellektuell verarbeitet.
Die beiden Areale des Gyrus cinguli und Gyrus parahippocampalis gehören als Teile der inneren Großhirnrinde ebenfalls zum Cortex.
- Gyrus cinguli (Cingulärer Cortex):
Dieses Areal ist vor allem an der bewussten Wahrnehmung von Gefühlen beteiligt, die in den ihm anatomisch und funktionell vorgelagerten Großhirnkernen autonom entstehen. So gibt es Verbindungen mit dem Mandelkern, die eine Aktivitätssteuerung durch den cingulären Cortex ermöglichen (→ Großhirnkerne).
- Gyrus parahippocampalis:
Auch der benachbarte Gyrus parahippocampalis könnte aufgrund der räumlichen Nähe zum Gyrus cinguli an der Verarbeitung von Affekten beteiligt sein. In der Literatur werden dessen Funktionen jedoch hauptsächlich im Zusammenhang mit dem Gedächtnis, dem visuellen Erkennen der Umgebung oder dem Verstehen sozialer Zusammenhänge beschrieben.
Neben dem Assoziationsareal und dem Gyrus cinguli könnte es weitere Cortex-Areale geben, die Emotionen bewusstmachen und bewerten und in direkter Verbindung mit den tiefer lokalisierten Hirnbereichen stehen, zum Beispiel durch komplexe Verbindungsnetze. Es ist auch eine interessante Frage, ob kognitive und emotionale Bereiche scharf voneinander abgegrenzt sind oder der Übergang fließend verläuft. All das kann derzeit nicht mit Sicherheit beantwortet werden.
Der Gyrus cinguli und die affektiven Anteile des Assoziationsareals sind aufgrund ihrer Beteiligung an emotionalen Vorgängen unbedingt dem affektiven System zuzuordnen.
Großhirnkerne als Bestandteile der Großhirnhemisphären
Zum affektiven System zählen auch die Großhirnkerne Hippocampus mit Fornix, der Mandelkern (Amygdala) sowie die Basalganglien. Die Kerne sind in jeder der beiden Großhirnhemisphären links und rechts vorhanden, treten also paarweise auf, Gyrus cinguli und Gyrus parahippocampalis bilden einen Ring um sie. In den beiden Großhirnkernen werden Affekte und die Angstverarbeitung gesteuert und reguliert, ohne dass sie auf dieser Stufe bereits bewusst werden. Der Hippocampus steuert auch essentielle Körperfunktionen und das Gedächtnis.
Die Großhirnkerne sind von der Entwicklungsgeschichte des Menschen aus betrachtet älter als der für Bewusstsein, Persönlichkeit und Intelligenz verantwortliche, verhältnismäßig junge äußere Cortex. Über diese Hirnkerne verfügten schon höhere Lebewesen in der Frühzeit der erdgeschichtlichen Entwicklung. Ihre Strukturen sind wesentlich filigraner und komplexer aufgebaut im Vergleich zur relativ uniformen Großhirnrinde.
Dem vierten Großhirnkern ‑ dem ebenfalls paarigen Mamillarkörper ‑ wurde früher Funktionen in der Emotionsverarbeitung unterstellt. Aktuellere Forschungen deuten jedoch darauf hin, dass er zusammen mit dem Hippocampus ausschließlich Aufgaben bei Gedächtnisvorgängen übernimmt. Beide Mamillarkörper sind auch anatomisch mit dem Hippocampus verbunden, was auf eine Zusammenarbeit hindeutet.
Durch die Übernahme verschiedener neurologischer Grundfunktionen in denselben Hirnegionen kann es zu korrelativen Phänomenen kommen: Bestimmte kognitiv-intellektuelle oder motorische Leistungen (zum Beispiel die Erinnerungs- und Konzentrationsfähigkeit) erfolgen in spezialisierten Großhirnkernen, die gleichzeitig auch für die Emotionsverarbeitung zuständig sind. Unterstellt man, dass Dysfunktionen emotionsverarbeitender Areale an depressiven Symptomen beteiligt sind, ist es nicht verwunderlich, dass viele von einer Depression Betroffene auch über Konzentrationsunfähigkeit, eine verminderte Merkfähigkeit oder gestörte Körperfunktionen klagen. HIer besteht kein kausaler Zusammenhang zwischen der gestörten Körperfunktion und der Affekterkrankung, sondern beide gehen auf eine Erkrankung von Hirnregionen zurück, die sowohl Affektivität als auch Körperfunktonen bzw. Gedächtnsivorgänge regulieren.
- Hippocampus mit Fornix:
Der paarige Hippocampus („Hippocampi“) ist die zentrale Schaltstelle des affektiven Systems. Er sorgt mit dem Fornix auch für die Übertragung von Informationen an das Langzeitgedächtnis.
An der Entstehung von Aufmerksamkeit, sozialem Verhalten, Lernvorgängen, der Verarbeitung von Angst und der Körperwahrnehmung ist der Hippocampus zentral beteiligt. Seine Mitverantwortung für die Entstehung oder Verarbeitung von Affekten ist wahrscheinlich.
Obwohl es als sicher gilt, dass weitere Areale zur Neurogenese fähig sind und neue Nervenzellen hervorbringen, ist diese Funktion für den Hippocampus sehr gut belegt. Neben seiner Aufgabe, Erinnerungen zwischenzuspeichern und über den Fornix weiterzuleiten, wofür eine Neurogenese unabdingbar ist, könnte der Hippocampus auch die Reparatur des Hirngewebes in anderen Arealen steuern.
- Mandelkern:
Der auch als Amygdala bezeichnete paarige Hirnkern spielt ‑ zusammen mit dem Hippocampus ‑ eine zentrale Rolle bei der Entstehung und Verarbeitung von Angst und Affekten.
- Basalganglien:
Die auch als Stammganglien bezeichneten paarigen Großhirnkerne gehören ebenfalls zu den älteren Großhirnstrukturen. Auch hier ist das Verständnis ihrer Bedeutung noch sehr beschränkt. Ihnen werden zahlreiche Funktionen zugeschrieben, vor allem die Steuerung der willkürlichen (Grob-)Motorik. Heute ist bekannt, dass sie auch an emotionalen Vorgängen beteiligt sind, unter anderem an Affekten, Antrieb und Willenskraft. Ein Beispiel ist der Nucleus accumbens als Teil des „Belohnungszentrums“ mit seinen vielen Dopaminrezeptoren, der unter anderem bei der Entstehung von Suchterkrankungen und Morbus Parkinson eine Rolle spielt.
Ein weiteres Basalganglienareal, das Corpus striatum, spielt im Zusammenhang mit Affekten und Antrieb ebenfalls eine Rolle. So basiert Chorea Huntington, eine neurodegenerative Erkrankung mit Störungen der Grob- und Feinmotorik als Hauptsymptomatik, vor allem auf der Zerstörung des Corpus striatum und geht mit Affekt-, Antriebs- und Persönlichkeitsstörungen einher.
Eine Aufgabe der Basalganglien besteht auch in der Weiterleitung von Sinneseindrücken aus den Großhirnarealen an den Thalamus (→ Zwischenhirn).
Zwischenhirn
Das Zwischenhirn hat drei Bestandteile: Thalamus, Hypothalamus und Hypophyse und bedient mit der zum affektiven System gehörenden Emotions- bzw. Aufmerksamkeitssteuerung einerseits und der Körperfunktionssteuerung andererseits zwei Hauptfunktionsbereiche des Gehirns.
- Thalamus:
Sinnbildlich als „Tor zum Bewusstsein“ bezeichnet. Nervenreize aus dem Körper werden hier autonom bewertet und an die zuständigen Hirnrindenareale weitergeleitet („umgeschaltet“). Der Thalamus entscheidet damit, welche Reize mit welcher Intensität in der Großhirnrinde bewusst wahrgenommen werden. Er trifft seine Entscheidungen mit Hilfe von Informationen aus anderen Hirnarealen, die ihn ständig darüber informieren, was gerade wichtig ist. Damit findet auf der Thalamus-Ebene eine erste unbewusste Informationsverarbeitung statt.
Narkotika wirken oftmals in dieser Gehirnregion, auch sind viele Opiatrezeptoren im Thalamus lokalisiert. Fehlsteuerungen des Thalamus werden daher sowohl mit Schizophrenie bzw. Psychosen als auch der Manie in Verbindung gebracht. Insbesondere die Nuclei anterioventrales des Thalamus werden zum emotionalen System gezählt.
- Hypothalamus und Hypophyse:
Der Hypothalamus ist unterhalb des Thalamus angeschlossen und das wichtigste Steuerzentrum des vegetativen Nervensystems mit seinen nicht willentlich beeinflussbaren autonomen Regelkreisen. Beispiele sind die Regulation von Körpertemperatur und Blutzuckerspiegel, die Steuerung der Nahrungsaufnahme und die Schlafregulation. Gemeinsam mit der an seinem Ende angehängten Hypophyse steuert er auch die Hormonregulation. Daher spricht man von der Hypothalamus-Hypophysen-Achse, deren Störungen erhebliche Auswirkungen auf den emotionalen und körperlichen Gesundheitszustand haben können.
Zirbeldrüse (Epiphyse cerebri)
Die an der Oberseite des Thalamus liegende kleine Drüse ist für die Produktion des Hormons Melatonin verantwortlich, das in der Nacht bzw. bei Dunkelheit verstärkt produziert wird und an der Steuerung des Tag‑Nacht-Rhythmus beteiligt ist. Melatonin stellt eine Vorstufe des Neurotransmitters Serotonin dar. Fehlsteuerungen der Epiphyse werden mit der sogenannten „Winterdepression“ bzw. Saisonalen Depression (SAD) in Zusammenhang gebracht. Eine gestörte Melatoninproduktion führt eventuell zu Störungen des Schlafrhythmus.
Die Epiphyse wird in der Literatur manchmal dem Zwischenhirn zugeordnet.
Mittelhirn (Mesencephalon bzw. Oberes Stammhirn)
Die relativ kleine Hirnregion ist in eine Vielzahl von Kernen differenziert und steuert vor allem automatisierte Bewegungsabläufe. Ebenfalls werden Impulse der Augen bzw. Ohren und von Oberflächenrezeptoren der Haut an andere Hirnbereiche weitergeleitet. Das Mittelhirn ist daher auch an der Wahrnehmung von Sinnesreizen und Schmerzen beteiligt.
Die wichtigsten Mittelhirnkerne sind: Nucleus ruber (rote Substanz) und die Substantia nigra (schwarze Substanz). Eine Erkrankung der Substantia nigra ist ein Hauptgrund des Morbus Parkinson, denn hier wird ein großer Teil des wichtigen Neurotransmitters Dopamin produziert. Der ist nicht nur für Bewegungsprozesse (Motorik) verantwortlich, auch an der Enstehung und Steuerung von Antrieb bzw. Aktivitätsdrang wesentlich.
Die zum Mittelhirn gehörenden Raphe-Kerne produzieren darüber hinaus Serotonin.
Medulla oblongata (Verlängertes Mark bzw. Unteres Stammhirn)
Direkt oberhalb des Rückenmarks beginnt übergangslos die Medulla oblongata und markiert den Beginn des Gehirns. Auch hier werden ‑ wie beim Mittelhirn ‑ nicht willentlich beeinflussbare (autonome) Regelkreise gesteuert, beispielsweise der Blutkreislauf, die Atmung oder der Niesreflex. Eine direkte Beteiligung dieser Hirnregion an emotionalen Vorgängen ist eher unwahrscheinlich.
Da das aufsteigende retikulär‑aktivierende System (ARAS) seinen Ursprung auch im unteren Stammhirn hat (→ Formatio reticularis) und die dort befindlichen Raphe‑Kerne ‑ wie auch die Raphe‑Kerne des Mittelhirns ‑ für die Synthese des Neurotransmitters Serotonin mitverantwortlich sind, würden Teile der Medulla oblongata die Entstehung und Steuerung von Emotionen vielleicht beeinflussen, sofern ‑ siehe oben ‑ Serotonin hier eine Bedeutung hat. Es hängt auch davon ab, auf welche Weise Serotonin emotionale Vorgänge generell beeinflusst und ob das in der Medulla oblongata synthetisierte Serotonin dabei überhaupt eine Rolle spielt (→ Abschnitt 1.1 f.).
Kleinhirn mit Brücke
Obwohl über eine Beteiligung des Kleinhirns an kognitiven Fähigkeiten diskutiert wird, scheint dieser Teil des Gehirns in erster Linie mit der Feinsteuerung von Bewegungsabläufen (Feinmotorik) und der Steuerung des Gleichgewichts in Verbindung zu stehen. Erlernte Bewegungsabläufe, zum Beispiel das Radfahren oder das Spielen eines Musikinstruments, sind hier gespeichert.
Störungen des Kleinhirns führen daher zu einem Verlust der Bewegungskoordination, jedoch nicht zum Ausfall der Bewegungsabläufe und äußern sich dann in ungelenk wirkenden Bewegungen oder Sprechstörungen, sofern die grobmotorischen Zentren der Basalganglien noch ausreichend aktiv sind.
Die Brücke (Pons) bildet funktionell eine Einheit mit dem Kleinhirn. Sie liegt zwischen Mittelhirn und Medulla oblongata und leitet die Nervenimpulse aus den Großhirnhemisphären an die Kleinhirnregionen weiter.
Neueste Forschungen vom März 2022 zeigen, dass das Kleinhirn mit verschiedenen Bereichen des Großhirns kommuniziert und bei der Abspeicherung emotionaler Eindrücke vermutlich eine Rolle spielt (Quelle: Matthias Fastenrath et al., Human cerebellum and corticocerebellar connections involved in emotional memory enhancement, University of California Irvine, Irvine, USA, https://www.pnas.org/doi/...). Es könnten daher in Zukunft noch weitere Funktionen des Kleinhirns entdeckt werden, die bei der Emotionsverarbeitung eine Rolle spielen und die Sicht auf diesen Teil des Gehirns verändern.
Eine Beteiligung von Kleinhirn und Brücke an der Entstehung und Verarbeitung von Emotionen ist daher nicht ganz auszuschließen, aber aus heutiger Sicht eher unwahrscheinlich.
Aufsteigendes retikulär-aktivierendes System (ARAS)
Interessant ist die Formatio reticularis als ein weit verzweigtes und schwierig abzugrenzendes Nervennetz des Hirnstamms und des Zwischenhirns. Sie ist daher Bestandteil von Thalamus, Mittelhirn und Medulla oblongata. Ihre absteigenden Neuronen dringen bis ins Rückenmark vor, ebenfalls bestehen Verbindungen in das Kleinhirn. Ihre aufsteigenden Neuronen und Neuronenfortsätze führen über das Zwischenhirn und Mittelhirn zum Nucleus accumbens der Basalganglien. Die als mesolimbische Bahn bezeichnete zentrale dopaminerge Verbindung startet im Tegmentum des Mittelhirns (Mittelhirnhaube).
Die aufsteigenden Nervenbahnen regulieren das Erregungsniveau für den Wachzustand und reichen bis hoch in Cortexbereiche. Dieser Teil der Formatio reticularis wird daher auch als aufsteigendes retikulär‑aktivierendes System (ARAS) bezeichnet. Ohne ein funktionierendes ARAS ist kein Bewusstsein möglich.
Die Formatio reticularis ist auch für die Verarbeitung von Sinneseindrücken und Emotionen zuständig. Letztere erfolgt durch die Verknüpfung von Bereichen des Hypothalamus und des Mittelhirns mit den affektrelevanten Zentren der Basalganglien, dort vor allem mit dem Nucleus accumbens.
Viele Neuroforscher betrachten das ARAS als eine Schlüsselstruktur, weil es die notwendige Aktivierungsgrundlage für jedes phänomenal‑subjektive Erleben bereitstellt. Ohne die tonische Wachheitsregulation des ARAS können weder bewusste Wahrnehmung noch die höheren Netzwerke des Selbst- und Individualitätsbewusstseins aktiv werden. Damit spielt das ARAS eine zentrale Rolle für das Verständnis jener Phänomene, die das erlebbare Sein ermöglichen: Das ARAS stellt die notwendige „technische“ Grundlage dar, während das sogenannte Default Mode Network (DMN) die neuronale Architektur des Selbst- und Individualitätsbewusstseins bildet.
Übersicht der verschiedenen Hirnareale
Abbildung 2 stellt das Gehirn schematisch in der Übersicht dar, die nicht die tatsächlichen Größenverhältnisse der Areale oder deren Lage korrekt abbildet.
ABBILDUNG 2: DIE VERSCHIEDENEN HIRNAREALE („GEHIRNLANDKARTE“)
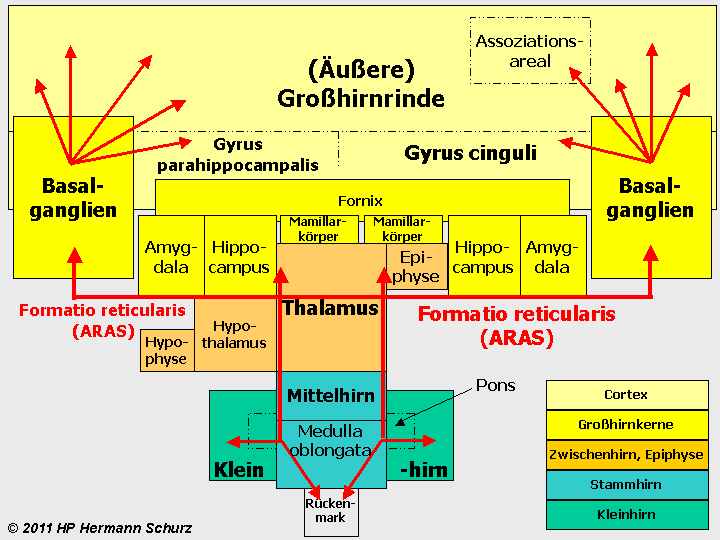
Abbildung 2: Eine schematische Darstellung der verschiedenen Hirnregionen. Das Rückenmark ist Teil des zentralen Nervensystems (ZNS), aber nicht Bestandteil des Gehirns, das übergangslos mit der Medulla oblongata beginnt. Hellgelb: Großhirnrinde; Dunkelgelb: untere Großhirnkerne; Orange: Zwischenhirn (einschließlich Hypophyse) und Epiphyse; Türkisblau: Stammhirn; Grün: Kleinhirn mit Brücke (Pons). Die Nervenbahnen der Formatio reticularis (rote Pfeillinien) sind vor allem im Tegmentum des Mittelhirns und im Thalamus lokalisiert, reichen aber als aufsteigendes, retikulär‑aktivierendes System (ARAS) über die Basalganglien (dort vor allem im Nucleus accumbens) bis in verschiedene Regionen der Großhirnrinde. Nach unten führen die Bahnen der Formatio reticularis bis ins Kleinhirn bzw. Rückenmark.
1.3.2 Affekte verarbeitende Gehirnareale
Anhand von Gehirnlandkarte (→ Abbildung 2) und den Funktionsbeschreibungen werden in der nächsten Abbildung Gehirnbereiche markiert, die für die Entstehung und Modulation von Affekten/Emotionen, Antrieb und Angst verantwortlich sind, einschließlich einer groben Bewertung ihres Beteiligungsgrads an diesen Vorgängen. Im Umkehrschluss ergibt sich eine Rangfolge der Relevanz verschiedener Hirnareale an der Genese einer affektiven Erkrankung.
In seiner Gesamtheit stellt das dunkel markierte Areal das affektive System des zentralen Nervensystems dar (→ Abbildung 3). Die Gewichtung der Areale ist durch unterschiedliche Grauwerte gekennzeichnet:
- Die schwarz markierten Gehirnregionen sind primär für die autonome Entstehung, Verarbeitung, Steuerung oder Wahrnehmung von Affekten, Emotionen, Ängsten und Antrieb zuständig. Dazu gehören ein Teil des unteren Cortex (Gyrus cinguli), der Hippocampus mit dem Fornix sowie die Amygdala. Der Gyrus cinguli fungiert als zentraler Integrator zwischen limbischer Affektentstehung und vegetativer Reaktion. Die Amygdala ist der Trigger für autonome affektive Reaktionen wie Furcht, Alarm und aversive Valenz. Der Hippocampus liefert die zeitlich‑räumliche Kontextualisierung affektiver Reize, die für die Angstregulation entscheidend ist. Der Fornix stellt die Hauptausgangsbahn des Hippocampus in Richtung Cortex dar und ist daher funktionell eng mit dessen affektiver Rolle verknüpft.
- Die dunkelgrau markierten Gehirnregionen sind sekundär für die autonome Entstehung, Verarbeitung oder Steuerung von Affekten, Emotionen, Ängsten und Antrieb verantwortlich. Dazu gehören die Basalganglien sowie der Thalamus. Die Basalganglien modulieren Antrieb, Initiation und Motivation und beeinflussen damit die energetische Komponente affektiver Zustände. Der Thalamus übernimmt eine Art Türsteherfunktion, indem er filtert, welche sensorischen Informationen affektive Relevanz erhalten und an die entsprechenden limbischen und kortikalen Areale weitergeleitet werden.
- Hypothalamus, Hypophyse, Epiphyse cerebri und das Assoziationsareal der äußeren Großhirnrinde beeinflussen die autonome Entstehung, Verarbeitung oder Wahrnehmung von Affekten, Emotionen, Ängsten und Antrieb als endokrine, vegetative, circadiane und bewertend‑interpretierende Modulatoren. Damit bilden sie ein tertiäres Affektsystem und sind dementsprechend hellgrau markiert. Der Hypothalamus ist der oberste Regler vegetativer Affektantworten (Stressachse, HPA‑Achse), während die Hypophyse rein endokriner Effektor ist. Die Beteiligung der Epiphyse ist unklar; sie wird dennoch einbezogen, weil circadiane Rhythmen affektive Zustände modulieren können. Da Nervenbahnen der Formatio reticularis vom Mittelhirn über den Nucleus accumbens der Basalganglien bis in Cortex‑Regionen reichen und dort auch Dopamin synthetisiert wird, zählt das Mittelhirn ebenfalls zur tertiären Struktur des affektiven Systems. Im Assoziationsareal werden Affekte nicht erzeugt, sondern bewertet, interpretiert und bewusst gemacht.
- Die weiß belassenen Bereiche sind nach dem jetzigen Stand (April 2026) nicht an der Entstehung und Verarbeitung von Affekten, Emotionen, Ängsten und Antrieb beteiligt. Beim Gyrus parahippocampalis, der primär Gedächtnis- und Szenenverarbeitung betreibt und keine autonome Affektentstehung zeigt, sowie bei den Mamillarkörpern, die vor allem Gedächtnisinhalte verarbeiten, symbolisieren die Fragezeichen einen Rest von Unklarheit. Da in den Raphe‑Kernen der Medulla oblongata ein Teil des Serotonins produziert wird, könnten diese Kerne eine modulatorische Rolle bei Affekten spielen; eine autonome Affektentstehung findet dort jedoch nicht statt. Auch die genaue Funktion des Serotonins ist weiterhin ungeklärt. Daher ist die Medulla oblongata ebenfalls mit einem Fragezeichen versehen.
ABBILDUNG 3: DIE AFFEKTIV-EMOTIONALEN GEHIRNAREALE (FUNKTIONSMODELL)
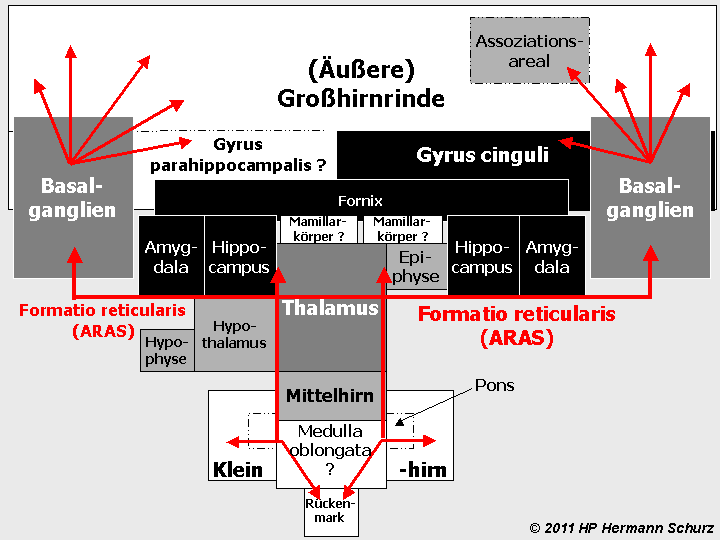
Abbildung 3: Während Abbildung 2 die anatomische Makroorganisation des Gehirns schematisch darstellt, zeigt Abbildung 3 eine funktionelle Gewichtung derjenigen Areale, die nach heutigem Kenntnisstand an der autonomen Entstehung und Verarbeitung von Affekten beteiligt sind. Alle dunkel markierten Areale sind hier involviert - je dunkler das Areal markiert ist, desto stärker ist es geschätzt beteiligt. Einen starken Anteil haben Gyrus cinguli, Amygdala, Hippocampus und Fornix (Schwarz). Von einer mittelgradigen Beteiligung ist bei den Basalganglien und dem Thalamus auszugehen (Dunkelgrau), während Hypophyse, Hypothalamus und Epiphyse durch ihre autonomen Steuerungsaufgaben beteiligt sind (Hellgrau). Das Kleinhirn mit Brücke und das nicht zum Gehirn zählende Rückenmark sind unbeteiligt. Mamillarkörper und Gyrus parahippocampalis wurden aufgrund ihrer unsicheren Zuordnung jeweils mit einem Fragezeichen versehen, sind wahrscheinlich nicht an der Affektverarbeitung beteiligt. Ähnliches gilt für die Medulla oblongata, denn deren Raphe-Kerne sind ein Ort der Serotoninproduktion und zählen zur Formatio reticularis, die fast alle emotionalen Bereiche durchzieht. Bei Funktionsstörungen in Arealen, durch die das Netz der Formatio reticularis führt, kann es zu Unterbrechungen oder Veränderungen von Reizen kommen.
Die Bewertungen der Makroebene hinsichtlich der Affektverarbeitnung führen zur dritten (und letzten) Hypothese.
- Hypothese: Affektive Störungen entstehen durch Funktionsstörungen in jenen Hirnarealen, die autonom an der Entstehung, Verarbeitung oder Modulation von Affekten beteiligt sind. Die Schwere und Ausprägung der Störung hängt davon ab, welche primären, sekundären oder tertiären Areale betroffen sind und in welchem Ausmaß ihre Funktion eingeschränkt ist. Durch die dichte Vernetzung über die Formatio reticularis (ARAS) können Funktionsstörungen einzelner Areale systemweite Effekte auslösen.
Bei einer affektiven Störung können
- primär die Hirnregionen Gyrus cinguli, Hippocampus mit Fornix und Amygdala (Mandelkern),
- sekundär die Basalganglien, der Thalamus und das Assoziationsareal und
- tertiär die Hypothalamus-Hypophysen-Achse, die Epiphyse cerebri und das Mittelhirn
von den in den Hypothesen 1 und 2 beschriebenen Funktionseinschränkungen betroffen sein.
Die oberen Verbindungsbahnen der Formatio reticularis (ARAS) durchziehen nahezu alle affektrelevanten Hirnregionen und sind daher in besonderem Maße an Affekten und deren Störungen beteiligt. Funktionsstörungen einzelner Areale können über diese Verknüpfungen unmittelbare Auswirkungen auf alle mit dem ARAS verbundenen Strukturen haben.
Ein Zusammenhang der Fehlsteuerungen bestimmter Gehirnregionen mit der Entstehung von Psychosen als weiterem Merkmal affektiver Erkrankungen ist wahrscheinlich. Das betrifft zum Beispiel das Assoziationsareal oder den für die Filterung von Sinneseindrücken zuständigen Thalamus.
Die Betroffenheit mehrerer Hirnbereiche gleichzeitig ist nicht zwingend, Funktionsstörungen können auch auf ein einzelnes Areal begrenzt sein. Sind mehrere Bereiche involviert, ist zudem wahrscheinlich, dass der Grad der Funktionseinschränkungen unterschiedlich ausfällt. Die zentrale Rolle der Formatio reticularis erschwert klare Zuordnungen und eindeutige Abgrenzungen.
1.4 Verminderte neuronale Leistungsfähigkeit und Drei-Stufen-Basismodell ▲
Affektive Erkrankungen entstehen, wenn sich informationsverarbeitende Neuronen bzw. Gliazellen in affektverarbeitenden Hirnarealen (→ Abschnitt 1.3 mit Hypothese 3) funktionell ungünstig verändern (→ Abschnitt 1.2 mit den Hypothesen 1 und 2).
Vor allem die ersten beiden Hypothesen sind noch nicht ausreichend exakt formuliert. Kennzeichen von Dysfunktionalität sind komplex und können die gesamte Reizverarbeitungskette betreffen. Es ist daher noch zu klären, was „funktionell ungünstig verändern“ in diesem Zusammenhang bedeutet.
Charakteristiken degenerativer Entwicklungen
Bei einer neurologischen Erkrankung befinden sich funktionelle Störungen nicht überall auf einem einheitlichen Niveau, eine solche Annahme ist unrealistisch. Sie sind eher durch unterschiedliche Zustände gekennzeichnet. Diese können ‑ zumindest theoretisch ‑ einer Skala zugeordnet werden, und reichen von „leichten Einschränkungen der Zellaktivitäten“ bis „Zelltod“. Auch andere neuronale Leistungsmerkmale ‑ wie Neuronenvernetzung oder Zelldichteanforderungen ‑ spielen bei der Informationsverarbeitung entscheidende Rollen. Eine Definition eingeschränkter neuronaler Leistungsfähigkeit sollte nur folgende drei Grundmerkmale umfassen:
- Einschränkungen der Neuronen- und Gliazellenfunktionen mit verschiedenen Intensitäten
- Zu geringe bzw. fehlerhafte Neuronenvernetzung
- Zu geringe Neuronen- bzw. Gliazellendichte
Die Merkmale sind ebenfalls voneinander abhängig. Ungünstige Aktivitätsveränderungen einzelner Neuronen wirken sich aufgrund der Vernetzung auf andere Neuronen negativ aus. Auch für zeitliche Abhängigkeiten spricht vieles. Die Entwicklung ist daher mit großer Wahrscheinlichkeit durch einen kontinuierlichen Prozess gekennzeichnet, der mit leichten Störungen einzelner Zellen beginnt und mit deren komplettem Verschwinden endet und drei Stufen umfasst (→ Abbildung 4).
- Stufe 0: Ausreichende neuronale Leistungsfähigkeit
Nerven- und Gliazellen erfüllen ihre Funktionen vollständig und situationsangemessen. Nervenzellen weisen typische Reizverarbeitungsaktivitäten auf, eine ausreichende Vernetzung und intakte Vernetzungsmuster. Die Dichte bzw. Anzahl von Nerven- und Gliazellen ist ausreichend.
- Stufe 1: Funktionsstörungen
Einzelne Nerven- und Gliazellen beginnen mit einer unangemessenen pathologischen Zu- oder Abnahme ihrer funktionellen, nach außen gerichteten Aktivitäten, es kann zu verschiedenen Störungen der Reizverarbeitung, Reizentstehung, Reizweiterleitung oder Reizübertragung kommen, die sich von Zelle zu Zelle unterscheiden. Im mittel- bis langfristigen Verlauf nehmen die Veränderungen in den schon betroffenen Zellen ggf. kontinuierlich zu und erfassen darüber hinaus immer mehr Zellen.
- Stufe 2: Vernetzungsabbau
Zunehmend gestörte Neuronen können ‑ auch aufgrund ungünstiger Gliazellenveränderungen ‑ Verbindungen mit anderen Neuronen nicht mehr aufrechterhalten und reduzieren ihre Vernetzung.
- Stufe 3: Nerven- und/oder Gliazellenabbau
In letzter Konsequenz stellen immer mehr Hirnzellen ihre Aktivitäten ein, und es kommt zum Zelltod (Apoptose). Im günstigsten Fall werden abgestorbene Zellen vom Immunsystem beseitigt, im ungünstigsten Fall wird das gesunde Gewebe durch nicht abbaubare, abgestorbene Zellreste belastet.
ABBILDUNG 4: DREI-STUFEN-BASISMODELL
Abbildung 4: Auf Stufe 0 weisen Neuronen (und Gliazellen) ausreichende Zellfunktionen und Zellendichte bzw. -anzahl auf, die Neuronen sind ausreichend vernetzt. Stufe 1 zeigt erste Aktivitätsstörungen der grau markierten Zellen, was sich in verschiedenen nach außen sicht- oder messbaren Störungen zeigen kann. Die Verbindungen zu anderen Nervenzellen sind noch stabil. Auf Stufe 2 gehen Neuronenverbindungen nach und nach verloren. Auf Stufe 3 stirbt ein Teil der Zellen ab, womit auch deren restliche Verbindungen verloren sind, das System ist sichtbar reduziert.
Weitere Randbedingungen
Das Drei‑Stufen‑Basismodell konkretisiert die einfachen Erklärungen der Hypothesen 1 und 2, ist aber immer noch eine sehr vereinfachte Darstellung eines degenerativen Veränderungsprozesses. Zum Verständnis realer Situationen sind einige Ergänzungen notwendig:
- Dichte, Anzahl und Vernetzung
Hirnareale können sich hinsichtlich ihrer jeweiligen Anforderungen an Zellendichte, Zellenanzahl und Neuronenvernetzung unterscheiden.
- Unterschiedliche Verlaufsentwicklung
Degenerative Verläufe entwickeln sich in verschiedenen Hirnarealen autonom und unterschiedlich. Ein stetiger Verlauf von Stufe 1 zur Stufe 3 ist ebenfalls nicht zwingend. Der Verlauf kann jederzeit zum Stillstand kommen. Eine Umkehrung ist möglich. Durch beschleunigte Entwicklungen kann der Eindruck übersprungener Stufen entstehen.
- Individuelle Wahrnehmungen
Die Wahrnehmungen kognitiver oder affektiver Veränderungen können aufgrund individueller degenerativer Entwicklungen sehr unterschiedlich sein.
- Embryogenese/Neurulation
Störungen der Zellaktivitäten, -vernetzung und ‑dichte sind auch während der vorgeburtlichen Nervensystembildung möglich.
1.5 Kausale Theorie: Primärursachen affektiver Erkrankungen ▲
Die Verbindung von Drei-Stufen-Basismodell mit funktionaler Gehirnlandkarte ergibt ein vollständiges Kausalmodell:
Affekterkrankungen ‑ wie Depression, Manie oder Bipolarität ‑ beruhen auf den im Drei‑Stufen‑Basismodell beschriebenen Funktionsstörungen von Neuronen und Gliazellen in den Affekte verarbeitenden Hirnarealen, wobei drei Kategorien von Arealen nach dem geschätzten Grad ihrer Beteiligung (stark, weniger und gering involviert) unterschieden werden.
Stark involvierte Areale sind Gyrus cinguli, Hippocampus, Fornix und Amygdala.
Weniger involvierte Areale sind Basalganglien, Thalamus und Assoziationsareal.
Gering involvierte Areale sind Hypothalamus-Hypophysen-Achse, Epiphyse und Mittelhirn.
Das aufsteigende, retikulär-aktivierende System (ARAS) der Formatio reticularis verbindet die Affekte verarbeitenden Hirnareale miteinander. Daher ist auch die Beteiligung eines dysfunktionalen ARAS am Erkrankungsprozess wahrscheinlich.
Diese einfachen Hypothesen erfüllen aufgrund weniger Annahmen die Anforderungen des wissenschaftlichen Sparsamkeitsprinzips, auch als „Ockhamsches Rasiermesser-Prinzip“ oder Prinzip der Parsimonie bezeichnet, nach der die Wahrscheinlichkeit des Zutreffens einer Theorie mit ihrer Einfachheit steigt unter der Voraussetzung, dass diese Einfachheit nicht unangemessen gesteigert wird: So wenig wie möglich und so viel wie nötig.
Sind die kausaltheoretischen Hypothesen plausibel?
Wenn es gelänge, bekannte Charakteristiken Affektiver Störungen auf der Basis des Kausalmodells zumindest grob nachzuvollziehen, wäre das ein erster Hinweis auf die Plausibilität der Hypothesen. Beispielhaft soll das nun anhand folgender Merkmale erfolgen:
- psychosomatischer Phänomene,
- der larvierten Depression als psychosomatischer Sonderfall,
- Symptomarten und Symptomanzahl (Symptomvielfalt),
- Erkrankungsintensität,
- Resilienz vs. Vulnerabilität,
- allgemeiner Chronifizierung und
- der Entwicklung von der depressiven Verstimmung zur Depression als Ausdruck einer speziellen Chronifizierung affektiver Erkrankungen.
Die Analysen sind auch hier wieder grundlegend ohne zu sehr ins Detail zu gehen, die Erklärungen und Modelle dementsprechend bewusst einfach formuliert bzw. konstruiert und zeigen nur die grobe Richtung auf. Auch hier ist Ockhams Rasiermesserprinzip der vorgegebene Rahmen.
Psychosomatische Phänomene kausaltheoretisch betrachtet
Der Fachbegriff Psychosomatik ist eine Kombination der Begriffe Psyche und Körper (griechisch sṓma). Die Psychosomatik beschäftigt sich mit Zusammenhängen und Wechselwirkungen zwischen Psyche und Körper. Ungelöst ist in vielen Fällen die Frage, wie diese Zusammenhänge zu begründen sind.
Hinweise darauf, dass sich Wechselwirkungen aufgrund hirnorganisatorischer Zusammenhänge ergeben, kann der kausaltheoretische Ansatz geben, denn die funktional bewertete Gehirnlandkarte (→ Abbildung 3) legt eine Organisation in drei übergeordnete Funktionsbereiche nahe, wobei der dritte für die Affektsteuerung zuständige Funktionsbereich eine Besonderheit aufweist:
- Der erste Bereich des Gehirns umfasst die kognitiven Anteile, also bewusstes Wahrnehmen, bewusstes Handeln und die Persönlichkeit, die in der äußeren und inneren Großhirnrinde (Cortex) gesteuert werden.
- Der zweite Bereich des Gehirns steuert autonome Körperfunktionen, Bewegungen und Gedächtnis und ist sowohl in den Großhirnkernen unterhalb des Cortex, zu denen Basalganglien, Hippocampi, Fornix und Mamillarkörper zählen, als auch im Zwischenhirn einschließlich Hypophyse und Epiphyse, im Stammhirn mit Mittelhirn und verlängertem Mark (Medulla oblongata) und im Kleinhirn mit Brücke lokalisiert. Erster und zweiter Funktionsbereich bilden das Gehirn strukturell vollständig ab, denn der dritte Bereich stellt keine eigenständigen Strukturen, sondern ist in beide Bereiche strukturell integriert.
- Dieser dritte Bereich ‑ und der hier entscheidende ‑ ist für die Verarbeitung von Affekten, Angst, Emotionen und Antrieb zuständig. Dessen Strukturen befinden sich fast alle im Zentrum des Gehirns zwischen den Bereichen 1 und 2 und ihnen ist gemein, dass sie nicht unabhängig von diesen sind. In Richtung des Cortex gibt es Überschneidungen mit dem ersten (kognitiven) Funktionsbereich und in der Gegenrichtung hin zum Rückenmark bzw. verlängerten Mark gibt es Überschneidungen mit dem für Körperfunktionen zuständigen zweiten Funktionsbereich. Die dem dritten Funktionsbereich zugeordneten Hirnareale sind nicht ausschließlich für die Verarbeitung von Affekten zuständig, sie sind immer funktional mit einem der beiden anderen Bereiche verwoben.
Diese spezielle Organisation des Gehirns sagt sehr viel aus über potentielle Zusammenhänge zwischen Affekten, affektiven Erkrankungen und körperlichen Symptomen:
- Zu den im oberen Teil des Affekte steuernden Funktionsbereichs 3 gehören die zum Großhirn zählenden Areale Gyrus cinguli, das Assoziationsareal und ggf. der Parahippocampus, die parallel auch zum kognitiven Funktionsbereichs 1 gehören.
Gyrus cinguli und Parahippocampus erhalten Reize der darunterliegenden affektverarbeitenden Areale, die auf diese Weise in das Bewusstsein vordringen. Ebenfalls werden Reize an das Assoziationsareal des äußeren Cortex weitergeleitet, um dort bewusst intellektualisiert und bewertet zu werden.
- Der untere Teilbereich des Affekte steuernden Funktionsbereichs 3 ist parallel für somatische Funktionen (Körper-, Bewegungs-, Lern- und Gedächtnisfunktionen) des Bereichs 2 zuständig. Das gilt für die Basalganglien, die Amygdala, für die Hippocampi mit Fornix, für den Thalamus, Hypothalamus und die Hypophyse, für das Mittelhirn und die Epiphyse, ggf. auch die Mamillarkörper.
Dass Affektverarbeitung und die Steuerung körperlicher Funktionen zu einem großen Teil in denselben Hirnstrukturen stattfinden, bildet auf der hirnorganischen Ebene genau das umgangssprachlich als „Verbindung von Körper und Seele“ bezeichnete Phänomen ab. Hier können Körperreaktionen bzw. Körperstörungen auf den affektiven Bereich übertragen werden und umgekehrt.
Darüber hinaus sind beide Hirnbereiche durch übergeordnete netzartige Strukturen, wie der Formatio reticularis, miteinander verknüpft ‑ und schaffen damit weitere „Verbindungen von Körper und Seele“.
Die Erklärungen für Zusammenhänge zwischen körperlichen und psychischen Phänomenen sind auf hirnorganischer bzw. -organisatorischer Ebene damit eigentlich trivial. Dass das kausaltheoretische Modell eine so einfache Erklärung zulässt, ergibt sich auch aus der Anwendung von Ockhams Parsinomieprinzip.
Das Modell kann psychosomatische Zusammenhänge sogar ohne die Existenz komplexer Zusammenhänge zwischen Körper und Psyche erklären, denn danach könnten diese auch auf simplen, hirnorganisatorisch bedingten korrelativen Wechselwirkungen beruhen. Das bedeutet nicht automatisch, dass psychosomatische Phänomene ausschließlich auf diese Weise entstehen, aber vermutlich ein großer Teil von ihnen.
Die Abbildungen 5a und 5b veranschaulichen die dreiteilige Struktur des Gehirns mit ihren jeweiligen räumlich‑funktionellen Überschneidungen zwischen der Steuerung kognitiver, affektiv-emotionaler und körperlicher Funktionen.
ABBILDUNGEN 5 A/B: DAS AFFEKTIVE GEHIRN ALS BRÜCKE ZWISCHEN KÖRPER UND BEWUSSTSEIN
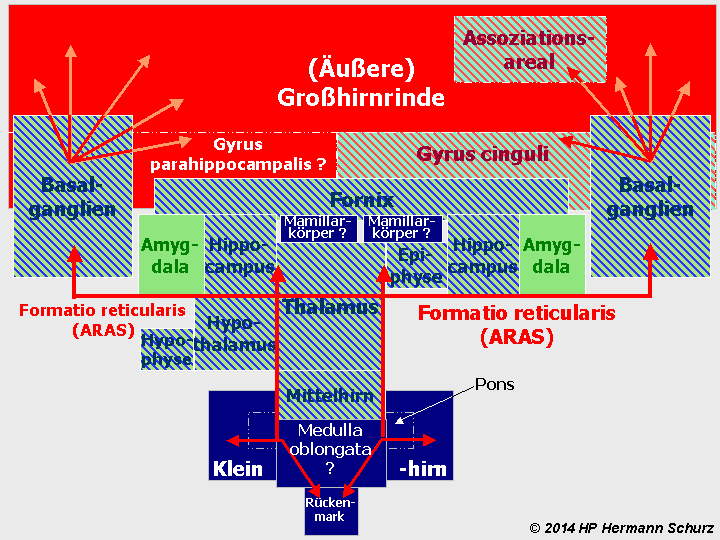
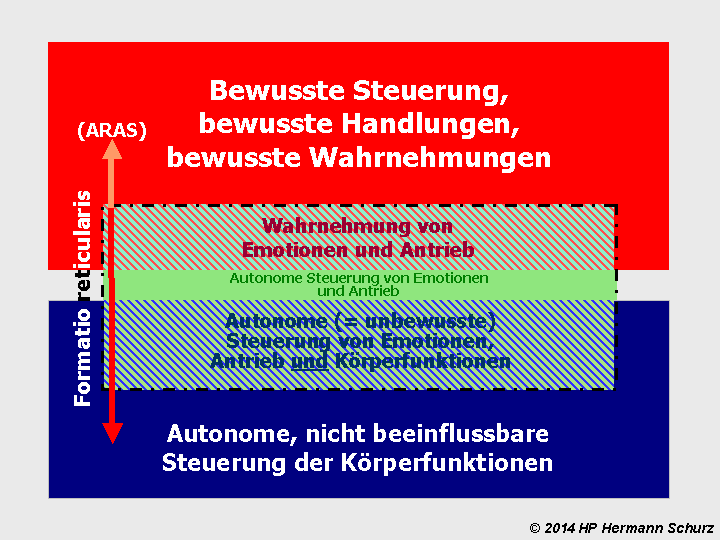
Abbildungen 5a und 5b: Der Affekte/Emotionen verarbeitende dritte Funktionsbereich (schraffiert) befindet sich in der Gehirnmitte, wobei dessen oberen bzw. unteren Areale auch dem jeweiligen angrenzenden oberen (ersten) bzw. unteren (zweiten) Funktionsbereich zugeordnet werden. Abbildung 5b unten verdeutlicht die Zusammenhänge schematisch. Aus funktionellen Überschneidungen ergeben sich Konsequenzen für das Zusammenspiel zwischen Körper und Psyche und begründen psychosomatische Zusammenhänge auf der Ebene des zentralen Nervensystems. Die Formatio reticularis verknüpft alle drei Funktionsbereiche zusätzlich und schafft dadurch eine weitere Verbindung zwischen Körper und Psyche.
Die larvierte Depression kausaltheoretisch betrachtet
Bei der mit körperlichen Beschwerden einhergehenden larvierten Depression (synonym maskierte oder somatisierte Depression) handelt es sich um einen psychosomatischen Spezialfall. Die kausaltheoretischen Modelle helfen hier auf ähnliche Weise wie im vorhergehenden Abschnitt.
Leider werden parallele körperliche Beschwerden bei psychiatrischen Grunderkrankungen häufig einseitig psychologisch gedeutet und dem Patienten unterstellt, er verstecke dahinter seine Unfähigkeit, psychische Probleme zu erkennen. Aufschlussreich in dieser Hinsicht ist ein Text über die larvierte Depression auf einem medizinischen Fachportal aus Österreich: „Bei vielen depressiven Patienten stehen unspezifische somatische Beschwerden im Vordergrund. «Diese Patienten klagen über Rückenschmerzen oder gastrointestinale Symptome, sprechen aber nicht über eine depressive Symptomatik. Aus ihrer Befindlichkeit und ihrem Verhalten ist auch nicht erschließbar, dass letztendlich eine Depression die Ursache dieser Symptome ist», erklärte Müller-Spahn das Konzept der larvierten Depression. (...) Laut einer epidemiologischen Untersuchung an der Psychiatrischen Klinik Basel leiden zwischen 5 und 10% der depressiven Patienten an einer larvierten Depression und etwa 50% der Hausärzte berichten, dass depressive Patienten mit einer solchen Symptomatik in der Praxis vorstellig werden. Gründe dafür sind einerseits, dass Betroffene nicht über Depression sprechen möchten, und andererseits, dass sie die zugrunde liegende Störung nicht erkennen. Das Konzept der larvierten Depression wurde in den 70er Jahren von dem Basler Psychiater Kielholz entwickelt. Dabei wurde auch versucht, ein Ranking der somatischen Symptome zu erstellen, an dessen erster Stelle die Schlafstörungen standen. Schlafstörungen bei Depressionen weisen ein charakteristisches Symptommuster mit frühmorgendlichem Erwachen, Zwangsgrübeln, massiver Hoffnungslosigkeit und erhöhtem Suizidrisiko in den frühen Morgenstunden auf. Dazu kommen Müdigkeit, Abgeschlagenheit, Obstipation und Gewichtsverlust. «Das sind scheinbar ganz unspezifische Symptome, die für sich genommen keine diagnostische Relevanz haben, aber einen Hinweis auf die Depression geben können, wenn keine somatischen Ursachen zu finden sind», erklärte Müller-Spahn. (...) Das Konzept, dass somatische Störungen eine Depression derartig überlagern können, dass die zugrunde liegende Erkrankung nicht mehr erkennbar ist, ist zumindest seit den 1920er Jahren bekannt. So hat bereits Bleuler den Begriff 'somatisierte Depression' geprägt, unter dem er eine endogene Depression verstand, bei der sich Patienten spontan nur mit somatischen Symptomen in der Sprechstunde präsentieren und deren depressiver Gemütszustand erst nach geeigneten Fragen offensichtlich wird. Im anglo-amerikanischen Sprachraum war von der 'physical form of depression', 'hidden depression' oder 'masked depression' die Rede, wobei letzterer Begriff sich zum weltweit am häufigsten verwendeten entwickelte. Weit verbreitet waren auch die Termini 'vegetative Depression' beziehungsweise 'vegetative Dystonie' als Sammelbegriffe für Phänomene erhöhter autonomer Reagibilität, diese jedoch nicht wirklich fassbar machten. Müller-Spahn: «Das Charmante am Konzept der larvierten Depression war, dass es eine klare therapeutische Konsequenz hatte. Hinter dieser vielgestaltigen Phänomenologie verbirgt sich eine Depression, die mit Antidepressiva zu behandeln ist.»“ (Quelle: Die larvierte Depression: wenn sich die Seele hinter dem Körper verbirgt, Webportal der Universimed Cross Media Content GmbH, Wien/Österreich, http://neurologie‑psychiatrie.universimed.com/...).
Es ist zweifellos wichtig, Schilderungen körperlicher Beschwerden bei einer parallel verlaufenden Affektstörung zu hinterfragen. Es ist aber fragwürdig zu glauben, einem Patienten mit einer larvierten Depression müsse lediglich ein antidepressiv wirkendes Medikament verabreicht werden, um die Probleme zu lösen. Es sollte auch nicht einseitig eine Depression als Ursache körperlicher Beschwerden gedeutet werden oder das Bündel körperlicher Symptome vulgärpsychologisch missdeutet werden als sei es Ausdruck dessen, dass „sich die Seele hinter dem Körper verbirgt“.
Kausal ist auf hirnorganischer Ebene eher von einer Korrelation zwischen depressiver und körperlicher Symptomatik auszugehen, bei denen beide Formen real existieren und primär aus Fehlfunktionen von Hirnarealen resultieren, die für körperliche als auch psychiatrische Beschwerden verantwortlich sind (→ Abbildung 5).
Eine vergleichbare Sicht der larvierten Depression scheint sich durchzusetzen, interessant ist hier ein Eintrag des Webportals doccheck.com zur Pathophysiologie: „In neurobiologischen Untersuchungen konnte der Nachweis erbracht werden, dass somatische Symptome mit Hirnfunktionsstörungen korrelieren, die auch für die Depression verantwortlich sind. So konnte in Untersuchungen gezeigt werden, dass psychischer und emotionaler Schmerz zu einer Aktivierung der gleichen Regionen wie physische Schmerzreize führen. Untersuchungen der Stressachse dokumentieren sowohl bei der Depression, als auch bei Schmerzen eine neuroendokrine Dysregulation der Hypothalamus-Hypophysen-Nebennieren-Achse mit Überproduktion des Corticotropin-freisetzenden Hormons CRH, was die Parallelität funktioneller Veränderungen physiologischer Parameter in der Depression und bei Schmerzzuständen belegt.“ (Quelle: Pathophysiologie der larvierten Depression, Webportal der DocCheck Medical Services GmbH, Köln, http://flexikon.doccheck.com/...).
Symptomarten und Symptomanzahl kausaltheoretisch betrachtet
Eine endogene Depression ist eine heterogene Erkrankung mit individuellen Merkmalen, die sich von Patient zu Patient unterscheiden können (→ Abschnitt 1.1):
- Verschiedene Symptome der Bereiche Denken, Emotionalität/Fühlen, Verhalten und Körper sind individuell zuordenbar.
- Die individuelle Symptomanzahl ergibt sich automatisch aus der Aufzählung der Symptome.
Symptomarten und Symptomanzahl lassen sich mit dem Begriff der Symptomvielfalt gemeinsam beschreiben.
Die Gründe dieser Symptomvielfalt ist nach den hier getroffenen Annahmen relativ einfach durch die Art (und Anzahl) betroffener affektrelevanter Hirnareale oder Teilen von ihnen nachzuvollziehen (→ Graphik 1).
GRAPHIK 1: BEGRÜNDUNG DER SYMPTOMVIELFALT EINER AFFEKTIVEN ERKRANKUNG
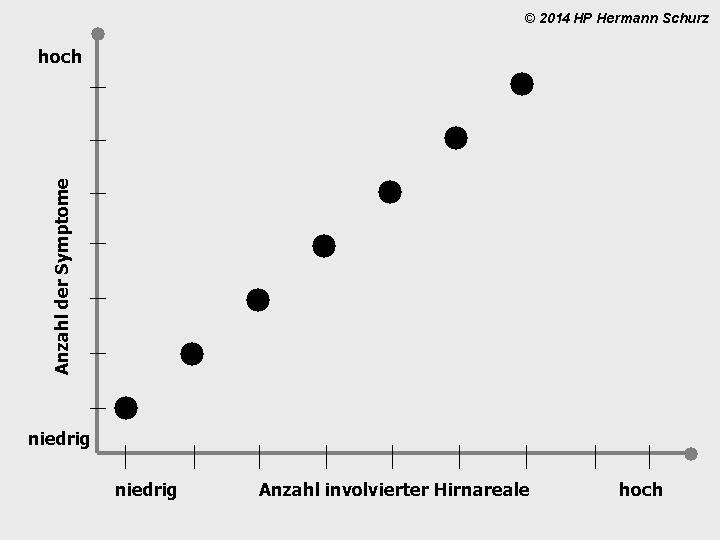
Graphik 1: Mit der Anzahl involvierter Hirnareale steigt tendenziell auch die Anzahl der wahrgenommenen Symptome. Ein Symptom entsteht, wenn die betroffene Hirnstruktur nicht mehr zur Regulation der betreffenden Funktion in der Lage ist.
Erkrankungsintensität kausaltheoretisch betrachtet
Die Schweregrade einer Affektstörung (leicht, mittelgradig, schwer und schwerst) beschreiben im hier diskutierten Zusammenhang Fähigkeiten zur Gestaltung des Tagesablaufs während einer akuten Erkrankungsphase (→ Abschnitt 1.1). Von außen betrachtet lassen sich diese Fähigkeiten anhand objektiver Anhaltspunkte auf den ersten Blick gut einschätzen.
Der subjektiv empfundene Leidensdruck kann von der sichtbaren Situation jedoch abweichen und erheblich höher sein, als dies rein äußerlich den Anschein hat, aber auch der umgekehrte Fall ist möglich. Zur besseren Einschätzung ist eine persönliche Befragung Betroffener daher anzuraten. Auf jeden Fall ist eine differenzierte Betrachtung beider miteinander korrelierender Merkmale gerechtfertigt.
Es liegt nahe ‑ unter Berücksichtigung dieser Einschränkungen ‑ einen Zusammenhang zwischen Erkrankungsintensität bzw. Leidensdruck auf der einen Seite und der Art und Weise von Veränderung des Zentralnervensystems auf der anderen Seite herzustellen. Dysfunktionale Hirnstrukturen des Funktionsbereichs 3 (Affektsteuerung) und die Merkmale Erkrankungsintensität bzw. Leidensdruck stehen in einem Zusammenhang, der einen kausalen Charakter hat:
- Je dysfunktionaler ein Affekte steuerndes Hirnareal (nach dem Drei-Stufen-Basismodell) ist, desto stärker beeinflusst es die Merkmale Erkrankungsintensität und Leidensdruck positiv. Das bedeutet: Je weiter die degenerative Entwicklung fortschreitet, desto größer sind tendenziell Erkrankungsintensität und Leidensdruck.
- Erkrankungsintensität und Leidensdruck steigen ebenfalls tendenziell mit der Anzahl involvierter Hirnareale und damit auch mit der Symptomanzahl.
Erkrankungsintensität und Leidensdruck werden zusätzlich von der Persönlichkeit Betroffener beeinflusst. Beide Merkmale sind zwischen zwei Personen nicht direkt vergleichbar, auch nicht anhand theoretisch (aber praktisch unmöglich) zu messender Daten.
Zusätzlich zur nervlichen Situation des Funktionsbereichs 3 spielt demnach der Gehirnfunktionsbereich 1 eine weitere Rolle, der Bewusstsein, Handeln und Persönlichkeit bestimmt. Das leitet über zum Phänomen der Resilienz.
Resilienz vs. Vulnerabilität ‑ kausaltheoretisch betrachtet
Der Begriff der Resilienz erfreut sich schon länger großer Beliebtheit. Resilienz bedeutet Widerstandsfähigkeit. In der Psychologie wird Resilienz als die Fähigkeit bezeichnet, eine persönliche Krise bewältigen zu können, ja eventuell sogar gestärkt aus ihr herauszukommen. Das Gegenteil von Resilienz ist die mit dem Fachbegriff der Vulnerabilität umschriebene Verletzlichkeit. Auf den ersten Blick scheint es schwierig, derart komplexe Charaktereigenschaften umfassend definieren und begründen zu wollen.
Es gibt den Versuch, die Voraussetzungen für Resilienz anhand von sieben „Säulen der Resilienz“ einzugrenzen, wobei deren Vollständigkeit und Widersprüche hier nicht zur Diskussion stehen. Sie lauten:
- Akzeptieren, was nicht zu ändern ist und Rückschläge positiv nutzen
- Lösungen finden und aus Fehlern lernen
- Gemeinsam mit anderen Menschen Probleme lösen
- Positiv denken, Negatives ausblenden
- Die eigenen Stärken (er)kennen
- Der Glaube, etwas verändern zu können
- Perspektiven entwickeln und Ziele setzen
Die Aussagen sind im Hinblick auf die Bewertung der Resilienz affekterkrankter Menschen hilfreich. Ohne zu verallgemeinern verfügen depressive Menschen nämlich tendenziell eher nicht über diese Merkmale. Affektive Störungen sind vor allem durch Vulnerabilität charakterisiert. Aber es gibt Menschen, die trotz Erkrankung erstaunlich gut funktionieren und resiliente Eigenschaften zu haben scheinen. Wie passt das alles unter einen Hut?
Mit der funktional bewerteten Gehirnlandkarte und dem Drei‑Stufen‑Basismodell (→ Abbildungen 3 ff.) lassen sich sowohl Vulnerabilität und Resilienz als auch Mischformen kausaltheoretisch zumindest mitbegründen. Dabei sind die Hirnfunktionsbereiche 3 und 1 bzw. deren Zusammenspiel von entscheidender Bedeutung:
- Die vulnerable Persönlichkeit ist durch ein Gehirn gekennzeichnet, das im Funktionsbereich 3 (Affektsteuerung) eher dysfunktionale Strukturen aufweist. Mit steigender Dysfunktionalität dieser Hirnareale verschwinden resiliente Eigenschaften kontinuierlich, die Vulnerabilität steigt.
- Die resiliente Persönlichkeit ist durch ein widerstandsfähiges Gehirn gekennzeichnet, das im Funktionsbereich 3 eher keine dysfunktionalen Strukturen aufweist. Vollständige Resilienz würde demnach auch auf einem starken und vollständig funktionsfähigen Funktionsbereich 3 basieren.
- Es ist daher unwahrscheinlich, dass Vulnerabilität und Resilienz in der Realität absolut im binären Sinne vorkommen, eher sind Mischvarianten auf einer Skala zwischen 0 (vollständig vulnerabel) und 1 (vollständig resilient) realistisch, die sich mit individuellen Unterschieden des Hirnfunktionsbereichs 3 erklären lassen und von Person zu Person abweichen.
Eine Beurteilung von Vulnerabilität und Resilienz ausschließlich hinsichtlich der Funktionsfähigkeit der zentralnervösen Affektverarbeitung ist unvollständig, denn gerade der Ursprung kognitiver Eigenschaften, die im Kern die Resilienz oder Vulnerabilität einer Person ausmachen, bliebe dabei unberücksichtigt. Persönlichkeit, Intellekt oder die Problemlösungskompetenz charakterisieren Resilienz ‑ und diese Eigenschaften sind vor allem Leistungen des Hirnfunktionsbereichs 1 (→ Abbildungen 5):
- Eine vulnerable Persönlichkeit weist aus kausaltheoretischer Sicht im Hirnfunktionsbereich 1 tendenziell Defizite auf, die Aufbau und Erhalt resilienter Eigenschaften erschweren. Das Drei‑Stufen‑Basismodell kann hier erste Erklärungsansätze liefern.
- Eine resiliente Persönlichkeit ist durch einen eher gut ausgeprägten Hirnfunktionsbereich 1 gekennzeichnet.
- Auch hier erscheint die Annahme von Mischvarianten zwischen 0 (vollständig vulnerabel) und 1 (vollständig resilient) plausibel, die sich mit individuellen Zuständen des Funktionsbereichs 1 nach dem Drei‑Stufen‑Basismodell erklären lassen und von Person zu Person unterscheiden.
Graphik 2 zeigt, wie das Zusammenspiel der beiden Hirnfunktionsbereiche Resilienzeigenschaften mitbestimmen kann.
GRAPHIK 2: KAUSALTHEORETISCHES RESILIENZ-VULNERABILITÄTS-MODELL
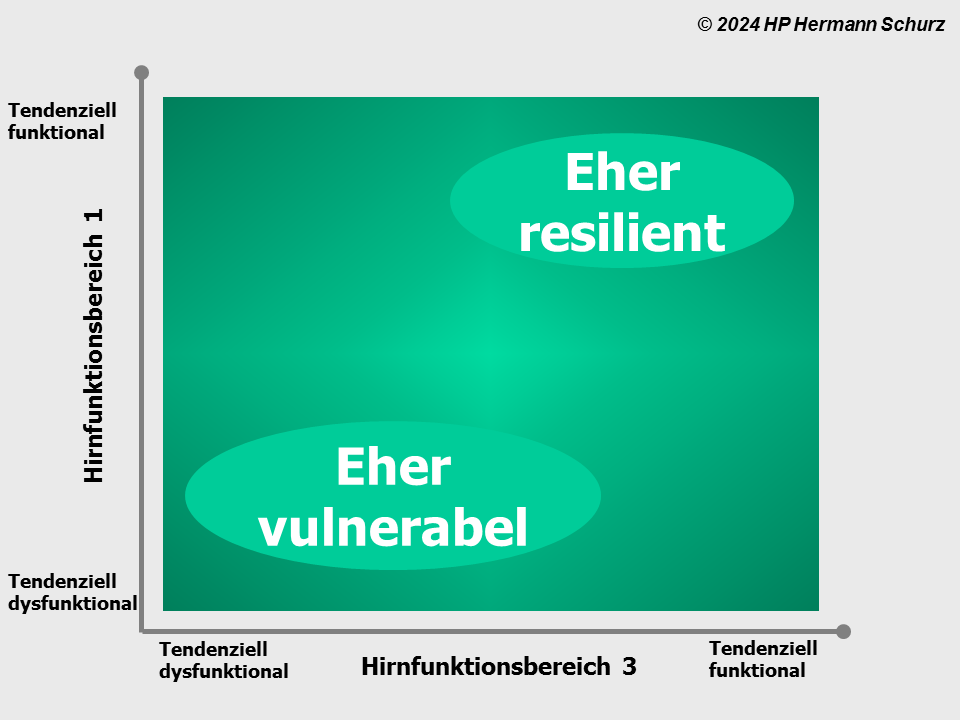
Graphik 2: Das auf den kausaltheoretischen Annahmen basierende Resilienz-Vulnerabilitäts-Modell zeigt auf vereinfachende Form, wie die individuellen Ausprägungen der Merkmale auf der hirnorganisatorischen Ebene mitbestimmt werden. Menschen mit einer ausreichend intakten Affektsteuerung im Funktionsbereich 3 und einer hohen kognitiven Kompetenz durch einen intakten Funktionsbereich 1 gehören tendenziell zu den resilienten Persönlichkeiten. Von ausgeprägteren Formen ist im linken unteren und rechten oberen Quadranten auszugehen. In den anderen Bereichen liegen tendenziell eher Mischformen vor.
Chronifizierung kausaltheoretisch betrachtet
Chronifizierung bezeichnet den Übergang einer vorübergehenden zur dauerhaften Erkrankung bzw. eines sporadisch auftretenden zum ständig präsenten Symptom. Wie bei der Erkrankungsintensität sind bei der Ursachendeutung Drei‑Stufen‑Basismodell und funktional bewertete Gehirnlandkarte hilfreich:
- Aussagen zur Chronifizierung beziehen sich aufgrund vieler unterschiedlicher Symptome des affektiven Formenkreises immer auf einzelne Symptome bzw. Symptombündel, für die jeweils unterschiedliche Hirnregionen verantwortlich sind.
- Je dysfunktionaler ein Affekte steuerndes Hirnareal gemäß Drei‑Stufen‑Basismodell ist, desto stärker die Gefahr einer allgemeinen Tendenz zur Chronifizierung des Symptoms bzw. Symptombündels, welches dieses Hirnareal verantwortet. Vor allem auf der dritten Stufe, also bei schon massivem Verlust von Nerven- bzw. Gliazellen, ist das Gehirn zu Kompensationsleistungen nicht mehr in der Lage mit den entsprechenden Folgen.
Wie schnell oder wie intensiv eine Chronifizierung verläuft, ist vom Einzelfall abhängig, hier spielen viele - auch unbekannte - Einflüsse eine Rolle. Diese Einflüsse könnten Symptomanzahl, Art der Symptome, die Persönlichkeit des Betroffenen (und damit auch seine kognitive Verfassung) oder periphere Einflüsse von außerhalb des Zentralnervensystems sein. Die Frage, ob und wie Symptomanzahl oder die Art der Symptome die Chronifizierungstendenz genau beeinflusst, ist aber auch mit Hilfe der Modelle nicht eindeutig zu beantworten.
Das Phänomen der Chronifizierung lässt sich mit den Modellen nur grob beschreiben und Graphik 3 zeigt genau das. Die verschiedenen Graphen in unterschiedlichen Farben stellen personenbezogene, individuelle Verläufe dar. Sämtlichen Verläufen gemein ist aber die Steigerung der Chronifizierungstendenz bei degenerativem Verlauf.
GRAPHIK 3: CHRONIFIZIERUNG UND DREI-STUFEN-BASISMODELL
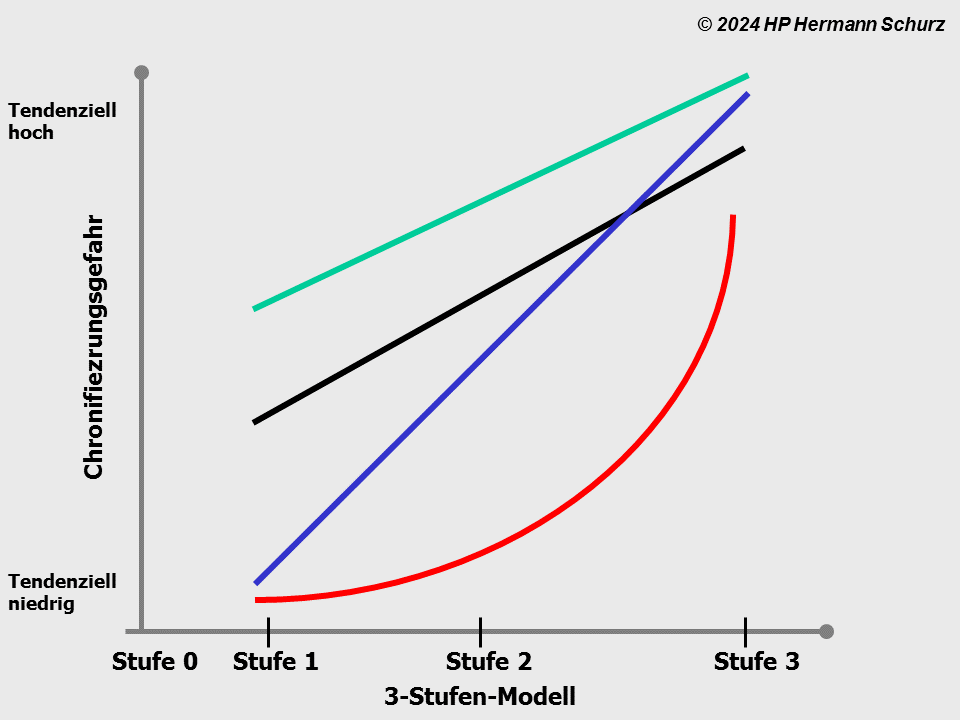
Graphik 3: Die Gefahr der Chronifizierung eines Symptoms (bzw. Symptombündels) aus dem Spektrum affektiver Erkrankungen steigt tendenziell mit dem Grad an Degeneration der verantwortlichen Hirnregion und ist bei Stufe 3 am höchsten. Die Verläufe können von Fall zu Fall abweichen, was die verschiedenen Graphen beispielhaft verdeutlichen und sind wahrscheinlich von zahlreichen Faktoren abhängig, beispielsweise vom individuellen Symptomen-Mix der/des Betroffenen oder dessen allgemeiner gesundheitlichen Verfassung.
Von der depressiven Verstimmung zur Depression: Analyse einer chronischen Entwicklung
Nach diesen allgemeinen Betrachtungen der Chronifizierung soll das Phänomen auf gleicher theoretischer Grundlage nun realitätsnaher an einem potentiellen Erkrankungsverlauf diskutiert werden:
- Die depressive Verstimmung ist keine Erkrankung im eigentlichen Sinne und nicht von vorneherein behandlungsbedürftig, denn es handelt sich um eine völlig normale bzw. erwartbare Reaktion auf negativen Stress, beispielsweise auf den Tod eines nahestehenden Menschen oder ungewollte berufliche und familiäre Veränderungen. Innerhalb einer angemessenen Zeit und insbesondere nach Beseitigung der Stressoren sollten auch depressive Verstimmungen verschwinden.
- Die reaktive Depression kann einer depressiven Verstimmung folgen aber auch unvermittelt auftreten und ist durch wesentlich heftigere Reaktionen auf Negativstress gekennzeichnet und behandlungsbedürftig.
Wenn depressive Verstimmungen an Intensität zunehmen anstatt zu verschwinden und in eine reaktive Depression übergehen, deutet das auf eine möglicherweise beginnende Chronifizierung hin.
- Sowohl depressive Verstimmung als auch reaktive Depression sollten mit der Stressfaktorenbeseitigung überwunden sein, ansonsten wäre das ein starkes Indiz für den vollzogenen Übergang in eine (endogene) Depression chronischen Verlaufs. Aber auch die endogene Depression kann unvermittelt und ohne Vorstufen auftreten.
Die Entwicklung einer Depressionserkrankung kann also gekennzeichnet sein durch eine beginnende depressive Verstimmung, die sich zur reaktiven Depression ausweitet, um schließlich in einer (endogenen) Depression zu enden. Potentielle Mechanismen dieses Prozesses auf der Ebene des Zentralnervensystems werden auch bei diesem praktischen Beispiel mit dem Drei‑Stufen‑Basismodell nachvollziehbar:
- Die Entwicklung einer depressiven Verstimmung zur reaktiven und schließlich endogenen Depression stellt die lineare Entwicklung und Steigerung eines zusammengehörenden Krankheitsbildes dar.
- Eine depressive Verstimmung ist schon auf Stufe 0 möglich ‑ also bei einer strukturell und funktional völlig intakten Affektsteuerung des Hirnfunktionsbereichs 3. Aufgrund der „Nervenstärke“ des depressiv Verstimmten durch die intakte Affektsteuerung wird die Situation jedoch schnell überwunden.
- Je weiter sich die Situation im Gehirn jedoch zur Stufe 3 verschiebt, desto wahrscheinlicher ist ein Übergang von der depressiven Verstimmung zur reaktiven Depression bzw. chronifizierten endogenen Depression.
- Auch hier spielt der Hirnfunktionsbereich 1 (kognitive Fähigkeiten und Persönlichkeit) eine erhebliche Rolle, dessen Funktionalität bzw. Dysfunktionalität ebenfalls die Erkrankungsentwicklung bestimmt.
Weitere Einflüsse, beispielsweise Anzahl der Symptome, Symptomarten oder Allgemeinzustand, sind zu berücksichtigen. Die mit Graphik 3 verdeutlichten Zusammenhänge gelten hier also ebenfalls.
1.6 Nachweise funktionell-struktureller Hirnveränderungen bei Affekterkrankungen mit bildgebenden Verfahren und postmortal ▲
Die im vorhergehenden Abschnitt durchgeführten Prüfungen anhand verschiedener charakteristischer Erkrankungsmerkmale haben Aussagekraft, muten aber eher theoretisch an. So wären nachgewiesene Hirnstrukturveränderungen mittels bildgebender Verfahren jenen theoretischen Prüfungen überlegen, liegen sie schließlich „schwarz auf weiß“ vor.
Die konservative psychiatrische Forschung scheint seit einigen Jahren etwas aus ihrem Dämmerschlaf zu erwachen. Es wurden erste Studien erstellt, die einen Zusammenhang zwischen einer Depression und funktionellen bzw. strukturellen Hirnveränderungen aufspüren sollen. Im Verdacht stehende Hirnareale wurden mit Hilfe von PET‑, fMRT- und MRT‑Technologien untersucht. Es sind vor allem die Strukturen des linken und rechten Hippocampus, des Mandelkerns, der Basalganglien, bestimmter Cortex‑Regionen und des Zwischenhirns, um die sich die Mediziner bemühen und die auch kausaltheoretisch als erkrankungsrelevant gelten.
Grenzen bildgebender Verfahren
Bei der Bewertung der Untersuchungsergebnisse sind die Ungenauigkeiten aller drei bildgebenden Verfahren zu berücksichtigen. Sie sind vergleichbar mit kleinen Teleskopen, die auf den Mond gerichtet werden und nur grobe Strukturen auflösen. Im Gehirn entscheiden aber schon kleinste Veränderungen über Funktionalität bzw. Dysfunktionalität ‑ und die sind mit diesen Methoden nicht erkennbar.
Gerade bei der MRT‑Methode können nur Grobstrukturen abgebildet werden. Ebenfalls liegen häufig keine Langzeituntersuchungen zwecks Vergleichs vor. Bestimmte funktionelle Veränderungen sind mit einer MRT nicht zu erkennen. Weiter ist bekannt, dass abgestorbene Neuronen durch Gliastützzellen ersetzt werden können, die für die Reizverarbeitung aber keine Rolle spielen. Ein solcher Ersatz durch neurologisch funktionslose Gliastützzellen ist beim Alkoholismus bekannt. Derartige Veränderungen sind mit einer MRT aber überhaupt nicht einschätzbar und erst im Rahmen einer Gewebeuntersuchung nach dem Tode feststellbar. Daher kann davon ausgegangen werden, dass viele krankhafte Veränderungen mit der MRT nicht bemerkt und „unter dem Radar“ bleiben.
Die fMRT reagiert lediglich auf Durchblutungsveränderungen und bildet neuronale Aktivitäten nur indirekt ab. Ähnliches gilt für die PET, die ausschließlich den Abbau von Glukose sichtbar macht.
Wird also bedacht, dass viele neurologische Veränderungen mit den Verfahren derzeit gar nicht festzustellen sind, ist es umso bemerkenswerter und aussagekräftiger, wenn Veränderungen mit den grobschlächtigen Verfahren überhaupt nachweisbar sind.
Ergebnisse bildgebender Verfahren
Die Studien von Sheline et al. an depressiven Patienten aus den Jahren 1996 bis 1999 und weitere stellten signifikante Volumenminderungen des linken und rechten Hippocampus fest. Mehrere Studien weisen Atrophien des frontalen und präfrontalen Cortex nach, ebenso Volumenminderungen im Gyrus cinguli.
Untersuchungen der Amygdala lieferten unterschiedliche Resultate. Sie reichen von Volumenzunahme (Weniger et al. 2006 bzw. Frodl et al. 2002) oder Volumenabnahme (Sheline et al. 1998 bzw. Strakowski 2002) bis zu Veränderungen der Symmetrie.
Interessant ist hier die Volumenzunahme. Eine solche ist auf den ersten Blick im Drei‑Stufen‑Basismodell zwar nicht vorgesehen, steht damit aber auch nicht im Widerspruch. Derartige Veränderungen werden im Zusammenhang mit einer Affektstörung zwar selten festgestellt und es könnte sich dabei um ein relativ kurzfristiges Phänomen handeln, bei der sich ein relevantes Hirnareal zunächst aufgrund negativer Einflüsse vergrößert. Vielleicht sind auch Situationen denkbar, bei denen eine Volumenzunahme ähnliche Auswirkungen hat wie eine Volumenabnahme oder die Vergrößerung ist eine Reaktion auf degenerative Vorgänge in anderen, ebenfalls Affekte verarbeitenden Hirnarealen. Solche Differenzierungen müssen im Modell nicht berücksichtigt werden, denn sie ändern nichts Grundsätzliches, denn auch die Volumenzunahme ist eine Abweichung von der Norm.
Eine über drei Jahre angelegte Dissertationsstudie der LMU München (Quelle: Palladino 2009) ergab, dass „(...) sich bezüglich des Amygdala-Volumens zeigte, dass Patienten mit rezidivierenden depressiven Episoden dann symptomfrei blieben, wenn sie ein signifikant größeres Amygdala-Volumen besaßen als Patienten, die sich in einem nicht-remittierten Zustand befanden. (...) Das Alter korrelierte mit einem erniedrigten Volumen der rechten und linken Amygdala.“ Auf jeden Fall konnte „kein signifikant größeres Amygdala-Volumen bei depressiven Patienten verglichen mit gesunden Probanden festgestellt werden.“.
Ebenfalls sind Volumenminderungen der Basalganglien im Zusammenhang mit depressiv Erkrankten nachgewiesen worden (Krishnan et al. 1992).
Eine Untersuchung aus dem Jahr 2004 analysierte 12 Studien, die eine Reduzierung der Hippocampi-Volumina mit unterschiedlichen Intensitäten bestätigten, die sich in ihren Voraussetzungen (Alter, Geschlecht, Krankheitsbeginn und -verlauf) stark unterschieden. Die Metastudie ergab, dass die Hippocampi der von einer unipolaren Depression Betroffenen im Schnitt eine Volumenminderung von 8% auf der linken und 10% auf der rechten Seite aufwiesen. Darüber hinaus ergaben die Auswertungen eine positive Korrelation der Volumenminderungen des rechten Hippocampus mit der Anzahl der depressiven Phasen (Quelle: Videbech/Ravnkilde 2004).
Sogar globale Volumenminderungen des Gehirns sind nachweisbar, wenn auch nicht mit einer großen Signifikanz, wie eine andere an der LMU München durchgeführte Dissertationsstudie herausfand. Für die Gruppe von Patienten mit einer Major Depression „(...) konnte eine leicht erhöhte (...) und in der Varianz verbreiterte globale Atrophierate nachgewiesen werden (...)“. Weiter heißt es: „Es ergaben sich Hinweise, dass bipolare Patienten sowie Patienten mit schweren Verläufen, gemessen an Suizidalität und psychotischem Erleben, möglicherweise erhöhte globale oder temporomesiale Atrophieraten aufweisen. Ob diese Veränderungen im Rahmen schwerer Episoden mit protrahierter Stresshormon-Dysregulation auftreten oder ob vorher oder parallel ablaufende Umbauvorgänge diese Krankheitsverläufe begünstigen, sollte durch prospektive Studien untersucht werden.“ (Quelle: E. Golgor 2009).
Interessant sind die PET- und fMRT-Technologien und deren Nachweise funktioneller Veränderungen im Hirnstoffwechsel, da sie neben der These über die Beteiligung bestimmter Gehirnregionen an der Erkrankung ebenfalls die Aussagen über die ersten beiden Stufen des Drei‑Stufen‑Basismodells stützen.
Studien der Universitätsklinik Wien für Psychiatrie und Psychotherapie, die u. a. mit Hilfe der PET-Technologie durchgeführt wurden, stellten generell Veränderungen im präfrontalen Cortex und im emotionalen System fest (Quelle: CliniCum, Mag. Silvia Hecher 2009, www.clinicum.at):
- Erhöhte Aktivitäten in verschiedenen Bereichen des präfrontalen Cortex,
- verminderte Aktivitäten im dorsolateralen präfrontalen Cortex, wobei der Grad der Hypoaktivität mit dem Grad der Erkrankung korreliert,
- erhöhte Aktivitäten in der Amygdala und
- Dysfunktionen in den Hippocampi.
Bestätigt werden die kausaltheoretischen Aussagen ebenfalls durch die Ergebnisse der Wiener Wissenschaftler bei der Beobachtung des Krankheitsverlaufs. So stellten sie fest, dass die Hippocampi bei anhaltender Erkrankung immer mehr an Größe verlieren. Die Entdeckung steht im Einklang mit der unterstellten zeitlichen Abfolge beim Drei‑Stufen‑Basismodell, denn dort kommt es in letzter Konsequenz auf Stufe 3 zu einem Abbau von Neuronen und Gliazellen, der sich bei andauernder Erkrankung weiter fortsetzt.
Ebenfalls ergaben die Analysen, dass die Wahrscheinlichkeit eines Verschwindens der Symptome (Remission) mit zunehmender Größe der Hippocampi steigt.
Auch degenerative Veränderungen von Gliazellen geraten in der letzten Zeit in Zusammenhang mit der Ursachenforschung erfreulicherweise in den Fokus der Psychiatrie. Untersuchungen an Verstorbenen haben gezeigt, dass die Gliazellendichte bei depressiv Erkrankten wesentlich reduziert ist. In einer anderen Untersuchung wurde ein signifikanter statistischer Zusammenhang zwischen der abnehmenden Dichte von Mikroglia und Fällen von vollzogenen Selbstmorden festgestellt (Quelle: F.A.Z. vom 3.12.2009).
In ihrer Dissertation aus dem Jahre 2002 beschreibt die Psychologin Jennifer Uekermann verschiedene neuropathologische Veränderungen bei einer unipolaren Depression, der hier zum Abschluss noch zitiert werden sollen. Die Autorin bezieht sich auf verschiedene Untersuchungen, die weitere interessante Belege für die vermuteten Kausalzusammenhänge zwischen funktionalen und strukturellen Hirnveränderungen und einer Affektstörung sind: „Um die Frage nach Dysfunktionen umschriebener Hirngebiete bei depressiven Erkrankungen zu untersuchen, wurden in den letzten Jahren Studien mithilfe von EEG- und bildgebenden Verfahren wie der Positronenemissionstomographie durchgeführt (vgl. Uekermann & Daum, 2000). Dabei fanden sich übereinstimmend Funktionsstörungen im Frontalhirn der linken Hemisphäre. Auch Analysen des Spontan-EEGs zeigten bei Depressiven eine verminderte linksfrontale Aktivierung. Für eine Funktionsstörung der linken Hemisphäre spricht ebenso die Tatsache, dass depressive Symptome weit häufiger nach links- als nach rechtshemisphärischer Läsion auftreten (Robinson et al., 1984). In den letzten Jahren ist in verschiedenen morphometrischen Studien ein vermindertes Volumen des frontalen Kortex (Drevets et al., 1997), des Nucleus caudatus (Krishnan et al., 1992), Putamen (Husain et al., 1991), der Hypophyse (Axelson et al., 1992), des Hippocampus (Bremner et al., 2000) und der Amygdala (Sheline et al., 1998) festgestellt worden. In Post-mortem-Studien wurde außerdem ein reduziertes Volumen des orbitofrontalen und dorsolateralen präfrontalen Kortex gefunden (Rajkowska et al., 1999; Ongur et al., 1998; Rajkowska, 2000; Sheline, 2000). Aktivierungsstudien zeigen einen reduzierten Blutfluss und eine verminderte Stoffwechselaktivität im medialen frontalen und im lateralen präfrontalen Kortex, im Zingulum und im Nucleus caudatus (Baxter et al., 1989; Baxter et al., 1985; Dolan et al., 1992; Bench et al., 1992; Cummings et al., 1993a; Devinsky et al., 1995). Dabei geht eine Verbesserung der klinischen Symptomatik mit einer Aktivierungszunahme in einigen betroffenen Regionen einher (Bench et al., 1995), während die Abnormalitäten im orbitalen und medialen präfrontalen Kortex bestehen bleiben (Drevets, 2000). Setzt man die gefundenen Aktivierungsminderungen mit kognitiven Variablen in Beziehung, bestätigt sich der Befund, dass vor allem der präfrontale Kortex eine wichtige Rolle für kognitive Funktionen bei Depressionen spielt (Dolan et al., 1994). Dafür spricht auch die Untersuchung von Bench et al. (1993), die über eine negative Korrelation zwischen der Stärke der Depression und dem regionalen Blutfluss im linken dorsolateralen präfrontalen Kortex und eine positive Korrelation zwischen kognitiven Leistungen und dem Blutfluss im linken frontalen medialen Kortex berichtete. Außerdem führt eine medikamentöse, antidepressive Therapie zu einer Erhöhung des Blutflusses im Frontallappen und Gyrus Cinguli (Buchsbaum et al., 1997). Die Minderaktivierung des medialen präfrontalen Kortex ist bei Depressiven u. a. deshalb von Bedeutung, da diese Region einen Teil des Belohnungssystems darstellt. Über einen verminderten Blutfluss in posterioren Arealen der linken Hemisphäre im Bereich des Gyrus angularis wurde ebenfalls berichtet, doch diese Aktivierungsminderung änderte sich nicht in Abhängigkeit von der Besserung der klinischen Symptomatik (Bench et al., 1995). Von besonderer Bedeutung für die neuropathologischen Veränderungen im Rahmen depressiver Erkrankung ist die Glukokortikoid-Hypothese. Dabei wird angenommen, dass die stressbedingte Ausschüttung von Cortisol zu einer Schädigung hippocampaler Neurone und einer nachfolgenden Hippocampus-Atrophie führen kann (Duman et al., 2000; Fujita et al., 2000; Sapolsky, 1992; vgl. Daum & Suchan, 2001).“ (Quelle: Jennifer Uekermann, Kognitive Veränderungen bei Alkoholismus und Depression, Inaugural-Dissertation, Fakultät für Psychologie der Ruhr-Universität Bochum, Bochum 2002, https://api.deutsche‑digitale‑bibliothek.de/binary/...).
Ergebnisse neuropathologischer Autopsien
Auf die Problematiken hinsichtlich Sensibilität und Genauigkeit bildgebender Verfahren wurde schon hingewiesen. Gehirnautopsien haben zumindest gegenüber dem MRT-Verfahren Vorteile: Hirnstrukturveränderungen können mit histopathologischen Untersuchungen häufig exakter bestimmt werden. Die (nur nach dem Tode durchzuführenden) Untersuchungen sind allerdings ausschließlich forschungsrelevant.
An dieser Stelle soll ‑ um Redundanzen zu vermeiden ‑ auf Kapitel 4 B verwiesen werden, in dem über Beispiele postmortaler Diagnostik berichtet wird. Dabei geht es um die Chronisch‑traumatische Enzephalopathie (CTE), wegen der in den letzten Jahren vermehrt Gehirnautopsien vor allem an verstorbenen Footballspielern in den USA durchgeführt wurden, nachdem diese verhaltensauffällig wurden oder sich das Leben nahmen (→ Abschnitt 4.13.4). Bei einer Erkrankung an CTE stehen häufig massive Veränderungen von Affekten und Persönlichkeit als Symptome im Vordergrund, die wahrscheinlich auf den CTE‑bedingten Veränderungen des Gehirns beruhen und mit häufigen Kopftraumata, vor allem bei den sogenannten Gefahrensportarten, ursächlich in Zusammenhang gebracht werden.
1.7 Erweitertes Drei‑Stufen‑Basismodell ▲
Das dreistufige Basismodell charakterisiert ‑ gemeinsam mit der bewerteten Gehirnlandkarte ‑ die neurologischen Kennzeichen einer affektiven Erkrankung, es erklärt aber nicht deren Ursachen. Um es für die Ursachensuche zu nutzen, muss es erweitert werden.
1.7.1 Zellpathologielehre als Basis
Biologie und Medizin beruhen wesentlich auf grundlegenden Erkenntnissen über Zellen als Einheiten des Lebens, die ab Mitte des 19. Jahrhunderts ‑ zunächst von den Berliner Ärzten Robert Remak und Rudolf Virchow ‑ erarbeitet wurden. Rudolf Virchow erkannte als Erster, dass alle Leistungen des Körpers und seiner Organe auf den Leistungen der Zellen und ihrer Zusammenarbeit beruhen und legte im Jahre 1858 mit der Veröffentlichung seiner „Cellularpathologie“ die Grundlagen der Zellpathologielehre, nach der Krankheiten auf Zellstörungen beruhen. Seitdem hat sich die Zelltheorie rasant entwickelt, aber diese Aussagen sind immer noch aktuell.
Auch das Drei‑Stufen‑Basismodell (→ Abschnitt 1.4) steht mit Virchows Zelltherorie im Einklang: In einem gesunden Nervensystem weisen Nervenzellen eine intakte Reizverarbeitung auf und werden von funktionstüchtigen Gliazellen optimal unterstützt. Es gilt auch die gegensätzliche Aussage, nach der affektive Erkrankungen auf dysfunktionalen Hirnzellen beruhen, zumindest ein Teil der Nerven- oder Gliazellen arbeitet nicht korrekt. Auch eine Erweiterung des Modells hat sich an diesen zelltheoretischen Grundlagen zu orientieren.
1.7.2 Die nächste Kausalebene: Zellprozesse
Beim ursprünglichen Basismodell dreht sich alles um Zellfunktionen. Zellfunktionen sind die nach außen sichtbaren, spürbaren oder messbaren Aktivitäten einer Zelle und der direkte Ausdruck ihrer Aufgabenerfüllung im engeren Sinne. Das Basismodell enthält weder Hinweise darauf, welche Vorgänge die funktionelle Qualität von Zellen aufrechterhalten, noch was für deren Niedergang verantwortlich sein könnte.
Zellfunktionen beruhen auf Prozessen, die im Zellinneren ablaufen. Beispiele für Zellprozesse sind Energieversorgung, Zellteilung oder die Proteinbiosynthese. Um die Ursachen von Funktionsstörungen überhaupt analysieren zu können, ist die Erweiterung des bisherigen Basismodells um Zellprozesse daher unumgänglich. Das erweiterte Modell ermöglicht, die nächste Kausalebene ins Visier zu nehmen: den Zusammenhang zwischen Zellprozessen und Zellfunktionen.
Von der funktionsorientierten zur prozessorientierten Sicht
Wenn intakte Zellprozesse eine notwendige Bedingung („Conditio sine qua non“) für intakte Zellfunktionen sind, ist auch die Negativaussage gültig: Fehlerhafte Zellprozesse in Neuronen und/oder Gliazellen können zu Störungen der Zellfunktionen führen mit der Konsequenz einer fehlerhaften Reizverarbeitung.
Das Basismodell interpretiert als Ergebnis dysfunktionaler Zellprozesse
Das Basismodell wird nun um Zellprozesse erweitert und ein Kausalzusammenhang zwischen Zellprozessen und Zellfunktionen postuliert.
- Stufe 0 (Vorstufe) mit intakter Zellfunktionalität
Aufgrund intakter Zellprozesse ist auch die Zellfunktionalität (Reizentstehung, Reizweiterleitung und Reizübertragung) unauffällig. Die Unterstützung der Nervenzellen durch Gliazellen ist optimal. Nervenzellen sind ausreichend und bedarfsrecht vernetzt. Hirnregionen weisen eine ausreichende Dichte an Nerven- und Gliazellen auf. Das Gehirn ist in der Lage, bei Bedarf auch Nervenzellen zu bilden und für Ersatz zu sorgen (Neurogenese) bzw. bestehende Strukturen umzubauen und anzupassen (Neuroplastizität). Defekte Gliazellen werden bedarfsgerecht ersetzt.
Erste latente Prozessstörungen sind in dieser Phase möglich, haben aber (noch) keine Konsequenzen für die Zellfunktionen.
- Stufe 1: Aus Zellprozessstörungen resultieren Störungen der Zellfunktionen
Prozessstörungen führen zu atypisch verminderten oder atypisch erhöhten Reizverarbeitungaktivitäten.
- Bei atypisch verminderten Reizverarbeitungsaktivitäten auf Stufe 1 werden...
- zu wenig oder keine Reize ausgelöst und/oder
- zu wenig oder keine Reize weitergeleitet bzw. übertragen und/oder
- Reize mit zu geringer Impulsstärke (zu niedrige Aktionspotentialfrequenz) übertragen/weitergeleitet oder
- Reize mit zu geringer Geschwindigkeit weitergeleitet (reduzierte Nervenleitgeschwindigkeit).
Eine atypisch verminderte Reizverarbeitung beruht auf Prozessstörungen, bei denen...
- notwendige funktionsaktivierende Zellprozesse zu langsam ablaufen,
- notwendige funktionsaktivierende Zellprozesse fehlerhaft/unvollständig sind oder komplett ausfallen oder
- notwendige funktionshemmende Zellprozesse übermäßig ausgeführt werden.
Neben Prozessstörungen in den Nervenzellen können auch solche in Gliazellen zu einer sich verschlechternden neuronalen Reizverarbeitung beitragen, denn Nervenzellen werden nicht mehr ausreichend isoliert, gestützt, versorgt bzw. von Schadstoffen entsorgt oder die Modulation der Reizübertragung ist unzureichend. So kommt es bei Multipler Sklerose (MS) zu einer Degeneration myelinbildender Gliazellen mit dem Ergebnis einer immer schlechteren Isolierung der Nervenbahnen und Reduzierung der Reizweiterleitungsgeschwindigkeit. Atypische Aktivitätssteigerungen der Gliazellen als Folge prozessualer Störungen, die in letzter Konsequenz zu verminderter Reizverarbeitung führen, sind ebenfalls möglich. Beim Charcot‑Marie‑Tooth‑Hoffmann‑Syndrom, einer genetisch bedingten neuromuskulären Erkrankung des peripheren Nervensystems, kommt es aufgrund einer übermäßigen Myelinisierung der Schwann'schen Gliazellen zu atypisch verdickten Myelinscheiden. Infolgedessen sinkt ebenfalls die Nervenleitgeschwindigkeit mit der Folge einer Muskelatrophie, da die Signalfolge des Gehirns nicht mehr ausreicht und sich die Muskulatur zurückbildet.
- Bei atypisch erhöhten Reizverarbeitungsaktivitäten der Stufe 1 werden...
- übermäßig viele Reize ausgelöst,
- übermäßig viele Reize weitergeleitet und/oder übertragen,
- Reize mit einer zu hohen Impulsstärke (hohe Aktionspotentialfrequenz) übertragen/weitergeleitet oder
- Reize mit einer zu hohen Nervenleitgeschwindigkeit weitergeleitet.
Eine atypisch erhöhte Reizverarbeitung beruht auf Prozessstörungen, bei denen...
- notwendige funktionshemmende Zellprozesse zu langsam ausgeführt werden,
- notwendige funktionshemmende Zellprozesse fehlerhaft/unvollständig sind oder komplett ausfallen oder
- notwendige funktionsaktivierende Prozesse übermäßig ausgeführt werden.
- Weitere Einflussfaktoren
Prozessfehler können sich im Laufe der Zeit intensivieren und führen zu mehr und weiteren Funktionsfehlern.
Prozessstörungen und eine dadurch atypisch veränderte Reizverarbeitung bergen für Zellen ein zusätzliches Erschöpfungsrisiko, wodurch die Reizverarbeitungsqualität weiter absinkt und das Risiko steigt, wenn Störungen länger anhalten oder besonders intensiv sind.
In neuronalen Netzwerken hat jede Zellaktivität Auswirkungen auf benachbarte Zellen und pathologische Reize werden ‑ vergleichbar mit einem Dominoeffekt ‑ in andere Hirnareale übertragen.
- Stufe 2: Abbau neuronaler Vernetzung
Die nächste Eskalationsstufe funktioneller Einschränkungen aufgrund von Prozessstörungen betrifft den direkten oder indirekten Abbau der Neuronenvernetzung:
- Nervenzellen sind nicht mehr in der Lage, Verbindungen zu anderen Nervenzellen aufrechtzuerhalten und bauen diese kontinuierlich ab.
- Prozessgestörte Gliazellen beschleunigen den Verbindungsabbau, da sie Nervenzellkörper, Nervenleitungen oder Nervenverbindungen durch ihre Dysfunktionalität weiter belasten.
- Nervenzellen kappen von sich aus Verbindungen zu atypisch agierenden Nachbarzellen, von denen sie aufgrund deren Erschöpfung entweder keine oder nur noch wenig Impulse bekommen oder übermäßig unter „Beschuss“ stehen.
- Stufe 3: Abbau von Nervenzellen
Bei weiter anhaltenden oder schwerwiegenden Prozessstörungen kommt es auf der letzten Eskalationsstufe zum Zelltod. Im günstigsten Fall werden abgestorbene Nerven- und Gliazellen als Zellschrott vom Immunsystem abgebaut, im ungünstigsten Fall führt nicht abbaubarer Zellschrott zu weiteren Problemen, beispielsweise Entzündungsreaktionen. Auch hier können prozessgestörte Gliazellen eine wichtige Rolle spielen, die als Bestandteile des Immunsystems für die Zellmüllbeseitigung mitverantwortlich sind und diese Rolle nun nicht mehr ausreichend ausfüllen.
Dringend gesucht: Ein geeignetes Zellprozessmodell
Mit dem erweiterten Basismodell hat eine erste Eingrenzung der Ursachen funktioneller Störungen stattgefunden. Die Gründe der Zellprozessfehler müssen jetzt näher bestimmt und bewertet werden, was ein Zellprozessmodell voraussetzt, mit dem physiologische Zellschwachstellen gezielt aufgedeckt, analysiert und bewertet werden können. Im nachfolgenden Kapitel 2 wird ein solches Modell konstruiert.
Zum nächsten Kapitel 2 (Zellprozessmodell) bitte hier klicken: ►