[ Deutsch ] [ English ] [ Русский ]
Herzlich willkommen!
molekulartherapie.de
Eine universelle Theorie & Therapie der Erkrankungen des zentralen Nervensystems
Zellprozessmodell
2. Ein aggregiertes Zellmodell als Basis einer multikausalen Theorie
2.1 Die vier Zellprozessbereiche ▲
Um überhaupt eine Chance zu haben, die Ursachen der gegen Ende des ersten Kapitels postulierten acht Kategorien von Zellprozessstörungen herauszufinden, wird ein geeignetes Zellmodell benötigt.
Das Modell muss drei Forderungen erfüllen:
- Es muss sich um ein Prozessmodell handeln.
Ursachen von Prozessstörungen können nur prozessorientiert ermittelt werden.
- Es muss sämtliche Prozesse in einer geeigneten Weise aggregiert darstellen.
Nur durch eine sinnvolle Aggregation, das heißt eine systematische Zusammenfassung von Zellprozessen in möglichst wenig Kategorien kann Ordnung in die Darstellung des Chaos zehntausender unterschiedlicher Abläufe gebracht werden. Auf diese Weise wird eine Analyse überhaupt erst ermöglicht.
- Das Zellmodell muss externe Einflüsse ausblenden.
Endogene Prozessstörungen beruhen auf Zellschwachstellen, für deren Analyse die Um- bzw. Außenwelt zunächst keine Bedeutung hat.
Die aggregierte Darstellung folgender vier Zellprozessbereiche erfüllt diese Forderungen und repräsentiert sämtliche endogenen Zellvorgänge:
- Die Kern- und Zellteilung ist der Ursprung jeder Zelle und ein grundlegender Prozess.
- Energiegewinnungsprozesse sind die Voraussetzung aller Zellvorgänge.
- Die Produktion zelleigener Peptide schafft die substantielle Grundlage aller Prozesse.
- Die funktionsbezogenen Prozesse umfassen alle restlichen Prozesse.
Für das Verständnis der nachfolgenden Themen sind keine Vorkenntnisse der Zellphysiologie erforderlich, obwohl sie es zweifelsfrei erleichtern. Die Analyse erfolgt exemplarisch anhand der entscheidenden Prozesse. Es geht um das prinzipielle Verständnis und dazu bedarf es keines Detailwissens, denn es soll hier ja gerade nicht „die Rückseite des Mondes kartographiert“ weden (→ Abschnitt 1.3.1).
Die Darstellung der Proteinbiosynthese erfolgt ausführlicher und wird mit Hilfe von Animationen anschaulicht. Der Proteinbiosyntheseprozess ist für das Verständnis aller nachfolgenden Ausführungen fundamental, er sollte daher in den groben Zügen verstanden werden.
Kern- und Zellteilung (DNA-Replikation, Mitose und Zytokinese)
Kern- und Zellteilung sind bei höheren Lebewesen die Voraussetzungen für Wachstum und Entwicklung: Aus einer Mutterzelle werden zwei identische Tochterzellen, indem alle Zellbestandteile einschließlich des Zellkerns und der darin enthaltenen Erbinformation aufgeteilt werden und dazwischen eine neue Zellmembran entsteht. Die auf diesem Wege weitergegebenen Erbinformationen sind die Grundlage für sämtliche Prozesse und Aktivitäten der beiden neu entstandenen Tochterzellen.
Im Zellkern ist die gesamte Erbinformation auf den Chromosomen gespeichert. Menschliche Zellen verfügen über 46 Chromosomen, bestehend aus 22 Chromosomenpaaren und zwei Chromosomen für die Geschlechtsdetermination. Die Erbinformation repräsentiert die Baupläne aller Zellbestandteile (Gewebeproteine), Reaktionssubstanzen (Enzyme und Proteine) und Informationsträgersubstanzen (nicht-codierende Ribonukleinsäuren).
Die als Mitose bezeichnete Teilung des Zellkerns geht der eigentlichen Zellteilung voran. Zunächst werden die Chromosomen im Zellkern verdoppelt: Die als schraubenförmige Doppelstränge vorliegenden Chromosomen entschrauben und teilen sich, danach bildet sich an jedem Einzelstrang ein komplementärer Strang. Am Ende des Prozesses liegen jeweils zwei identische schraubenförmige Doppelstränge vor.
Da ein Chromosom aus dem Biomolekül der Desoxyribonukleinsäure, kurz DNA, besteht, wird die Verdoppelung der Erbinformation auch DNA‑Reduplikation bzw. kurz DNA‑Replikation genannt. Durch ihn verfügt jede der beiden Tochterzellen später über die für künftige Aktivitäten nötigen identischen Erbinformationen. Die DNA-Verdoppelung wird von zahlreichen Enzymen und Proteinen und speziellen zur Gruppe der nicht-codierenden Ribonukleinsäuren ‑ oder kurz ncRNA ‑ gehörenden Primern gesteuert. DNA ist die international gebräuchliche Abkürzung für den englischen Begriff „Desoxyribonucleic acid“, RNA steht an Stelle des Begriffs „Ribonucleic acid“.
Das genaue Verständnis der Zellteilungsvorgänge im Detail ist hier nicht wichtig. Wichtig ist jedoch das Verständnis, dass sehr viele unterschiedliche Enzyme, Proteine und Primer‑RNA diese Vorgänge steuern. Einige dieser Substanzen(-gruppen) sind beispielhaft genannt und durch Fettdruck hervorgehoben, in der Realität wird eine ungleich höhere Zahl von ihnen benötigt. Im Abschnitt 3.3 finden Sie eine anschauliche Animation der DNA‑Verdoppelung (Animation 12 am Beispiel der Replikation eines Bakterium-Chromosoms).
Nachfolgend eine kurze Beschreibung des dreiteiligen Zellteilungsvorgangs, so wie er beim Menschen stattfindet.
- Initiations- oder Startphase:
Die Aufteilung der beiden DNA-Doppelstränge in zwei Einzelstränge (Leit- und Folgestrang) und eine anschließende Markierung erfolgen durch das Enzym Topiosomerase (entschraubt den Doppelstrang), das Enzym Helikase (trennt die beiden Stränge in einen Leitstrang und einen Folgestrang) und die Primer‑RNA (markiert den Startpunkt).
Leit- und Folgestränge dienen nach der Trennung als Vorlagen für die Synthese der jeweiligen Tochterstränge. Primer-RNA werden mit Hilfe eines Primase-Enzyms synthetisiert und an die beiden Startstellen von Leit- und Folgestrang gebunden. Erst dann beginnen die DNA-Polymerasen alpha mit dem Verdoppelungsvorgang an beiden Strängen.
- Elongations- oder Verlängerungsphase:
Die beiden Tochterstränge werden unterschiedlich verlängert. Die für den Leitstrang zuständige DNA-Polymerase delta unterscheidet sich von der für den Folgestrang zuständigen DNA‑Polymerase delta, die mittlerweile die DNA-Polymerasen alpha ersetzt haben. Auch bei der Verlängerungstechnik gibt es Unterschiede. Während der Leitstrang kontinuierlich in die Richtung der Aufspaltung verdoppelt wird und nur einen Primer als Starter benötigt, wird der Folgestrang fragmentiert in die andere Richtung verdoppelt, was auch als diskontinuierliche Verknüpfung bezeichnet wird und den ganzen Prozess stark verkompliziert. Für jedes Fragment des Tochter-Folgestrangs, auch als Okazaki‑DNA‑Fragment (nach der Entdeckerin Tsuneko Okazaki) bezeichnet, wird deshalb ein bestimmter Primer als Starter benötigt.
Aufgrund der diskontinuierlichen Verknüpfung besteht der Tochter-Folgestrang aus einer Abfolge von Primer-RNA und Okazaki‑DNA‑Fragmenten, wobei jede Primer-RNA quasi eine Lücke darstellt. Daher müssen die Primer-RNA anschließend beseitigt und durch DNA-Bausteine ersetzt werden. Die Entfernung der Primer-RNA geschieht vermutlich mit Hilfe der Polymerase alpha und der RNase H (die Enzyme sind noch nicht mit absoluter Sicherheit identifiziert), das Auffüllen der Lücken mit DNA-Fragmenten erfolgt mit Hilfe einer DNA-Polymerase beta, die Verknüpfung zwischen den Fragmenten erledigt das Enzym DNA-Ligase.
Während der Verlängerung führen die Enzyme Topiosomerase und Helikase ihre Aufgaben weiter fort, denn die DNA wird stückweise verlängert und daher auch nur stückweise entschraubt und getrennt.
- Terminations- oder Schlussphase:
Für die Beendigung die DNA-Replikation spielt das Protein Tus eine Rolle, da es die Aktivitäten der Helikase zum Stillstand bringt.
Darüber hinaus enthält das Chromatin, ein grundlegender Bestandteil von Chromosomen, Histone. Diese Proteine übernehmen wichtige Aufgaben bei der Verpackung und Reparatur der DNA. Darüber hinaus sind sie auch an der Genregulation beteiligt, die in den noch folgenden Abschnitten genauer erklärt wird.
Der die nun verdoppelten Erbinformationen umschließende Zellkern wird nach der DNA-Replikation geteilt, wobei der zweifache Chromosomensatz mit einem aufwändigen Prozess getrennt und je ein Satz zur Seite gezogen wird. Jeder der beiden neuen Zellkerne ist danach – bei im Idealfall fehlerloser Replikation und Mitose – mit einer vollständigen, identischen Erbinformation bestückt.
Im zweiten Schritt erfolgt die eigentliche Zellteilung oder Zytokinese, indem sich neue Außenmembranen (= Zellhüllen) bilden, das Zellplasma mit den Zellorganellen (so werden die winzigen „Zellorgane“ genannt) aufgeteilt wird und zwei Zellen mit jeweils einem Zellkern, einer identischen Erbinformation und einer Organellen-Erstausstattung entstanden sind. Dafür werden ebenfalls Proteine und Enzyme benötigt. Für Transporte innerhalb der beiden entstehenden Tochterzellen stehen MT-basierte Motorproteine wie Kinesin oder Dynein zur Verfügung. Die in der Hauptsache beim Bau von Zellmembranen beteiligten Substanzen sind die Membranproteine.
Die Energiegewinnung (Zellatmung)
Energie ist eine der Grundvoraussetzungen jeder Zellaktivität. Beim Vorgang des Energiestoffwechsels, der auch als Zellatmung, aerobe Atmung oder „innere Atmung“ bezeichnet wird, entsteht Energie durch die vollständige Umwandlung organischer in nicht organische Stoffe.
Dies geschieht durch den Abbau (Oxidation) organischer Kohlenhydrate und Proteine bei gleichzeitigem Verbrauch von Sauerstoff. In den Körperzellen wird Energie auch aus dem Abbau unterschiedlicher Fettsäuren gewonnen.
Im Gehirn nuzten die Nervzellen jedoch ausschließlich Glukose als Energieträger. Eine Ausnahme davon ist die Energienotversorgung des Gehirns bei Kohlenhydratmangel, die hier vernachlässigbar ist.
Der Energiestoffwechsel besteht aus drei Teilen: die anaerobe Glycolyse, der Citratzyklus und die Atmungskette. Die beiden letzten Prozesse finden in bestimmten Zellorganellen statt – den Mitochondrien. Diese produzieren die Zellbrennstoffe Adenosintriphosphat und Guanintriphosphat – kurz ATP bzw. GTP – und als Neben- bzw. Abbauprodukte u. a. Wärme (ca. 60% der Energie), Wasser und Kohlendioxid. Für die Atmungskette ist Sauerstoff notwendig. Mitochondrien sind hochkomplexe Proteine und gehören zur Gruppe der Zellorganellen, die wiederum Gewebeproteine sind.
Mitochondrien sind die einzigen Zellbestandteile, die mit der mitochondrialen DNA über einen eigenen Erbinformationsträger verfügen. Das ist ein sehr kleines Chromosom und nicht zu vergleichen mit den Chromosomen im Zellkern. Auf diesem winzigen Strang befinden sich Informationen über einige Enzyme und Proteine, die für den Energiestoffwechsel wichtig sind. Der größte Teil der für die Durchführung der Energieversorgung nötigen Erbinformation befindet sich aber auf den Zellkernchromosomen.
Kohlenhydrate, Fette und Proteine erhält der Körper über die Nahrung, Sauerstoff in der Form des molekularen Sauerstoffs (O2) durch die Atmung. Für die Steuerung des hochkomplexen Energiegewinnungsprozesses ist eine große Anzahl körpereigener Enzyme und Proteine zuständig, zum Beispiel Citrat-Synthase, Adenylatcyclase, Aconitase, Phosphodiesterase oder Cytochrom c usf.
Die Einzelheiten sind auch hier nicht entscheidend. Das ist auch gut so, denn die Energieversorgung der Zelle ist ein komplexes Thema, das ganze akademische Lehrbücher ausfüllt. Hier geht es einzig um die Tatsache, dass zelleigene Enzyme und Proteine – wie bei der Kern- oder Zellteilung – wesentlich an der Prozessdurchführung beteiligt sind und diese steuern.
Die funktionsbezogenen Prozesse
Jede Zelle erfüllt zusätzlich noch eine Vielzahl individueller Funktionen. Denn Zellteilung und Energiegewinnung sind nur die Voraussetzungen, damit eine Zelle überhaupt entstehen und bestehen kann – sie sind „Pflicht“. Nervenzellen haben darüber hinaus spezielle Aufgaben – die „Kür“: Sie müssen beispielsweise Nervenreize weiterleiten. Gliazellen müssen die Nervenzellen u. a. stützen, voneinander isolieren oder für den An- bzw. Abtransport von Nähr- und Schadstoffen sorgen.
Zur Ausführung aller Funktionen benötigen Nerven- und Gliazellen wiederum viele Substanzen aus eigener Produktion. Zunächst sind das die Gewebeproteine, aus denen die Strukturen ihres inneren und äußeren Aufbaus bestehen – beispielsweise Zellorganellen, die wichtigen Dendriten (= Nervenzellenfortsätze für die Signalaufnahme) oder Axone mit ihren Synapsen.
So wird die Myelinschicht der Schwann'schen Gliazellen und der Oligodendrocyten u. a. mit Hilfe folgender Enzyme synthetisiert: Cholesterolester-Hydrolase, verschiedenen Enzyme für den Auf- und Abbau von Phospholipid, Proteasen, Proteinkinasen, CGT usw.
Neben Enzymen sind auch Proteine bei der Myelinisierung der Axone notwendig, laut einer Studie aus dem Jahr 2009 SCAP (Cleavage-activating protein) und SREBP (Sterol regulatory element-binding protein). Die Proteine Dlg1 und PTEN steuern die Dicke der Myelinschicht der Gliazellen. Sowohl eine zu dünne als auch eine zu dicke Myelinschicht kann zu Erkrankungen führen, da Nervenleitgeschwindigkeit und Isolierungseigenschaften davon negativ beeinflusst werden: Bei Multipler Sklerose liegt eine zu geringe, bei der Charcot-Marie-Tooth-Erkrankung eine zu starke Myelinisierung vor, siehe auch die Erläuterungen im vorhergehenden Abschnitt 1.8.
Noch interessanter sind Enzyme und Proteine zur Steuerung neuronaler Hauptfunktionen:
- Das Enzym Decarboxylase ist für die Bereitstellung monoaminer Neurotransmitter notwendig, beispielsweise Adrenalin, Dopamin, Histamin, Melatonin, Noradrenalin, Octopamin, Serotonin oder Tyramin. Das Gleiche gilt für die Enzyme Tyrosin-Hydroxylase bzw. Tryptophan-Hydroxylase, die an der Synthese von Dopamin bzw. Serotonin beteiligt sind.
- Die zur Gruppe der Neuropeptide gehörenden Botenstoffe sind Proteine. Dazu zählen unter anderem Oxytocin, Somatostatin und GHRH oder verschiedene Opioide.
- Das für die Übertragung von Nervenreizen wichtige Enzym Monoaminoxidase baut monoamine Neurotransmitter nach der Reizübertragung zwischen den Nervenzellen ab. Spezielle Antidepressiva, die Monoaminoxidase-Hemmer oder kurz MAO-Hemmer, greifen in diesen Prozess hemmend ein und erhöhen damit die Anzahl der monoaminen Neurotransmitter im synaptischen Spalt der Nervenzelle.
Da Enzyme und Proteine offensichtlich bei allen Zellprozessen im Mittelpunkt stehen, möchte man nun wissen: Was sind das für Substanzen und wie entstehen sie? Die Frage führt zur Proteinbiosynthese, dem Ursprung aller Peptide.
Die Produktion zelleigener Enzyme und Proteine (Proteinbiosynthese)
Enzyme und Proteine, zu denen auch Neuropeptide und Neurotrophine gehören, bestehen aus verschiedenen Aminosäuren, die in einer bestimmten Reihenfolge miteinander verkettet sind und als Aminosäureverbindungen bezeichnet werden. Im menschlichen Organismus sind nur 20 proteinogene Aminosäuren notwendig, die mit dem Nahrungsprotein aufgenommen werden, welches das Verdauungssystem wiederum in die einzelnen Aminosäuren zerlegt. Einige Aminosäuren kann der Körper selber herstellen.
Alle Aminosäureverbindungen werden kurz als Peptide oder Peptidverbindungen bezeichnet. Nach der Anzahl der Aminosäuren in der Kette ist folgende Peptidklassifikation üblich:
- Verbindungen von nur zwei Aminosäuren nennt man Dipeptide.
- Tripetide nennt man Verbindungen von drei Aminosäuren.
- Verbindungen mit weniger als 10 Aminosäuren werden generell auch Oligopeptide genannt.
- Polypeptide sind Verbindungen von 10 bis 100 Aminosäuren. Enzyme und viele Neuropeptide gehören häufig zu dieser Gruppe.
- Ein Makropeptid mit mehr als 100 Aminosäuren in der Kette wird i. d. R. als Protein bezeichnet. Dazu zählen u. a. Gewebeproteine und einige Neuropeptide.
Der Vorgang der Peptidbildung bzw. der Aminosäureverkettung heißt Proteinbiosynthese oder Proteinsynthese. Richtigerweise müsste es „Peptidbiosynthese“ heißen, aber in der Wissenschaft hat sich dieser Begriff etabliert. Viele verwenden auch den Begriff Genexpression, da die Proteinbiosynthese die auf den Chromosomen gespeicherte Erbinformation (= Gene) in Peptide überträgt. Die Durchführung und Steuerung der Proteinbiosynthese wird interessanterweise wiederum von Enzymen und Proteinen übernommen – also von Peptiden, die selber ein Ergebnis des Prozesses sind.
Daneben wird im Körper noch eine vergleichsweise geringe Anzahl nicht-proteinogener Aminosäuren und biogener Amine synthetisiert, wobei biogene Amine nicht zur Peptid-Gruppe gezählt werden. Verschiedene Neurotransmitter gehören zur letzteren Gruppe und werden Monoamine genannt (→ Abschnitt 1.1 f.). Bei deren Synthese sind ‑ und das ist entscheidend ‑ immer Enzyme beteiligt.
Die Proteinbiosynthese hat aufgrund dessen eine zentrale Bedeutung im Zellmetabolismus. Alle nachfolgenden Ausführungen und Schlussfolgerungen sind eng mit ihr verbunden. Aufgrund dessen erhält sie einen eigenen Abschnitt 2.3 mit ausführlicher Darstellung.
ABBILDUNG 6: DIE VIER GRUNDLEGENDEN ZELLPROZESSBEREICHE
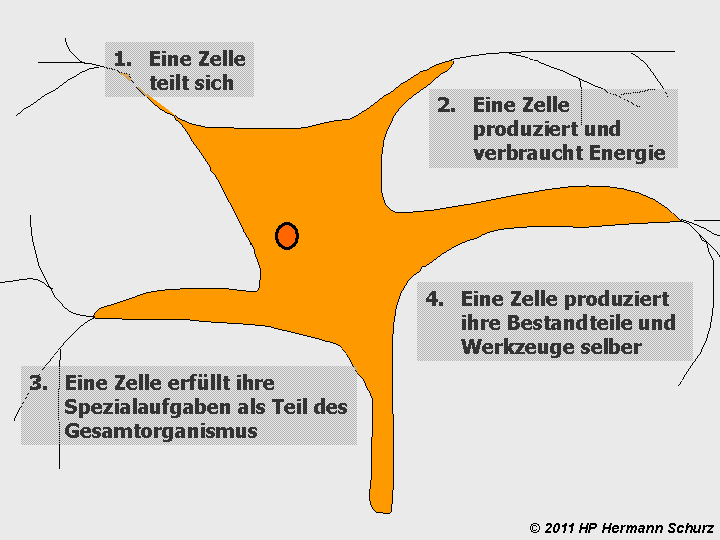
Abbildung 6: Alle Prozesse von Nerven- und Gliazellen lassen sich in vier Bereiche systematisieren. Fast ausschließlich steuern Aminosäureverbindungen – Peptide in Form von Enzymen oder Proteinen – sämtliche Abläufe oder sind als Gewebeproteine beteiligt. Die wenigen Ausnahmen, beispielsweise die auf Cholesterin basierenden Steroidhormone oder biogene Amine, werden mit Hilfe von Aminosäureverbindungen synthetisiert, so dass ebenfalls eine Prozessbeteiligung besteht. Die Proteinbiosynthese bzw. Genexpression (4.) bezeichnet den Herstellungsprozess aller Peptide.
2.2 Die Proteinbiosynthese (Genexpression) ▲
Aminosäuren werden im Verdauungssystem durch die Zerlegung des Nahrungseiweißes aufgenommen. Mit Nahrungsergänzungsmitteln ist die Zufuhr einzelner Aminosäuren möglich. Gesunde Erwachsene produzieren darüber hinaus 12 der 20 Aminosäuren selber. Bei acht Aminosäuren ist der Organismus demnach auf die Zufuhr von außen unbedingt angewiesen; sie werden als essentielle Aminosäuren bezeichnet und sollten in der Nahrung keinesfalls längerfristig fehlen.
Die Proteinbiosynthese verkettet Aminosäuren zu Peptidsorten, die von der Zelle benötigt werden. Jeder spezialisierte Zelltyp hat sein individuelles Peptidprofil. Das ist ein ganz bestimmtes Peptidbündel, welches er für seine Aktivitäten benötigt. Eine Leber- oder Nierenzelle unterscheidet sich von einer Nervenzelle erheblich, daher unterscheiden sich auch deren Peptidprofile. Sogar die Zellen einzelner Organe sind stark differenziert, beispielsweise Nieren- oder Nervenzellen: Es gibt Nierenzellen, welche die Tubuli bilden oder andere, die sich in den Glomerulum-Kapseln befinden. Zellen einer bestimmten Mittelhirnregion haben ein anderes Peptidprofil als Zwischenhirnzellen. In der Mittelhirnregion gibt es wiederum Nervenzellen mit verschiedenen Aufgaben, die sich auch stark voneinander unterscheiden.
Bei der Beschreibung der Zellteilung wurden die Begriffe „Erbinformation“ und „Chromosom“ schon erwähnt: Die Chromosomen im Zellkern enthalten genau die (Erb-)Information über das zu produzierende Peptidprofil und sind ‑ etwas vereinfacht dargestellt ‑ eine gigantische Abfolge nur vier verschiedener Bausteine, den Nukleinbasen. Mit vier Basen codiert jeder DNA‑Strang die Informationen für die Herstellung aller notwendigen Peptide. Die DNA-Basen heißen Adenin, Cytosin, Guanin und Thymin und werden mit ihren Anfangsbuchstaben A, C, G und T abgekürzt. Eine Abfolge von drei Basen – Triplett genannt – enthält die Information für eine Aminosäure: Es ist eine Bauanleitung in Form von Basencodes mit nur vier unterschiedlichen „Buchstaben“ (= Basen) und einer Länge von nur drei Buchstaben.
Ein Peptid wird im Erbgut demnach von mehreren aufeinanderfolgenden Tripletts codiert. Jede Triplett-Abfolge, die ein vollständiges Peptid codiert, wird als Gen bezeichnet. Übertragen auf das obige Sprachbeispiel stellt ein Triplett ein Wort dar und das Gen als die Abfolge mehrerer Tripletts ist mit einem Satz zu vergleichen.
Warum die Erbinformation mit nur vier Nukleinbasen auskommt, ist leicht zu verstehen: Mit einem Triplett können alle 20 verschiedenen Aminosäuren codiert werden. Mathematisch ist eine Abfolge von drei Basen mit vier unterschiedlichen Basenarten sogar in der Lage, 4³ oder 4 x 4 x 4 = 64 Aminosäuren zu verschlüsseln – also wesentlich mehr als benötigt werden. Demnach reichen sogar drei Basen aus, da sie 3 x 3 x 3 = 27 Aminosäuren codieren ‑ ebenfalls mehr als notwendig. Da Tripletts aber auch noch bestimmte Befehle verschlüsseln und einige Aminosäuren von mehreren Basenkombinationen redundant repräsentiert werden, nutzt die Zelle alle 64 Möglichkeiten.
In den Zellkernen aller menschlichen Zellen befinden sich jeweils 46 Chromosomen in der Form von DNA-Doppelsträngen. Da jede Zelle des Körpers damit über die komplette Erbinformation verfügt, muss es den spezialisierten Zellen ‑ und das sind mit der Ausnahme der Stammzellen alle ‑ gelingen, ausschließlich Peptide zu produzieren, die es für ihre Aufgaben benötigen. Das erfordert eine exakte Steuerung der Peptidsynthese und die dazu nötigen Prozesse und Werkzeuge werden in den folgenden Beschreibungen vorgestellt.
Die Herstellung der Peptide erfolgt in zwei Stufen. Hierbei kommt eine weitere, wichtige Gruppe von Substanzen ins Spiel – die Ribonukleinsäuren oder kurz RNA. Deren Aufgaben liegen zunächst in der Übertragung der Erbinformation von den Chromosomen (1. Stufe oder Transkription) und danach in der Übersetzung in die gewünschten Peptide (2. Stufe oder Translation).
Bei der RNA handelt es sich – wie bei der DNA – um eine Nukleinsäure mit vier verschiedenen Basentypen. Drei davon stimmen mit denen der DNA überein (Adenin, Cytosin und Guanin), während anstelle von Thymin die Base Uracil verwendet wird. Weitere Strukturunterschiede bestehen in der Verwendung von Desoxyribose für die DNA bzw. Ribose für die RNA und in der Anzahl der Stränge: RNA bildet einen Einzelstrang, während DNA immer einen Doppelstrang bildet.
Ähnlich wie ein Farbnegativfilm die Farben komplementär abbildet (Rot – Grün, Schwarz – Weiß, Blau/Cyan ‑ Gelb etc.), repräsentiert jede der vier RNA-Basen eine bestimmte DNA-Base.
TABELLE 1: DNA-BASEN UND DAZU KOMPLEMENTÄRE RNA-BASEN
DNA-Basen |
RNA-Basen |
|---|---|
Adenin (A) |
Uracil (U) |
Cytosin (C) |
Guanin (G) |
Guanin (G) |
Cytosin (C) |
Thymin (T) |
Adenin (A) |
Tabelle 1: Es gibt insgesamt fünf Basen. DNA und RNA verwenden davon jeweils vier als Bausteine und unterscheiden sich u. a. in der Verwendung unterschiedlicher Komplementärbasen zu Adenin. Bei Adenin und Guanin handelt es sich um Purinbasen, bei Cytosin, Uracil und Thymin um Pyrimidinbasen.
Funktional unterscheiden sich die beiden Moleküle demnach erheblich: DNA repräsentiert die Erbsubstanz, RNA dient als deren Überträgersubstanz. Später wird gezeigt, dass andere RNA-Moleküle auch noch steuernde Funktionen übernehmen.
Die Proteinbiosynthese besteht im Wesentlichen aus zwei Teilen: der Transkription und der Translation.
Transkription
Vom Gen (= Matrize oder Vorlage, zum Beispiel für ein Peptid) auf einem DNA-Strang wird eine Boten-RNA hergestellt, die ‑ in Anlehnung an das Filmbeispiel ‑ das Negativ ist. Die Boten-RNA wird auf Englisch messenger-RNA (mRNA) genannt.
VIDEO 1: GROBE ERLÄUTERUNG DER TRANSKRIPTION
Video 1: Eine verständliche Erläuterung der Transkriptionsphase, die sich auf die wesentlichen Zusammenhänge beschränkt. Der verwendete Begriff „Botenstoff“ ist nicht zu verwechseln mit den Botenstoffen für die Reizübertragung zwischen den Nervenzellen, die im ersten Kapitel erläutert wurden; hier ist damit die Boten-RNA (mRNA) gemeint. Der Dozent verweist zum Schluss auf die Genregulation, die später noch ausführlich beschrieben wird.
(Quelle: YouTube / biotechnologie.de, Berlin, http://www.biotechnologie.de)
Translation
Die Boten-RNA wandert danach vom Zellkern ins Zytoplasma (das Zellinnere außerhalb des Zellkerns) zu einer bestimmten Sorte von Zellorganellen, den Ribosomen. Dort wird die Boten-RNA in das Peptid übersetzt. Dies ist der zentrale Vorgang der Proteinbiosynthese.
VIDEO 2: GROBE ERLÄUTERUNG DER TRANSLATION
Video 2: Die Darstellung der Translation beschränkt sich ebenfalls auf die wesentlichen Zusammenhänge. Auch hier bitte beachten: Mit dem vom Dozenten verwendeten Fachbegriff „Botenstoff“ ist die Boten-RNA gemeint.
(Quelle: YouTube / biotechnologie.de, Berlin, http://www.biotechnologie.de)
In den nächsten Abschnitten erfahren Sie mehr über Transkription und Translation. Dort wird auch auf die Wichtigkeit der Steuerungsenzyme und -proteine hingewiesen – wie schon oben bei den Beschreibungen von Kern- und Zellteilung, Energiegewinnung und Funktionalprozessen.
Sollte Ihnen die Darstellung bis hierher genügen: Einfach beim Abschnitt 2.2.3 weiterlesen. Es ist für das bessere Verständnis der weiteren Ausführungen jedoch sinnvoll, sich die Zeit zu nehmen und den ausführlichen Beschreibungen zu folgen.
2.2.1 Die Transkription von der DNA auf die Boten-RNA im Detail
Die Transkription verläuft in vier Phasen, deren Bezeichnungen teilweise schon aus den Vorgängen der DNA-Replikation bekannt sind. Es werden – wie bei den vorherigen Beschreibungen – nur einige der wichtigsten Peptide beispielhaft genannt. In der Realität werden dazu weit mehr als hundert unterschiedliche Peptide eingesetzt.
Die Initiationsphase (1)
Da jedes Chromosom als Doppelstrang (Doppel-Helix) mit den Basen in der Mitte vorliegt, muss zunächst die Stelle freigelegt werden, an der sich das Gen für das gewünschte Peptid befindet. Erst dann sind die komplementären RNA-Basen in der Lage, an das Gen zu koppeln und es zu kopieren.
Dabei hat die Zelle einige Schwierigkeiten zu überwinden, denn die Chromosomen enthalten immer das gesamte genetische Profil des Organismus: Jede Zelle verfügt über sämtliche Peptid-Baupläne und damit auch solche, die für die spezialisierte Zelle gar nicht nötig sind oder sogar schädlich wären bzw. von Peptiden, die der Zelle gerade ausreichend zur Verfügung stehen. Ebenfalls muss der richtige Strang abgelesen werden, denn nach der Entfaltung des Doppelstrangs liegen zwei DNA-Stränge frei, von denen nur einer als Matrizenstrang fungiert.
Hier kommen Steuerungspeptide, auch Transkriptionsfaktoren genannt, zum Einsatz, mit denen eine Zelle immer die Position auf der DNA findet, an der mit dem Ablesen des Gencodes begonnen werden muss. Diese Stelle wird Promotor genannt und mittels eines Proteinkomplexes einschließlich einer Helikase und dem Enzym RNA-Polymerase II erfolgt die Auftrennung des DNA-Doppelstrangs genau dort.
Die Zelle hat auch die Möglichkeit, die Auftrennung zu verhindern ‑ beispielsweise wenn sie das Peptid gerade nicht benötigt. Dann sitzt unmittelbar hinter dem Promotor ein Repressor-Protein und blockiert die RNA-Polymerase und die Transkription kommt nicht zustande.
Mit zahlreichen Repressor-Substanzen (z. B. Helix-Loop-Proteine, Zinkfingerproteine, Leucin-Zipper-Proteine) sind Peptide somit direkt an der Steuerung der Transkription beteiligt. Auch die schon bei der Kernteilung erwähnten Histone übernehmen Aufgaben bei der Transkriptionssteuerung. Von der Dichte der Histone hängt nämlich ebenfalls die Transkriptionsrate ab.
Neben einer direkten Beteiligung an der Transkriptionssteuerung können Peptide auch indirekt beteiligt sein: Zum Beispiel ist das genregulatorische Steroidhormon Glucocorticoid selber kein Peptid, wird aber mit Hilfe von Enzymen synthetisiert. Darüber hinaus benötigt es für seine Steuerungsaktivitäten ein Rezeptormolekül. Der Vorgang findet an Regulationsbereichen auf der DNA statt, die als Glucocorticoid-Response-Elemente (GRE) bezeichnet werden.
Diese Prozesse wurden im Video 1 schon erwähnt, sie beschreiben die Genregulation. Die gerade beschriebenen Fälle sind Beispiele für die transkriptionale Genregulation, da sie auf der Ebene der Transkription stattfinden.
Die Elongationsphase (2)
Vom Promotor beginnend legt die RNA-Polymerase II immer bis zu 20 Nukleinbasen frei, an denen sich nun die gegensätzlichen RNA-Basen anlagern und verbindet diese zu einer Basenkette.
Analog zu den Tripletts der DNA, die eine bestimmte Aminosäure codieren, werden drei zusammenhängende Basen der Boten-RNA als Codon bezeichnet.
Die RNA-Polymerase II benötigt für den Kopiervorgang noch zahlreiche andere Peptide, zum Beispiel TBP.
Die Terminationsphase (3)
Ein Terminator auf dem DNA-Strang signalisiert der RNA‑Polymerase II den Stoppbefehl, da das Gen nun vollständig kopiert ist. Die bis hierhin transkribierte RNA‑Codonfolge ist das vollständige, komplementäre Abbild eines Gens und heißt (unreife) Boten-RNA.
Das Erkennen des Terminators erledigt die RNA-Polymerase II mit Hilfe weiterer Proteine bzw. Enzyme. Das Enzym Exonuklease schneidet die Boten-RNA danach ab, der Proteinkomplex TREX ist ebenfalls für die Beendigung der Transkription notwendig.
Rückführung der Initiation (4)
Der gesamte Transkriptionsprozess ist beendet, wenn sich die Polymerase II vom DNA-Strang trennt und dieser wieder zusammen mit seinem komplementären Strang in der Doppel-Helix mit der ursprünglichen Basenpaarung vorliegt.
Die RNA-Polymerase II verbleibt im Plasma des Zellkerns und bewegt sich dort umher, bis sie zufällig oder gesteuert in Kontakt mit der DNA kommt und erneut eine Transkription beginnt.
Es schließen sich unmittelbar nach der bzw. parallel zur Transkription weitere Prozesse an.
Modifizierung (Processing) der unreifen Boten-RNA und Transport in das Zytoplasma
Die Boten-RNA löst sich – zusammen mit der Polymerase II – vom DNA-Strang. Sie ist aber noch nicht einsatzbereit, da sie überflüssige Basensequenzen aufweist und ihr Markierungen für die nächsten Schritte fehlen. Daher wird sie als unreife Boten-RNA oder pre-messenger-RNA bezeichnet und muss noch im Zellkern mit Hilfe weiterer Enzyme bearbeitet werden. Die Bearbeitung erfolgt parallel (co-transkriptional), d. h. das Processing startet noch während des Ablesevorgangs der RNA‑Polymerase.
Das Anbringen der Markierungen an die unreife Boten-RNA ist der erste Schritt. Parallel zur Elongation wird eine Kappe angebracht (Capping) und zum Schluss erfolgt eine Verlängerung mit einer Abfolge zahlreicher Adenin-Basen (Polyadenylierung), die auch als polyA-Kette bezeichnet wird. Parallel zur Elongation werden mittels des Spleißens (Splicing) auch die nicht notwendigen Basenfolgen ‑ Introns genannt ‑ herausgetrennt.
Auch hier sind verschiedene Enzyme bzw. Proteinkomplexe im Einsatz, beispielsweise Cleavage-Faktoren und die PolyA-Polymerase zur Anbringen der polyA-Kette. Das Spleißen wird von Splicosomen durchgeführt, das sind RNA‑Protein‑Komplexe, welche die überflüssigen Basenfolgen aus der unreifen Boten‑RNA entfernen. Das Spleißen wird in Kapitel 3 noch ausführlicher thematisiert.
Die modifizierte Boten‑RNA ‑ auch reife Boten‑RNA genannt ‑ gelangt nun durch die Poren des Zellkerns in das Zytoplasma der Zelle. An dem Vorgang sind Transportproteine beteiligt.
Die folgenden vier Animationen erleichtern das Verständnis der Transkription und des anschließenden Processings zur reifen Boten-RNA.
ANIMATION 1: TRANSKRIPTION OHNE DETAILS
Animation 1: Eine klare, vereinfachend schematische Darstellung der Transkriptions-Akteure ohne Berücksichtigung der Transkriptionsfaktoren oder der Helikasetätigkeit. Zu Beginn sieht man die DNA und ihre gewundene Doppel-Helix-Struktur mit ihren komplementären Basensträngen. Das zu kopierende Gen (entspricht der Coding Region) wird von Promotor und Terminator flankiert. Das blaue RNA-Polymerase-Molekül dockt am Promotor an und teilt die beiden DNA-Stränge. An den nun offenliegenden DNA-Basen lagern sich komplementäre RNA-Basen an. Welcher der beiden Basenstränge für die Transkription genutzt wird ist noch unklar. Die RNA-Polymerase bindet die RNA-Basen aneinander und macht sie zur (unreifen) Boten-RNA. Zum Schluss löst sie sich vom DNA-Strang und er verbindet sich mit dem komplementären DNA-Strang wieder zur Doppel-Helix.
(Quelle: YouTube)
Interessant sind die Mechanismen, mit denen Transkriptionsfaktoren die Promotoren auf den Chromosomen finden, damit die Polymerase in Verbindung mit weiteren Enzymen und Proteinen in Aktion treten kann. Die folgende Animation demonstriert das sehr anschaulich.
ANIMATION 2: TRANSKRIPTIONSFAKTOR AUF DER SUCHE NACH SEINEM PROMOTOR
Animation 2: Es gibt etwa 1.500 unterschiedliche Transkriptionsfaktoren, die in Zellen systematisch und effizient nach zu transkribierenden Genen suchen und nicht nach einem ineffizienten „Try-and-error-Prinzip“. Sie nutzen das Rückgrat der DNA und spulen sich bis zum von ihnen gesuchten Promotor vor. Dabei können sie auch Hindernisse, beispielsweise Repressor-Proteine, überwinden, mit anderen Proteinen interagieren oder von einem DNA-Strang zu einem anderen springen.
(Quelle: YouTube / Stroma Studios, Seattle, WA, USA, http://www.stromastudios.com)
Zum besseren Verständnis noch eine alternative Animation des Transkriptionsprozesses.
ANIMATION 3: DETAILLIERTERE DARSTELLUNG DER TRANSKRIPTION
Animation 3: Bei dieser weniger schematischen (und detaillierten) Animation wird auf die Echtzeit-Darstellung Wert gelegt; sie geht über die Beschreibung im Abschnitt oben hinsichtlich der Zusammensetzung des Proteinkomplexes, der zum Start der Transkription benötigt wird, hinaus. Zunächst ist ein Transkriptionsfaktor am Promotor zu sehen, der die für ihn maßgebliche Bindungsstelle auf dem Chromosom gefunden hat (→ Animation 2). Es erfolgt dann die Integration der RNA-Polymerase II (türkisgrün) mit Hilfe eines zusätzlichen Proteinkomplexes. Weitere Proteine bilden dann gemeinsam den Transkription-Initiations-Komplex. Ein Aktivator-Protein startet die Transkription und die RNA-Polymerase II rast über die DNA, teilt deren Doppel-Helix jeweils für ein kleines Stück und synthetisiert dabei die unreife Boten-RNA. Die RNA-Basen (in Gelb) strömen von links in den Polymerase-Komplex und die Kette des unreifen Boten-RNA-Moleküls schlängelt sich nach draußen.
(Quelle: YouTube / DNA Learning Center, http://www.dnalc.org)
Die Bearbeitung der unreifen Boten-RNA (Processing) durch Anbringen einer Kappe (Capping) bzw. die Polyadenylierung durch das Anbringen einer Adeninkette (polyA-Kette) an ihrem Ende mit Hilfe verschiedener Proteine veranschaulicht die folgende Animation.
ANIMATION 4: CAPPING UND POLYADENYLIERUNG (OHNE SPLEISSEN)
Animation 4: Capping und Polyadenylierung. Das parallel stattfindende Spleißen wird hier nicht gezeigt, was mit Animation 14 in Abschnitt 3.3.3 nachgeholt wird.
(Quelle: YouTube / Virtual Cell Animation, http://vcell.ndsu.edu/public)
2.2.2 Die Translation von der Boten-RNA zum Peptid im Detail
Nachdem die reife Boten-RNA mit Hilfe von Transportproteinen den Zellkern in Richtung Zytoplasma verlassen hat, erfolgt dort die Übersetzung ihres RNA-Basen-Codes in die gewünschte Aminosäurensequenz des Peptids. Dazu werden – neben zahlreichen weiteren Enzymen und Proteinen – zwei weitere Hauptakteure benötigt: Die Transfer-RNA und die Ribosomen.
Jedes Boten-RNA-Codon verschlüsselt eine Aminosäure, und die ganze Abfolge von Codons repräsentiert die zu synthetisierende Kette von Aminosäuren. Die sind jedoch nicht in der Lage, sich direkt an die Codons der Boten-RNA zu heften, da sich beide Substanzen strukturell zu stark unterscheiden. Daher wird eine Trägersubstanz benötigt, die beides kann: erstens eine Aminosäure an sich binden und zweitens das dazugehörige Codon der Boten-RNA erkennen und dort ankoppeln. Das ist die schon erwähnte Transfer-RNA. Sie besteht unter anderem aus drei aufeinanderfolgenden RNA-Basen, die ein Anticodon bilden, sowie einer bestimmten angehängten Aminosäure.
Die Transfer-RNA werden mit Hilfe verschiedener Formen des Enzyms AtRNA-Synthetase mit jeweils einer Aminosäure beladen. Für jede der 20 Aminosäuren gibt es eine andere AtRNA‑Synthetase.
Dreistellige Boten-RNA-Codons und vier Nukleinbasenarten ergeben 64 Kombinationsmöglichkeiten, obwohl aufgrund von nur 20 zu codierenden Aminosäuren und ein paar Start- und Stoppmarkierungen wesentlich weniger Kombinationen notwendig wären (→ Abschnitt 2.3). Viele Basen-Codes sind demnach redundant, so dass alle 64 Möglichkeiten ausgeschöpft werden. In menschlichen Zellen existieren dagegen nur 31 verschiedene Anticodons. Dennoch werden die Peptide während der Translation korrekt gebildet. Einer der Entdecker des genetischen Codes, der britische Forscher Francis Crick, erklärte das mit seiner Wobble-Hypothese, deren Details hier aber nicht weiter vertieft werden müssen.
Die Translation an den Ribosomen unterscheidet drei Phasen mit den schon bekannten Fachbegriffen Initiation, Elongation und Termination. Beim Ribosom handelt es sich um einen Proteinkomplex, der zusammen mit ribosomaler RNA (rRNA) die Paarung der Boten-RNA mit der Transfer-RNA ermöglicht.
Auch hier gilt das Gleiche wie zuvor: Die Prozesse werden nur grob mit beispielhaft ausgewählten Ausführungs‑ und Steuerungspeptiden beschrieben.
Die Initiation der Translation (1)
Im Ribosom findet die Verknüpfung eines Transfer-RNA-Anticodons mit dem ersten Codon der Boten-RNA statt und leitet die Translation ein. Dabei signalisieren Startcodons der Boten-RNA dem ersten Transfer-RNA-Nukleotid die Andockstelle. An der Initiation sind viele weitere Proteine beteiligt, sie werden als Initiationsfaktoren oder kurz eIFs bezeichnet. Derzeit sind bei höheren Organismen 11 eIFs bekannt: eIF1, eIF2, eIF3 usf.
Die Elongation der Peptidkette (2)
Nun wird die Peptidkette verlängert, indem sich weitere Anticondons an die komplementären Boten-RNA-Codons anlagern. Mit Hilfe der Proteine EF-Tu, EF-Ts und EF-G – auch als Elongationsfaktoren bezeichnet – erfolgt die Steuerung der Basenpaarung. Parallel verkettet das Enzym Peptidyltransferase die Aminosäuren. Bei den Vorgängen sind ribosomale RNA (rRNA) beteiligt.
Nach der Aminosäureabgabe zum Zwecke der Verknüpfung haben die Transfer-RNA-Nukleotide ihre Funktion erfüllt. Sie lösen sich vom Codon der Boten-RNA und verlassen unbeladen das Ribosom.
Die Termination der Translation (3)
Wenn das Terminationscodon der Boten-RNA erreicht ist, endet die Translation, und das neu gebildete Peptid löst sich vom Ribosom. Die Boten-RNA trennt sich vom Ribosom oder es erfolgt deren Weitergabe an ein anderes Ribosom zwecks einer weiteren Translation (siehe Animation 7).
Das Erkennen der Stelle zur Beendigung der Translation übernehmen die als Terminationsfaktoren (oder kurz eRFs für Release factors) bezeichneten Proteine. Bei höheren Organismen sind bisher drei verschiedene bekannt: eRF1, eRF2 und eRF3.
ANIMATION 5: TRANSLATION OHNE DETAILS
Animation 5: Eine klare, schematische Darstellung der Translations-Akteure und der Details, die teilweise über die Darstellung im Text hinausgehen. Das Ribosom wird in seiner Funktionsweise genauer dargestellt. Die Basenfolge AUG ist das Startsignal zur Koppelung mit der Untereinheit des Ribosoms. Dann erfolgt der Aufbau der Aminosäurenkette mit Hilfe der Transfer-RNA und den sich daran befindlichen Aminosäurebausteinen. Das Terminationscodon UAG der Boten-RNA beendet die Translation mit Hilfe eines Terminationsfaktors.
(Quelle: YouTube)
Hier eine zweite Darstellung zum besseren Verständnis.
ANIMATION 6: DETAILLIERTERE DARSTELLUNG DER TRANSLATION
Animation 6: Eine weniger schematische Darstellung der Translation, welche die Abläufe in Echtzeit simulieren soll.
(Quelle: YouTube / DNA Learning Center, http://www.dnalc.org)
Abschluss der Proteinsynthese durch das posttranslationale Auffalten (Strukturbildung der Peptide)
Danach erfolgen an vielen Peptidketten noch mehrere Veränderungen (Auffalten, gezielte Verbindung mit anderen Peptiden), so dass eine komplizierte räumliche Struktur entsteht. Aktive Peptide sind keine einfachen Ketten. Sehr kurze Aminosäureverbindungen schaffen die Auffaltung selber, aber die komplexeren benötigten dazu Hilfe. Sonst bestünde die Gefahr, dass sie sich mit anderen Peptidketten ungesteuert verbinden („aggregieren“) und funktionsuntüchtig werden.
Auch hier sind wieder Proteine im Spiel: Chaperone bzw. Chaperonine unterstützen die komplexeren Aminosäurenketten bei der Sekundär- und Tertiärstrukturbildung. Es gibt zahlreiche Chaperon-Chaperonin-Typen, sie werden in fünf Klassen unterschieden. Der gesamte Prozess verbraucht eine Menge Energie in Form von ATP. Animation 7 zeigt diese komplexen Prozesse sehr anschaulich in einer ca. 4-minütigen Animation.
Mit der Auffaltung der Aminosäurenketten zu funktionstüchtigen Peptiden ist die Proteinbiosynthese im engeren Sinne beendet.
ANIMATION 7: AUFFALTUNG DER AMINOSÄURENKETTEN MIT CHAPERONEN UND CHAPERONINEN
Animation 7: Der Film zeigt verschiedene Auffaltungsprozesse unterschiedlich langer Aminosäurenketten zu funktionsfähigen Peptiden mit Hilfe verschiedener Chaperone. Im ersten Teil werden zunächst die Unterschiede der vier Peptid-Grundstrukturen (Primär-, Sekundär-, Tertiär- und Quartärstruktur) anschaulich erklärt. Im zweiten Teil erfolgt eine Darstellung der Abläufe, die für die Sturkturbildung wesentlich sind. Die Translation erfolgt dabei mit zwei Ribosomen, die nacheinander die selbe Boten-RNA auslesen. Tatsächlich durchläuft Boten-RNA häufig mehrere Ribosomen hintereinander mit dem Ziel, die Peptidbildung zu beschleunigen. Findet kein Abtransport an den Ribosomen statt, verwursteln sich zwei Ketten schon kurz nach ihrer Entstehung zu funktionsuntüchtigem „Peptidschrott“. Um diese Verklumpung zu verhindern, werden die fertigen primären Aminosäurenketten sofort nach dem Austritt von Chaperonen in Empfang genommen, um eine korrekte Faltung zu ermöglichen. Diese Chaperone sind auch in der Lage, fehlgefaltete Peptidketten zu reparieren oder ‑ falls eine Reparatur nicht mehr möglich ist ‑ die fehlerhaften Ketten Proteasom-Proteinen zuzuführen, die sie auflösen und in einzelne Aminosäuren recyceln. Sehr lange Aminosäurenketten (bis zu 600 Aminosäuren) können sich jedoch auch auf diese Weise nicht korrekt falten, sie benötigen dazu einen Chaperon-Zylinder, auch Chaperonin genannt. Diese Aminosäurenketten werden von Chaperonen zu Chaperoninen geleitet und in den Zylinder befördert. Dort falten sie sich zu funktionsfähigen Peptiden.
(Quelle: YouTube / Max-Planck-Gesellschaft, © www.mpg.de/2014, http://www.mpg.de)
Zum Schluss noch eine Animation, die die meisten der bis hier beschriebenen Einzelprozesse darstellt.
ANIMATION 8: TRANSKRIPTION, TRANSLATION UND AUFFALTUNG (OHNE PROCESSING)
Animation 8 (derzeit nicht verfügbar, es wird nach Alternativen gesucht): Eine einfache und anschauliche Visualisierung der gesamten Proteinsynthese ohne Processing, die mit der Chaperonin-Auffaltung endet. Zum Schluss verweist der Dozent auf den Umstand, dass Proteine von Proteinen (u. a. Ribosomen) synthetisiert werden, was bei späteren Überlegungen zur Kausalität noch eine wichtige Rolle spielen wird.
(Quelle: YouTube)
2.2.3 Nicht-codierende Ribonukleinsäuren (ncRNA) und ihre Einflüsse auf die Proteinbiosynthese
Nun stehen die Aufgaben nicht-codierender Ribonukleinsäuren (ncRNA) im Mittelpunkt. Diese RNA-Moleküle werden als nicht‑codierend bezeichnet, um sie von den gencodierenden Boten‑RNA (mRNA) zu unterscheiden.
Drei nicht‑codierende RNA sind schon im Zusammenhang mit der Kernteilung und der Translation bekannt: Primer‑RNA steuern die DNA‑Replikation als Starthilfe und spielen somit bei der Verdoppelung der Erbinformationen eine wichtige Rolle. Die verschiedenen Transfer‑RNA und rRNA dienen der Verkettung einzelner Aminosäuren an den Ribosomen in der Translationsphase der Proteinbiosynthese.
Lange Zeit glaubte man, dass sich die Rolle der Ribonukleinsäuren auf die Übermittlerrolle der Boten‑ und Transfer-RNA zwischen dem genetischen DNA‑Code und dem späteren Peptid bzw. einigen Nebenaspekten bei der Translation durch rRNA beschränkt. Erst seit einigen Jahren ist bekannt, dass bis dahin noch unbekannte ncRNA-Moleküle weitere wichtige Funktionen im Rahmen der Regulation bzw. Modulation der Proteinbiosynthese übernehmen. Diese Substanzen sind deshalb auf nicht absehbare Zeit die interessantesten Gegenstände biologischer und medizinischer Forschung. Nur langsam klären sich ihre Funktionen, die heute noch nicht zu überblicken sind. Die Forschung hat hohe Erwartungen bezüglich ihres therapeutischen Potentials.
Bevor die Funktionen der ncRNA näher betrachtet werden, vorab zur Erinnerung nochmal die wichtigsten der schon beschriebenen transkriptionalen Genregulationsvarianten (→ Abschnitt 2.2.1), bei denen Enzyme bzw. Proteine direkt oder indirekt die aktivierende oder unterdrückende Rolle übernehmen.
- Genregulation durch spezifische Transkriptionsfaktoren: Mit Hilfe von Aktivator-Proteinen wird die Transkription bestimmter Gene begonnen, mit Hilfe von Repressor-Proteinen erfolgt das Gegenteil und die Gene werden „ausgeschaltet“. Beispiele für solche Proteingruppen sind Helix-Loop-, Zinkfinger-, Leucin-Zipper, Homöodomänen- oder Helix-Turn-Helix-Transkriptionsfaktoren. Zu deren Aktivierung werden weitere Proteine in Form von Proteinkinasen benötigt.
In noch folgenden Abschnitten (→ Abschnitt 2.3 ff.) werden einige Stoffe aus der Gruppe der Mikronährstoffe beschrieben, die als Co‑Faktoren zusammen mit Enzymen und Proteinen spezifische Transkriptionsfaktoren bilden. Das sind beispielsweise die Vitamin-A-Gruppe, Vitamin D3 und bestimmte Mineralstoffe bzw. Spurenelemente wie Jod.
Es gibt noch weitere Genregulationsvarianten, die diesen jedoch sehr ähnlich sind und auf deren Beschreibung daher verzichtet wird.
- Genregulation durch Histone: Diese speziellen Proteine sind Bestandteile der DNA und steuern unter anderem die Höhe der Transkriptionsrate.
- Genregulation durch Steroidhormone: Glucocorticoide sind in der Lage, mit Hilfe von Rezeptormolekülen und den als Glucocorticoid-Response-Elements (GRE) bezeichneten Basensequenzen auf der DNA im Promotorbereich die Transkription zu regulieren. Steroidhormone werden mit Hilfe von Peptiden synthetisiert.
Peptide sind beim Glucocorticoid-Mechanismus damit sowohl direkt (durch Rezeptormoleküle) als auch indirekt (mittels der durch sie synthetisierten Steroidhormone) beteiligt.
Dass Ribonukleinsäuren ebenfalls an der Genregulation beteiligt sind, ist also eine neue Erkenntnis. Im Gegensatz zur transkriptionalen Genregulation durch Enzyme und Proteine greifen Ribonukleinsäuren überwiegend erst unmittelbar nach der Synthese der Boten-RNA (post-transkriptionale Genregulation) oder sogar während der Translation (translationale Genregulation) in die Proteinsynthese ein.
Im Zentrum stehen zwei gegensätzliche Hauptmechanismen der RNA‑Interferenz, wobei dieser Begriff mit RNA‑Wechselwirkung zu übersetzen ist. Das RNA silencing stellt für die Zelle eine weitere Möglichkeit dar, die Proteinsynthese zu unterbinden. Die RNA‑Aktivierung eröffnet der Zelle die gegenteilige Möglichkeit, nämlich die Proteinsynthese zu forcieren.
Sowohl RNA silencing als auch die RNA-Aktivierung werden durch unterschiedliche Typen von (Unter‑)Mechanismen repräsentiert, wobei die derzeit bekannten keineswegs schon vollständig verstanden werden. Ebenfalls ist auch von weiteren, noch unbekannten Mechanismen auszugehen, die auf allen Ebenen der Proteinbiosynthese denkbar sind: Transkription, Processing, selektiver Transport ins Zytoplasma, Translation oder Inaktivierungen bestimmter Peptide nach ihrer Synthese. Die Schwerpunkte der Steuerung durch RNA sind aber Transkription und Translation und hier ist auch die Forschung am weitesten fortgeschritten.
RNA silencing: Verschiedene Möglichkeiten zur Stilllegung von Genen durch nicht-codierende RNA
Die im Jahre 1998 nachgewiesene Form der Genregulation (Quelle: Driver/Fire/Montgomery/Kostas/Mello, Potent and specific genetic interference by double-stranded RNA in Caenorhabditis elegans, Nature Journal No. 391, 2/1998, http://www.ncbi.nlm.nih.gov/...) betrifft vor allem das zielgerichtete Ausschalten der Aktivitäten von Boten-RNA bzw. Ribosomen durch kurzkettige ncRNA, aber es gibt auch einen Prozess der Transkriptionsverhinderung durch ncRNA, so dass es erst gar nicht zur Synthese von Boten-RNA kommen kann.
Derzeit sind vier verschiedene Interferenzmechanismen des RNA silencing bekannt. Nachfolgend werden die drei wichtigsten vorgestellt, von denen die beiden Letzten für die hier behandelten Themen von Bedeutung sind. Im Jahre 2006 erhielten die beiden amerikanischen Forscher Andrew Fire und Craig Mello für den Nachweis des nachfolgend unter 1. beschriebenen RNA-Interferenz-Mechanismus den Medizinnobelpreis, daher soll er hier ebenfalls kurz skizziert werden.
- Immunologische Funktion durch die Zerstörung fremden RNA-Erbguts
Dieser Prozess ist derzeit nur bei Pflanzen, Pilzen, Fadenwürmern und Insekten nachgewiesen und zielt in seiner natürlichen Alternative auf die Eliminierung eingeschleuster Viren-RNA. Viren sind ein Sonderfall der Evolution, u. a. weil einige von ihnen doppelsträngige RNA (dsRNA) statt DNA als Erbgut verwenden. Deren doppelsträngige RNA dringt in die Wirtszelle ein, wird als fremdes Erbgut erkannt und bekämpft: Bestimmte Enzyme, beispielsweise Dicer oder Drosha, schneiden die fremde RNA zunächst in Fragmente mit einer Länge von ca. 22 Nukleotiden, die man als siRNA oder short interfering RNA bezeichnet. Nun tritt ein zweiter Enzymkomplex, das RIS-Protein (RNA-induced-silencing protein, wird alternativ auch als Argonautenprotein bezeichnet) in Aktion und trennt bei allen Fragmenten die beiden siRNA-Stränge auf. Dabei verbleibt ein Strang der getrennten siRNA im RISC‑Protein, der als Leitstrang bezeichnet wird, während der zweite Strang nicht mehr benötigt und daher abgebaut wird. Nach der Verbindung mit weiteren Proteinen erfolgt das Andocken des RNA-Protein-Komplexes (RNA‑induced‑silencing complex oder kurz RISC) mit Hilfe der Leitstrang-siRNA an eine entsprechend komplementäre Basenfolge einer zellfremden Boten-RNA. RISC spaltet dort die Boten-RNA oder blockiert an dieser Stelle die Übersetzung der genetischen Information in ein Peptid. Die Zelle hat sich damit doppelt gegen den Eindringling abgesichert, indem sie fremdes Erbgut zerstört und mit den fremden RNA-Partikeln aktive unerwünschte Boten-RNA an der Translation gehindert hat. Jedoch ist auch die zelleigene Boten-RNA dem Risiko eines Angriffs der RISCs ausgesetzt. In der Animation 10 unten ist der Vorgang ausführlich dargestellt.
Eine Alternative zu diesem natürlichen Prozess ist die Verwendung synthetischer siRNA. Mit ihrer Hilfe sollen künftig vor allem virale Infektionskrankheiten behandelbar sein. Sehr vielversprechend sind Ansätze in der Krebs- und AIDS-Therapie.
- Regulation der Genexpression durch eine Verhinderung der Transkription
Maßgeblich für die Proteinbiosynthese sind jedoch die verschiedenen Einflüsse nicht-codierender RNA im Zusammenhang mit einer von der Zelle gewünschten Regulation eigener Gene. Denn es gibt Ribonukleinsäuren mit einer siRNA vergleichbaren Struktur, die im Erbgut der Zelle gespeichert sind: die micro-RNA oder kurz miRNA. Es wird vermutet, dass mindestens ein Drittel aller Gene des Menschen durch miRNA gesteuert werden, wahrscheinlich ist die Quote jedoch wesentlich höher.
Bei dem Prozess handelt sich um eine eher seltene Form der transkriptionalen Genregulation mittels micro-RNA. Mit Hilfe einer Variante des RISC-Proteins wird die Transkription vereitelt. Der als RITS‑Komplex (RNA‑induced-transcriptional-silencing complex) bezeichnete Protein-miRNA-Komplex manipuliert die Histone direkt an der DNA, so dass Enzyme keinen Zugang mehr zu diesen Stellen des Erbguts haben.
Bei neueren Untersuchungen von Lena Smirnova wurden miRNA-Bindungsstellen an der DNA gefunden, was auch auf eine unmittelbare Beteiligung der miRNA am Transkriptionsgeschehen schließen lässt (Quelle: Lena Smirnova, Regulation und Funktion der microRNA während der neuronalen Entwicklung und Spezifizierung von Stammzellen, FU Berlin, Berlin 2008, http://www.diss.fu‑berlin.de/...).
- Regulation der Genexpression durch eine Verhinderung oder Störung der Translation
Das RNA silencing betrifft aber vor allem die Verhinderung der Synthese von Proteinen durch Manipulation der reifen Boten‑RNA. Es handelt es sich – je nach Prozessvariante oder Sichtweise – um eine post‑transkriptionale oder translationale Repression durch miRNA.
Der Mechanismus ist noch nicht bis ins Detail durchschaut und die Wissenschaftler gehen auch von mehreren Prozessvarianten aus. So wird vermutet, dass miRNA in Zusammenarbeit mit Enzym- bzw. Proteinkomplexen mindestens drei post-transkriptionale Genregulierungsmöglichkeiten zur Repression der Boten-RNA haben.
Bei der ersten Variante blockieren miRNA die Initialisierungsfaktoren (eIFs) der Translation mit Hilfe von Argonauten-Proteinen durch eine Manipulation der Cap-Strukturen an der Boten-RNA, so dass die ribosomale Untereinheit ihre Aktivitäten nicht beginnen kann (→ Animation 9b unten).
Bei der zweiten Variante erfolgt eine Manipulation der durch die Polyadenylierung entstandenen polyA-Kette am Ende der Boten-RNA durch die miRNA mit Hilfe des RISC-Proteins, so dass ebenfalls keine Translation erfolgt (→ Beschreibungen des Cappings und der Polyadenylierung in den Abschnitten 2.3.1 und die dazugehörige Animation 4).
Die dritte Prozessvariante ist die durch miRNA ausgelöste Boten-RNA-Degradation. Das bedeutet die Zerstörung der Boten-RNA mit Hilfe der miRNA und weiteren Enzymkomplexen. Zunächst wird die polyA‑Kette entfernt, danach die Cap‑Strukturen und erst dann die restliche Boten-RNA aufgelöst. Es handelt sich dabei aber um einen energetisch höchst aufwändigen Prozess (→ Animation 9b unten).
Eine vierte Möglichkeit der translationalen Genregulation nach der Initiationsphase durch miRNA wird noch diskutiert. Man stellte nämlich fest, dass miRNA auch Boten-RNA reprimieren konnte, bei denen die Cap-Strukturen und die Polyadenylierung gar keine Rolle spielen. Es wird nun gemutmaßt, dass die miRNA entweder die Elongation während der Translation verlangsamt oder es zu einer vorzeitigen Termination der Translation – auch „Ribosomal drop‑off“ genannt – kommt (→ Animation 9a unten). In beiden Fällen hat das eine verringerte Syntheserate der betreffenden Peptide zur Folge.
Eine fünfte Möglichkeit besteht im parallelen Abbau der entstehenden Peptidkette durch einen miRNA‑Protein‑Komplex ‑ auch als kotranslationale Degradation bezeichnet ‑ , jedoch wurden die dafür nötigen Proteine noch nicht identifiziert (Quelle: Thermann, BIOspektrum , Nr. 3/2008).
Bei allen bisher beschriebenen Prozessen scheint es so zu sein, dass micro-RNA Enzyme und Proteine benötigen und nicht autonom agieren. Das bedeutet aber nicht, dass es immer so sein muss. Die RNA-Forschung steht noch ganz am Anfang und vieles ist noch völlig unklar.
Die RNA-Aktivierung: Verschiedene Möglichkeiten zur Aktivierung von Genen mittels nicht‑codierender RNA
Bei diesem Genregulationsmechanismus erreicht die Zelle den gegenteiligen Effekt: Die Synthese bestimmter Peptide wird verstärkt. Auch hier sind miRNA in Zusammenarbeit mit Enzym- oder Proteinkomplexen beteiligt. Insgesamt werden mehrere Möglichkeiten diskutiert, die den oben beschriebenen RNA‑silencing‑Prozessen ähneln. Diese könnten u. a. durch eine Aktivierung der Transkription mittels Promotor-spezifischer miRNA und einem RITS‑Komplex oder durch eine Aktivierung der Translation mit Hilfe von miRNA und Argonautenproteinen charakterisiert sein.
Prinzipiell sind die verschiedenen Mechanismen der RNA‑Aktivierung identisch mit denen des RNA silencing – nur eben unter umgekehrtem Vorzeichen.
Zur Spezifität der Wirkungsweise von micro-RNA
Wahrscheinlich werden micro‑RNA sehr unspezifisch zu Modulation der Proteinbiosynthese verwendet. Sie sind also nicht jeweils für die Regulation eines bestimmen Boten‑RNA‑Moleküls zuständig, sondern in der Lage, eine große Anzahl verschiedener Boten‑RNA zu regulieren. Die Basen-Sequenz der micro‑RNA muss also nicht 100%ig mit der Basen-Sequenz der Ziel-RNA übereinstimmen. So könnte ein einziges micro‑RNA‑Molekül hunderte verschiedene Boten‑RNA‑Moleküle beeinflussen (→ Animationen 9a und 10).
Gründe post-transkriptionaler oder translationaler Genregulationen
Seit Entdeckung der neuen Genregulierungsmechanismen wird über deren Gründe gerätselt: Warum führt die Zelle energetisch derart aufwändige Prozesse durch, in dem sie zunächst Boten-RNA katalysiert und sie dann an ihren Aufgaben hindert oder sogar zerstört?
Ein naheliegender, trivialer Grund ist beim RNA silencing die Unterbrechung der Peptidproduktion: Die Boten-RNA ist zwar nicht sehr stabil, würde ohne ein Regulativ dennoch für eine bestimmte Zeit unkontrolliert weiter Enzyme oder Proteine produzieren. Vor der Entdeckung der speziellen ncRNA-Regulationsmechanismen nahmen die meisten Wissenschaftler an, dass RNase‑Enzyme für die Deaktivierung der Boten-RNA verantwortlich sind oder die Boten-RNA aufgrund ihrer Instabilität irgendwann einmal von alleine aufhört, Proteine zu produzieren.
Die Genregulation durch miRNA könnte der Zelle darüber hinaus eine bessere Feinsteuerung erlauben, da die Informationswege zum Zellkern sehr lang sind und so umgangen werden. Das bedeutet: Im Zellkern werden bestimmte Boten‑RNA und ncRNA auf Vorrat oder Verdacht produziert und im Zytoplasma dann bedarfsgerecht gezielt und kurzfristig in Kooperation mit weiteren Proteinen ausgeschaltet.
Die RNA‑Aktivierung ist demgegenüber leichter nachzuvollziehen, denn mit der verstärkten Nutzung schon vorhandener Boten-RNA spart die Zelle weitere Transkriptionen, die höchstwahrscheinlich wesentlich aufwändiger sind. Das Argument einer besseren Feinsteuerung gilt bei der RNA-Aktivierung gleichfalls.
Darüber hinaus könnten die Mechanismen sich auch zufällig als Alternative zu anderen Möglichkeiten der Genregulation entwickelt haben.
2.2.4 Synthese zelleigener nicht-codierender Ribonukleinsäuren
Die Baupläne für miRNA und andere ncRNA-Sorten sind ‑ wie die der Peptide ‑ auf der DNA im Zellkern an unterschiedlichen Stellen gespeichert und werden dort transkribiert. Dabei handelt es sich um jene Basensequenzen, die bis in die 90er Jahre des vergangenen Jahrhunderts noch als rätselhaft galten, weil deren Nutzen sich Niemandem erschloss. Dieser Problematik widmen sich nachfolgende Kapitel noch genauer.
Neueste Forschungen zeigen, dass miRNA ihren Ursprung auch in der Transkription am komplementären DNA-Strang haben könnten. Hierbei handelt es sich um den DNA-Strang, der nicht der Transkription des Gens dient. Nicht-codierende RNA, deren Ursprung auf dem Komplementärstrang der DNA liegt, wird auch als Antisense-RNA (aRNA) bezeichnet.
Da eine Translation nur für die Übersetzung in Aminosäurenketten nötig ist, entfällt diese bei der ncRNA-Synthese. Nach dem derzeitigen Stand des Wissens erledigen fast alle ncRNA ihre Aufgaben im Zusammenhang mit der Herstellung von Enzymen und Proteinen; die einzige Ausnahmen sind Primer‑RNA, die als Starthilfe für die DNA-Replikation fungieren.
Es sind eine Menge verschiedener Enzyme an der Synthese unterschiedlicher ncRNA‑Arten beteiligt. Hauptsächlich verantwortlich sind RNA‑Polymerasen in drei verschiedenen Formen: RNA‑Polymerase I katalysiert die Bildung der ribosomalen RNA (rRNA), die RNA‑Polymerase II katalysiert neben der unreifen Boten‑RNA auch micro‑RNA, RNA‑Polymerase III katalysiert hauptsächlich die Transfer‑RNA, ferner auch micro‑RNA.
Über die Prozesse der miRNA‑Synthese besteht schon etwas mehr Klarheit, erste Arten wurden 1993 entdeckt und damit noch vor der Beschreibung der RNA-Interferenz durch Mello und Fire. Hier einige Fakten zur Synthese, die durch ein aufwändiges Processing gekennzeichnet ist:
- Die Vorstufe der miRNA, die „primäre micro‑RNA“ (pri‑miRNA) hat nach der Transkription eine Struktur von ca. 500 bis 3.000 Nukleotiden.
- Das Primärtranskript weist sowohl eine Kappe als auch eine polyA‑Kette am Ende auf.
- Zunächst faltet sich das RNA-Molekül zu einer Schleife mit einem langen Ende (Haarnadelstruktur oder „hairpin loop“). Durch die Haarnadelstruktur ist eine gewundene, doppelsträngige miRNA (ds‑miRNA) entstanden. Anschließend transportiert ein spezielles Proteins, beispielsweise Exportin 5, die ds‑miRNA vom Zellkern in das Zytoplasma, falls sie dort für die Genregulation vorgesehen ist.
- Jetzt wird die ds‑miRNA entwunden und mittels eines Dicer‑Enzyms in kurzkettige, ca. 20 Nukleotide umfassende doppelsträngige ds‑miRNA geschnitten. Anschließend wird die gekürzte doppelsträngige ds‑miRNA von einem Argonautenprotein übernommen und in eine einzelsträngige miRNA transformiert.
- Nachdem der Syntheseprozess abgeschlossen ist, übernimmt der im Argonautenprotein verbliebene genregulierende miRNA‑Strang mit Hilfe weiterer Proteine, die gemeinsam den RNA‑induced‑silencing complex (RISC) bilden, ihre regulatorischen Aufgaben an der Boten‑RNA.
Animationen von micro-RNA-Synthese und translationaler Gen-Regulation durch RNA-silencing
Zum besseren Verständnis zunächst zwei Animationen, die sowohl den Synthese- als auch verschiedene Genregulationsprozesse veranschaulichen. In Animation 9a wird die als Ribosomal drop-off bezeichnete translationale Genregulation durch vorzeitige Beendigung der Aminosäurenkettenbildung veranschaulicht (→ Beschreibung der vierten translationalen Prozessvariante oben). In der detaillierten Animation 9b werden zwei weitere translationale RNA‑silencing‑Mechanismen gezeigt: 1. Zerstörung der Boten‑RNA, auch Boten‑RN‑Degradation bzw. in der Animation Cut of messengerRNA genannt (→ entspricht ungefähr der dritten translationalen Prozessvariante oben), und 2. eine Blockade der ribosomalen Untereinheit (→ Beschreibung der ersten translationalen Prozessvariante oben).
ANIMATIONEN 9 A/B: MICRO-RNA-SYNTHESE UND GENREGULATION DURCH RNA-SILENCING
Animation 9a (ohne Audio-Kommentar): Synthese eines (aus Gründen der einfacheren Darstellung verkürzten) Primärtranskripts pri-micro-RNA durch eine RNA-Polymerase an der DNA (DNA to RNA) im Zellkern, Auffaltung zur Haarnadelstruktur, Transport ins Zytoplasma, Processing der gewundenen, doppelsträngigen pri-micro-RNA zur einsträngigen micro-RNA, Verbindung mit einem Proteinkomplex (gelb) und Genregulation durch die Unterbrechung der Translation mittels des entstandenen micro-RNA-Protein-Komplexes (Ribosomal drop-off). Auf die Darstellung der vielen beteiligten Hilfsenzyme wurde verzichtet. Die komplementären Basensequenzen der in der Animation dargestellten micro-RNA stimmen nicht genau mit den Sequenzen der Boten-RNA (mRNA) überein, was man an den vier nicht zusammenpassenden Basen in der Mitte erkennt; dennoch nimmt die micro-RNA ihre modulierende Aufgabe wahr, eine 100%ige Übereinstimmung der Basensequenz zwischen Boten-RNA und micro-RNA scheint nicht erforderlich. Offensichtlich sorgt das mit der micro-RNA verbundene Protein genau an der nicht übereinstimmenden Stelle für die Ausschaltung der nicht passenden Basensequenz. Die Zusammenarbeit mit verschiedenen Proteinkomplexen erlaubt es einer einzelnen Sorte micro-RNA, die Synthese mehrerer Typen von Boten-RNA zu steuern, indem immer gerade die Basen vom Protein „angehoben“ werden, die einer Paarung im Wege stehen (siehe dazu auch Animation 10 und den Hinweis zur Spezifität von micro-RNA).
(Quelle: YouTube / Rosetta Genomics, http://www.rosettagenomics.com)
Animation 9b (mit Audio-Kommentar auf Englisch): Diese Animation zeigt die Funktionen der Genregulation am Beispiel verschiedener RNA-Silencing-Prozesse (Gene silencing) und unterschiedlicher Haut-, Muskel- und Knochenzellen (Skin/Muscle/Bone cells). Trotz ihrer Verschiedenheit verfügen alle drei Zellarten über einen identischen Gencode im Zellkern (Nucleus), so dass es zwingend einen Zelldifferenzierungsmechanismus geben muss. Dieser Mechanismus ist die Genregulation, die hauptsächlich mit Hilfe kleiner RNA-Moleküle, zum Bespiel micro-RNA, gesteuert wird. Ein Untermechanismus davon ist das RNA-silencing, durch das nur diejenigen Gene in der exakten Häufigkeit translatiert werden, die für den betreffenden Zelltypen notwendig sind. Fehlende oder fehlerhafte micro-RNA haben Genregulationsstörungen und damit Zellfunktionsstörungen als Folge; im Beispiel werden Krebs- und Herz-Kreislauf-Erkrankungen (Cancer/Heart diseases) genannt. Natürlich betrifft das auch neurologisch-psychiatrische Erkrankungen, denn die Nerven- und Gliazellen des Zentralnervensystems sind ebenso auf eine exakte zelltypspezifische Genregulation angewiesen. Ein Blick in den Zellkern zeigt die schon beschriebene mehrstufige micro-RNA-Synthese durch Transkription und den nachfolgenden Transport durch die Zellkernporen in das Zytoplasma außerhalb des Kerns. Dort erfolgt eine Bearbeitung mit Hilfe mehrerer Proteinkomplexe (Dicer, Argonautenprotein AGO 2 und RISC-Komplex), so dass der micro-RNA-Proteinkomplex seine genregulierende Funktion übernehmen kann. Die Animation zeigt mit der Boten-RNA-Degradation und der rRNA-Blockade zwei Beispiele translationaler RNA-silencing-Prozesse.
(Quelle: YouTube / Katharina Petsche)
Alternativ eine ausführliche Darstellung der Proteinbiosynthese und verschiedener regulatorischer Prozesse mittels eines Vergleichs zwischen siRNA und miRNA mit deutscher Kommentierung.
ANIMATION 10: RNA-SILENCING MIT SHORT INTERFERRING RNA UND MICRO-RNA
Animation 10 (mit Audio-Kommentar in Deutsch): Darstellung der Genregulation bzw. des RNA silencing mittels siRNA und miRNA. Leider werden die Unterschiede zwischen siRNA und miRNA nicht klar beschrieben. siRNA gelangen immer von außen in die Zelle (durch Viren oder experimentell). miRNA werden von der Zelle selber zu Modulationszwecken katalysiert. Strukturell unterscheiden sich die beiden Sorten nicht oder nicht wesentlich.
(Quelle: YouTube / Spektrum der Wissenschaft, http://www.spektrum.de)
2.2.5 Neue ncRNA-Sorte entdeckt: Zirkuläre Ribonukleinsäuren (circular-RNA bzw. circRNA)
Anfang 2013 ist laut Veröffentlichungen im Nature Journal eine weitere Art nicht-codierender, relativ kurzkettiger ncRNA entdeckt worden, die aus ringförmigen RNA-Molekülen besteht und Bindungsmöglichkeiten für andere kurzkettige ncRNA aufweist (Quellen: Nature Journal bzw. Nature Reviews Genetics, doi:10.1038/nature11928, doi:10.1038/nature11993 und doi:10.1038/nrg3464, Februar + März 2013).
Es deutet einiges darauf hin, dass die Bindungsstellen dieser circular-RNA bzw. circRNA für micro-RNA vorgesehen sind. Die RNA-Ringe müssten dadurch ihrerseits eine Regulierung der micro-RNA betreiben, so dass eine Modulation der Proteinbiosynthese auf einer weiteren dritten Ebene stattfindet (→ Abbildung 7 unten). Damit wird die Genregulation insgesamt noch komplexer und unübersichtlicher.
Wird es aufgrund einer solch chaotischen Gemengelage überhaupt jemals möglich sein, einzelne ncRNA-Moleküle eindeutig mit bestimmten Prozessen oder Erkrankungen in Verbindung zu bringen, um auf diese Weise therapeutische Konzepte zu erarbeiten? Und wenn ja, bei welchen Arten von Erkrankungen (Karzinomen, Infektionserkrankungen, degenerative Erkrankungen) ist überhaupt mit Erfolgen zu rechnen?
Diese Fragen sind noch Gegenstand des vierten Kapitels, in dem pathologische Wirkungen fehlender oder dysfunktionaler kurzkettiger ncRNA-Moleküle erörtert werden und des zweiten Teils dieser Ausführungen, bei dem es um die therapeutische Anwendung dieser Substanzen geht.
ABBILDUNG 7: DREI EBENEN DER GENREGULATION?
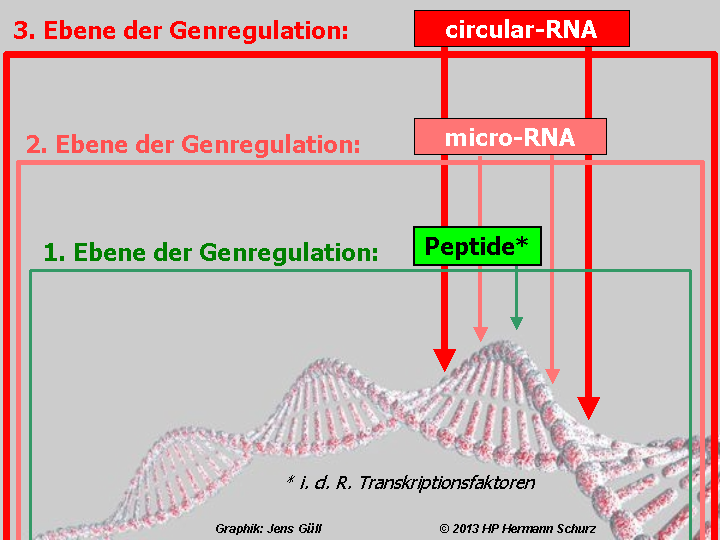
Abbildung 7: Die Proteinbiosynthese wird nach neuesten Erkenntnissen (3/2013) wahrscheinlich von weiteren RNA-Molekülen moduliert, die Bindungsstellen für micro-RNA aufweisen und als zirkuläre RNA oder circular-RNA bzw. circRNA bezeichnet werden, da sie einen ringförmigen Aufbau haben. Dadurch könnte die Genregulation auf drei Ebenen und fünf unterschiedlichen Arten ablaufen. Die schon seit langem bekannten Regulationspeptide (Transkriptionsfaktoren, Repressoren oder Histone bzw. einige andere Peptide, teilweise in Zusammenarbeit mit Hormonen) steuern die Genexpression direkt und autonom von den anderen Substanzen bzw. Ebenen (grüner Pfeil) oder ihre Synthese wird wiederum von micro-RNA reguliert (linker hellroter Pfeil), womit micro-RNA indirekt an den Genregulationsaktivitäten der Peptide beteiligt wären. Die dritte Möglichkeit ist, dass die Synthese der Peptide durch micro-RNA gesteuert wird, die ihrerseits von circular-RNA beeinflusst werden (dunkelroter Pfeil ganz links). Auch micro-RNA regulieren unabhängig von der 3. Ebene entweder direkt (rechter hellroter Pfeil), oder sie werden wiederum von circular-RNA gesteuert (dunkelroter Pfeil ganz rechts); die beiden Alternativen stellen die vierte und fünfte Genregulierungsvariante dar. Die Existenz dreier Modulationsebenen ist realistisch, wenngleich noch nicht endgültig belegt.
2.2.6 Der co- bzw. posttranslationale Proteintransport (Protein targeting)
Mit der Translation und dem anschließenden Auffaltungsprozess ist die Proteinbiosynthese im engeren Sinne beendet.
Einige Peptide verbleiben im Zytoplasma, andere müssen noch zu den Stellen in der Zelle gelangen, an denen sie gebraucht werden. Das gilt für die verschiedenen Zellorganellen oder entferntere Bereiche wie Zellkern oder Nervenzellenfortsätze bei Neuronen. Manche Enzyme oder Proteine erfüllen ihre Funktionen außerhalb der Zellmembran, zum Beispiel das Insulin (→ Animation 11).
Auch die Durchführung des Transports ist natürlich von Enzymen und Proteinen abhängig. Dazu nur zwei Beispiele:
- Der Proteinkomplex SRP (Signal recognition particle) sorgt dafür, dass Peptide zu einer bestimmten Zellstruktur, dem Endoplasmatischen Retikulum, transportiert werden.
- Das Enzym MPP (Mitochondrial processing peptidase) ist beim Peptidtransport zu den Mitochondrien beteiligt.
2.2.7 Weitere co- oder posttranslationale Modifikationen
Parallel zum Transport an den Einsatzort werden viele Proteine und Enzyme durch weitere Prozesse auch in ihrer Struktur verändert, damit sie in Aktion treten können. Diese Vorgänge finden zum Teil kurz nach der Synthese an den Ribosomen, nach der Chaperonin-Auffaltung oder auch außerhalb der Zellen statt. In den meisten Fällen sind jedoch Zellorganellen im Zytoplasma, beispielsweise das Endoplasmatische Retikulum (ER) oder der Golgi-Apparat, Orte für co- oder posttranslationalen Modifikationen. Auch hier steuern Enzyme und Proteine das Geschehen..
Insgesamt hat die Zelle sieben bis neun verschiedene Möglichkeiten, Peptide zu modifizieren. Dementsprechend gibt es auch viele verschiedene Substanzen, die dafür verantwortlich sind. Letzteres ist wichtig, die Einzelheiten sind für unseren Zweck wie immer nicht von Bedeutung.
Hier kann man sich nochmal den gesamten Prozess einschließlich des Peptidtransports und der Peptid-Modifikationen ansehen.
ANIMATION 11: TRANSKRIPTION, PROCESSING, SPLEISSEN, TRANSLATION, MODIFIKATION, TRANSPORT
Animation 11: Die gesamte Proteinbiosynthese und sich anschließende Prozesse bis zum Peptidtransport an den Einsatzort außerhalb der Zellmembran am Beispiel des Insulins. Die Prozesse werden zum Teil nicht in allen Einzelheiten gezeigt; so fehlen zum Beispiel die Aktivitäten von micro-RNA, da die Herstellung des Films schon einige Jahre zurückliegt. Die Transkription der mRNA (Boten‑RNA) erfolgt am freiliegenden Insulin-Gen, das sich zwischen zwei Histonkomplexen befindet. Eine dunkelgelbe Polymerase transkribiert rote mRNA (Boten‑RNA), welche parallel bzw. danach prozessiert wird (Capping, Spleißen und Polyadenylierung). Dann erfolgt der Transport aus dem Zellkern durch eine seiner Poren in das Zytoplasma, wo die Translation stattfindet. Da es sich bei Insulin um ein Peptid handelt, das später sekretiert, d. h. außerhalb der Zelle verbracht wird, erfolgt dessen Ausstoß in das Raue Endoplasmatische Retikulum (RER), nachdem das Ribosom dort an einer Öffnung angedockt hat. Das Insulin faltet sich hier von alleine, denn nicht alle Peptide sind auf Chaperone angewiesen. Das Innere des RER ist der Ort, an dem viele Peptide strukturverändert oder modifiziert werden. Insulinmoleküle werden nach dem Auffalten sofort in Vesikel „verpackt“ und zum Golgi-Apparat transportiert. Der Golgi-Apparat ist ein weiterer Ort der Proteinmodifikation bzw. dort wird eine Modifikation vorbereitet, die anschließend in Vesikeln während des Weitertransports vonstatten geht. Insulin gehört zur letzteren Sorte, d. h. seine Modifikation erfolgt während des Vesikel-Transports in Richtung Zellmembran. Zum Schluss werden die Insulinmoleküle durch die Zellwand nach außen befördert.
(Quelle: YouTube / Pearson Education Inc., http://www.pearson.com)
2.3 Mikronährstoffe und Aminosäuren für die Zellprozesse ▲
Bisher sind die Mikronährstoffe und ihre Aufgaben aus Gründen der besseren Übersicht und Verständlichkeit noch nicht beschrieben worden, was jetzt aber nachgeholt werden muss. Mikronährstoffe liefern im Gegensatz zu Kohlenhydraten bzw. Glukose, Fetten und Aminosäuren keine Energie, erfüllen bei fast allen Vorgängen in der Zelle gleichwohl wichtige Funktionen. Mikronährstoffe werden in der Regel mit der Nahrung aufgenommen, bei Bedarf stellt der Körper einige von ihnen auch selber her.
Mikronährstoffe sind notwendig bei der ...
- Verwandlung von Peptiden in eine Vielzahl von Derivaten,
- sind als Co-Enzyme an der Enzymtätigkeit beteiligt oder
- dienen als Radikalfänger und schützen die Zellen vor freien Radikale und oxidativem Stress durch reaktive Sauerstoff-Spezies (→ Abschnitt 14.13).
Zu den Mikronährstoffen zählen...
- Vitamine,
- vitaminähnliche Substanzen,
- die beiden n-3-Fettsäuren DHA und EPA,
- Mineralstoffe,
- Spurenelemente und
- Sekundärsubstanzen pflanzlichen Ursprungs.
Die nachfolgende Darstellung beschränkt sich auf das Nervensystem und die Bedeutung der Mikronährstoffe bei Transkription, Translation und wichtigen Funktionalprozessen, das sind Prozesse, die an Kernfunktionen von Hirnzellen mitwirken. Falls notwendig wird auch auf andere Funktionen hingewiesen, die im Gehirnstoffwechsel bedeutend sind.
Es geht – wie bei den vorigen Abschnitten – um das prinzipielle Verständnis. Mikronährstoffe sind selbstverständlich an sämtlichen Zellvorgängen beteiligt und im gesamten Körper aktiv. Auf die Beschreibung sekundärer Pflanzenstoffe, die beispielsweise aus Farb-, Bitter- und Gerbstoffen oder ätherischen Ölen bestehen, wird verzichtet.
Auch die Beschreibungen der 20 im menschlichen Organismus bedeutsamen Aminosäuren und ihre Funktionen als Enzym- und Proteinbausteine beschränken sich auf deren Rolle im zentralen Nervensystem.
2.3.1 Vitamine
Vitamine sind organische Verbindungen, die dem Körper von außen zugeführt werden müssen, weil er sie entweder gar nicht oder nicht in ausreichender Menge herstellen kann. Sie grenzen sich von den Mineralstoffen bzw. Spurenelementen ab, bei denen es sich um anorganische Substanzen handelt. Man unterscheidet fettlösliche und wasserlösliche Vitamine.
Vitamin-A-Gruppe (insbesondere Retinol)
Um im Körper wirksam zu sein und damit unerwünschte bzw. schädliche Aktivitäten unterbleiben, muss Retinol zuerst mit einem körpereigenen Retinol-Bindeprotein reagieren. Es ist für die Ausführung seiner Funktionen schon von vornherein von Proteinen abhängig.
- Transkription:
Vitamine der A-Gruppe sind an der Genregulation beteiligt. Sie fungieren als Stopp-Markierungen und unterbinden die Transkription von Peptiden bzw. deren Codes, die gerade nicht benötigt werden.
- Funktionale Prozesse von Gliazellen:
Vitamine dieser Gruppe sind an der Synthese des Myelins der Gliazellen im Gehirn und Rückenmark beteiligt.
Vitamin B1 (Thiamin)
Ähnlich wie das Retinol der Vitamin-A-Gruppe muss Thiamin mit einem Enzym verändert werden, bevor es im Stoffwechsel aktiv werden kann.
Eine direkte Beteiligung an der Transkription oder Translation in Hirnzellen ist nicht bekannt, jedoch ist Thiamin ‑ wie die weiteren B-Vitamine B2, B3, B5, B6 und B12 ‑ an der Aufspaltung der Proteine zu Aminosäuren im Verdauungssystem beteiligt. Erst dieser Vorgang ermöglicht die spätere Proteinbiosynthese.
- Funktionale Prozesse von Nerven- und Gliazellen:
1. Thiamin ist Bestandteil der Nervenzellmembranen, so dass eine Mitwirkung an der Nervenreizübertragung sicher ist.
2. Die Synthese und Aktivität wichtiger Neurotransmitter ist von Thiamin abhängig, nachgewiesen für GABA, Serotonin, Acetylcholin und Adrenalin, so dass Vitamin B1 auch an der Nervenreizübertragung beteiligt ist.
3. Thiamin schützt Cholin ‑ das ist die Vorstufe von Acetylcholin bzw. Phosphatidylcholin ‑ in Nerven- und Gliazellen vor Abbau und Aufspaltung.
Vitamin B2 (Riboflavin)
Auch Riboflavin übernimmt – wie Thiamin – Funktionen bei Aufspaltung des Nahrungsproteins in Aminosäuren.
- Funktionale Prozesse von Gliazellen:
Riboflavin ist gemeinsam mit Retinol aus der Vitamin-A-Gruppe beim Aufbau der Myelinschicht notwendig.
Vitamin B3 (Niacin)
Niacin hilft ebenfalls bei der Spaltung des Nahrungsproteins in seine Aminosäurebestandteile.
- Transkription:
Niacin ist für die Synthese der Histonproteine verantwortlich, die im Zellkern aktiv werden und u. a. DNA‑Brüche reparieren. Da Histone auch bei der Transkriptionsrate eine Rolle spielen, ist Niacin damit indirekt an der Genregulation beteiligt.
- Funktionale Prozesse von Nervenzellen:
Niacin verbindet sich mit mehr als 200 Enzymen, die auch im Zentralnervensystem eine Funktion übernehmen. So fördert Niacin beispielsweise die Synthese verschiedener Neurotransmitter.
- Weitere Besonderheiten im Zusammenhang mit dem Nervensystem:
1. Eine Unterversorgung mit Niacin hat ggf. einen indirekten, negativen Einfluss auf die Synthese des Neurotransmitters Serotonin. Im Falle eines Niacinmangels muss der Körper es aus der Aminosäure Tryptophan selber herstellen. Da Tryptophan wiederum wichtig für die Serotonin-Synthese ist, konkurrieren Serotonin- und Niacinproduktion miteinander.
Dazu kommen drei besondere Umstände, welche die ausreichende Produktionsmöglichkeit von Serotonin ggf. stören:
- Die Niacinsynthese ist nicht besonders effektiv und verbraucht viel Tryptophan, welches dann bei der Serotoninsynthese fehlt.
- Tryptophan ist in der Nahrung relativ zu den anderen Aminosäuren nur wenig enthalten, so dass die Gefahr eines Tryptophanmangels generell hoch ist.
- Tryptophan gehört zu den essentiellen Aminosäuren, die der Körper selber nicht herstellen kann. Daher kann ein Nahrungsmangel auch nicht durch körpereigene Produktion ausgeglichen werden.
2. Niacin ist ein Bestandteil des Glukosetoleranzfaktors, der Blutzuckerschwankungen glättet und somit auch einer Unterzuckerung nicht-diabetischen Ursprungs (Hypoglykämie‑Syndrom) entgegenwirkt, die für das Zentralnervensystem negative Folgen haben kann (→ Kapitel 4, Abschnitt 4.8.6).
Vitamin B5 (Pantothensäure)
Pantothensäure wird in der Form des Coenzyms A im Zellstoffwechsel aktiv. Es finden sich hohe Konzentrationen des Coenzyms A unter anderem im Gehirn. Auch an der Proteinaufspaltung ist es beteiligt.
- Funktionale Prozesse von Nerven- und Gliazellen:
1. Das Coenzym A ist an der Synthese des Neurotransmitters Acetylcholin beteiligt.
2. B5 wirkt an der Produktion von Taurin mit. Taurin hat mehrere Funktionen im Nervensystem, insbesondere im Bereich der Zellmembranstabilisierung und wirkt krampflösend bzw. beruhigend. Auch auf die Menge des Acetylcholins im zentralen Nervensystem hat Taurin einen positiven Einfluss, woraus vermutlich die leistungssteigernde Wirkung von Taurin resultiert. Somit ist die Pantothensäure für den Bestand des Neurotransmitters Acetylcholin doppelt wichtig.
Vitamin B6 (Pyridoxin)
Für Pyridoxin und dessen Derviate sind mehr als 200 enzymatische Reaktionen nachgewiesen. Seine allgemeine Bedeutung für das Nervensystem ist sehr hoch. Pyridoxin ist ein wichtiger Faktor im Stoffwechsel der Glukose, dem Energielieferanten des Gehirns.
Pyridoxin und dessen Derivate wirken an vielen Reaktionen im Aminosäurestoffwechsel mit, das heißt sie helfen bei der Synthese nicht-essentieller Aminosäuren. Wie schon beschrieben sind sie auch bei der Aufspaltung des Nahrungsproteins in Aminosäuren beteiligt.
- Funktionale Prozesse von Nerven- und Gliazellen:
1. Vitamin B6 wirkt am Aufbau der Neurotransmitter Serotonin, Dopamin und Noradrenalin mit.
2. Wie die Pantothensäure ist Pyridoxin auch für die Taurinbildung zuständig (wichtig z. B. für die Zellmembranstabilisierung, siehe oben bei B5).
Vitamin B7 (Biotin)
- Transkription und Translation:
1. Biotin arbeitet, u. a. gemeinsam mit B3, an der Veränderung der Histone mit. Wie B3 hat Biotin somit indirekt Auswirkungen auf die Genregulation, da Histone auf die Transkriptionsrate Einfluss nehmen.
2. Biotin ist für die Expression von mehr als 2.000 Genen zuständig, vermutlich auch in Zellen des zentralen Nervensystems.
- Weitere Besonderheiten im Zusammenhang mit dem Nervensystem:
Biotin ist wichtig für den Glukosestoffwechsel. Glukose ist der Energielieferant des Gehirns.
Vitamin B9 (Folsäure)
Das unter dem Namen Folsäure (seltener auch als Vitamin B11 bezeichnet) bekannte Vitamin wird erst durch die Umwandlung mittels eines Enzyms in Folat in der Leber biologisch aktiv – also auch hier ist wieder die Tätigkeit körpereigener Peptide nötig.
Vitamin B9 ist essentiell, der menschliche Organismus ist zur eigenen Produktion nicht in der Lage. Daher ist eine ausreichende Aufnahme über die Ernährung wichtig. Leider sind ca. 60 % der Menschen in Deutschland nur unzureichend mit Folsäure versorgt.
Es gibt in Deutschland daher eine Diskussion, Nahrungsmittel – insbesondere Weißmehl – mit Folsäure anzureichern. In den USA, Kanada und der Schweiz gingen Folsäuremangelerkrankungen (insbesondere Schädelknochen- und Neuralrohrerkrankungen) nach der gesetzlichen Einführung des Folsäurezusatzes signifikant zurück. In der Bundesrepublik wird eine solche Regelung von Seiten des Gesetzgebers mit dem Hinweis abgelehnt, jeder könne sich über eine gesunde Ernährung ausreichend mit Folsäure versorgen und ggf. zu Nahrungsergänzungsmittel greifen. Aus diesem Grunde kommen die genannten Erkrankungen in Deutschland leider vergleichsweise häufig vor.
Die Bedeutung des Vitamins B9 für Gehirn und Rückenmark ist sehr hoch. Sehr wichtige Funktionen übernimmt Folat im Rahmen der DNA-Replikation. Aber auch bei der Transkription und funktionellen Prozessen in Nervenzellen ist es maßgeblich beteiligt.
- Transkription:
Folat spielt eine wichtige Rolle beim Start der Transkription und damit bei der Synthese der Boten-RNA.
- Funktionale Prozesse von Nerven- und Gliazellen:
Folat ist an der Bildung vieler Neurotransmitter beteiligt, nachgewiesen insbesondere für Dopamin, Serotonin oder Noradrenalin.
Vitamin B12 (Cobalamin)
Cobalamin steht für eine Gruppe von sechs aktiven Substanzen, die alle Kobalt enthalten. Das Vitamin B12 ist die bedeutendste von ihnen und als Co-Enzym Teil mehrerer Enzyme.
B12 kann der Körper nicht selber herstellen und daher muss es mit der Nahrung oder Nahrungsergänzungsmitteln aufgenommen werden. Störungen bei der Absorption im Magen-Darm-Trakt sind bekannt, zum Beispiel bei Fehlen des Intrinsic-Faktors des Magens oder nach Operationen bzw. Erkrankungen am letzen Dünndarmabschnitt (sog. terminales Ileum, z. B. nach Operationen des Morbus Crohn). B12 wird nur mit Hilfe dieses Faktors und nur an speziellen Rezeptoren, die sich im terminalen Ileum befinden, aufgenommen.
Menschen mit chronischen Magen-Darm-Erkrankungen sollten daher ihre Resorptionsfähigkeit prüfen lassen, ebenfalls ältere Menschen, da mit zunehmendem Alter die Bildung des Intrinsic-Faktors zurückgeht.
B12 ist als eines der wenigen B-Vitamine in der Leber zeitlich begrenzt speicherbar. Da es bei veganer Ernährungsweise mittelfristig zu einem B12‑Mangel kommt, sollte hier die ergänzende Einnahme oder parenterale Verabreichung von B12 in Betracht gezogen werden.
B12 arbeitet eng mit B9 (Folsäure) zusammen, so dass die dort genannten Erkenntnisse indirekt auch auf Cobalamin zutreffen. Denn ohne B12 ist die Funktion von B9 blockiert oder eingeschränkt.
Wie schon bei anderen Vitaminen der B-Gruppe ist B12 auch an der Aufspaltung des Nahrungseiweißes in Aminosäuren beteiligt.
- Transkription:
B12 unterstützt die Synthese von DNA und Boten-RNA und sorgt damit auch für einen reibungslosen Ablauf von Zellteilung und Transkription.
- Funktionale Prozesse von Nerven- und Gliazellen:
1. Cobalamin ist für den Aufbau und Unterhalt bzw. Regeneration der Membranen Schwann'scher Gliazellen und Oligodendrocyten unerlässlich, und ohne B12 ist die Myelinschicht von Abbau bedroht.
2. Für die Metabolisierung verschiedener Neurotransmitter (beispielsweise Noradrenalin und Serotonin) verwendet eine Nervenzelle S-Adenosyl-Methionin (SAMe), ein Enzym, das wiederum mittels B12 synthetisiert wird.
3. Da B12 Cholin synthetisiert (→ Abschnitt 2.3.2), die Vorläufersubstanz des Neurotransmitters Acetylcholin und des Membranenbaustoffs Phosphatidylcholin, vergrößert sich dessen Einfluss auf die Funktionsfähigkeit der Nerven- und Gliazellen nochmals.
- Weitere Besonderheiten im Zusammenhang mit dem Nervensystem:
Bei einem B12-Mangel steigen die Konzentrationen bestimmter neurotoxisch wirkenden Substanzen an (nachgewiesen beispielsweise für Homocystein).
Vitamin C (Ascorbinsäure)
Ascorbinsäure ist vor allem für den Aufbau des Kollagens zuständig. Kollagen benötigt der gesamte Körper, nicht nur das Haut- und Bindegewebe. Ein Mangel an Vitamin C führt zu Skorbut, wie aus der Geschichte der Seefahrt bekannt ist. Noch im 18. Jahrhundert starben deswegen Seefahrer, die sich auf ihren Reisen fast ausschließlich von Fleisch ernährten, das kein Vitamin C enthält.
Primaten – und damit auch Menschen – gehören zu den wenigen Lebewesen, die Ascorbinsäure nicht selber produzieren.
- Funktionale Prozesse von Nerven- und Gliazellen:
1. Die Neurotransmitter Noradrenalin und Serotonin werden u. a. mit Hilfe von Vitamin C gebildet.
2. Gliazellen benötigen Vitamin C für die Kollagen-Synthese.
- Weitere Besonderheiten im Zusammenhang mit dem Nervensystem:
Die Ascorbinsäure ist auch für ihre antioxidativen Wirkungen bekannt, sie verhindert die negativen Wirkungen des Sauerstoffs und anderer Zellschädlinge in Nerven- und Gliazellen.
Vitamin-D-Gruppe (insbesondere Calciol bzw. Calcitriol)
Auch hierbei handelt es sich um eine Gruppe mehrerer Wirkstoffe, von denen das Calciol (auch als Vitamin D3 bezeichnet) der bedeutendste ist. Wie bei vielen anderen Vitaminen entsteht die Wirksamkeit im Körper erst durch eine Modifikation mit Hilfe des Enzyms 1‑alpha‑Hydroxylase zu Calcitriol.
Calciol ist ein nicht-essentielles Vitamin, das der Körper bei Lichteinwirkung mittels UV‑B‑Strahlung in der Haut produziert. Manche sind daher der Auffassung, dass es sich eher um ein Hormon als ein Vitamin handelt. Der strahlungsabhängige Calciol-Anteil deckt 90% des Körperbedarfs ab, den Rest liefert die durchschnitlliche Ernährung (Quelle: P. Knuschke et al., UV‑abhängige Vitamin D Synthese ‑ Bilanzierung der Expositionszeit durch UV zur Produktion des optimalen Vitamin D3‑Bedarfs im menschlichen Körper, Ressortforschungsbericht zur kerntechnischen Sicherheit und zum Strahlenschutz, 2007 ‑ 2011, Technische Universität Dresden und Medizinische Fakultät Carl Gustav Carus, Klinik und Poliklinik für Dermatologie).
Häufig reicht die körpereigene Menge jedoch nicht aus, da sich die Bevölkerung im Schnitt zu wenig dem Sonnenlicht aussetzt bzw. aus verschiedenen Gründen nicht aussetzen kann. Es wird allgemein angenommen, dass ein großer Teil der Bevölkerung mit Vitamin D unterversorgt ist. In der Bundesrepublik vertreten viele Fachleute diese Meinung, besonders hervorzuheben sind der Mediziner Prof. Jörg Spitz und der Ernährungswissenschaftler Dr. Nicolai Worm.
- Transkription:
Im Bereich von Darm, Knochen und Niere ist die Beteiligung an der Transkription über den Vitamin-D-Rezeptor (VDR) bekannt. Das ist auch im Bereich des Gehirns möglich, dazu gibt es aber derzeit noch keine Nachweise oder Studien.
- Funktionale Prozesse von Nerven- und Gliazellen:
1. Vitamin D ist an der Reizleitgeschwindigkeit motorischer Nervenzellen und am Wachstum von Nerven- und Gliazellen beteiligt. Letzteres erfolgt durch eine Beeinflussung der Synthese von Nervenwachstumsfaktoren durch Calcitriol.
2. Studien lassen darauf schließen, das Vitamin D auch an der Neurotransmitter-Synthese seinen Anteil hat. Die genauen Ursache-Wirkungs-Beziehungen sind jedoch noch unbekannt.
3. Im gesamten Gehirn befinden sich Calcitriol-Rezeptoren: im präfrontalen Cortex, Thalamus und Hippocampus, außerdem im Kleinhirn. Deren Bedeutung ist noch weitgehend unbekannt und Gegenstand der Forschung.
4. Untersuchungen deuten auf einen Zusammenhang zwischen neurologischen und psychiatrischen Erkrankungen und einem Vitamin-D-Mangel hin, insbesondere bei Morbus Parkinson, Multipler Sklerose, Depressionen und Demenz. Die genauen Ursachen und Wirkungen sind nicht bekannt, ergeben sich eventuell aus den oben geschilderten Zusammenhängen.
Weitere Besonderheiten im Zusammenhang mit dem Nervensystem:
1. Vitamin D steuert die Entwicklung des Zentralnervensystems im Embryonalstadium durch dessen positiven Einfluss auf Wachstumsfaktoren für Nerven- und Gliazellen.
2. Vitamin D bzw. D3 soll auch antioxidative Wirkungen haben, was dem Schutz der DNA vor Mutationen zugute kommt. Hier ist der Kenntnisstand jedoch noch dürftig.
Vitamin-E-Gruppe (Tocopherole und Tocotrienole)
Insgesamt zählen 16 Substanzen zur Gruppe der E-Vitamine, je vier davon gehörten zu den Tocopherolen bzw. den Tocotrienolen (alpha-, beta-, gamma- und delta-Tocopherole bzw. -Tocotrienole). Das bekannteste E‑Vitamin ist das alpha-Tocopherol.
- Transkription und Translation:
Ein Einfluss von alpha-Tocopherol auf die Genexpression während der Transkription ist durch Studien belegt, allerdings noch nicht für die das Nervensystem betreffenden Gene. Eine andere Untersuchung in den USA führte zur Feststellung, dass Tocotrienole einen Einfluss auf die Genexpression im Zusammenhang mit der Cholesterin-Synthese haben. Es besteht wegen dieser Erkenntnisse eine gewisse Wahrscheinlichkeit, dass E-Vitamine auch Aufgaben während der Proteinbiosynthese im Nervensystem erfüllen.
- Weitere Besonderheiten im Zusammenhang mit dem Nervensystem:
Die Hauptaufgabe der E-Vitamine ist der Schutz innerer und äußerer Zellmembranen vor freien Radikalen und reaktiven Sauerstoff-Spezies (ROS) – also aggressiven Einwirkungen von innen und außen – , so dass es nicht zu Membranschäden kommt. Der ständige, ungeschützte Beschuss von freien Radikalen und ROS führt zum vorzeitigen Erkranken der Zelle und schließlich zum Zelltod (→ u. a. Abschnitt 14.13.3).
Vitamin K-Gruppe (Phyllochinon bzw. Menachinon)
Die beiden K-Vitamine sind hauptsächlich für die Blutgerinnung und den Aufbau des Knochensystems zuständig, hier über eine Beeinflussung der Transkription zweier Gene, die in diesem Zusammenhang benötigt werden. Die Hälfte des Bedarfs an Vitamin K produziert der Köper selbst.
Über einen direkten Zusammenhang zwischen den beiden K‑Vitaminen und dem Nervensystem ist nichts bekannt.
2.3.2 Vitaminähnliche Substanzen
Vitaminähnliche Substanzen oder „Pseudo-Vitamine“ sind organische Mikronährstoffe, die sowohl Bestandteil der Nahrung sind als auch vom Körper synthetisiert werden. Der Unterschied zu Vitaminen besteht in der Annahme, dass der Körper sie in ausreichender Menge herstellen kann, er wäre also auf eine Zufuhr von außen nicht angewiesen. Ein Vitamin ist ja gerade dadurch gekennzeichnet, dass der Körper es entweder gar nicht oder nicht in genügender Menge selber herstellt.
Die beiden Substanzen Phosphatidylcholin und -inositol gehören zur Gruppe der Phospholipide und werden als fettähnliche bzw. lipotrophe Substanzen den Fettbegleitstoffen zugeordnet. Da sie in der Literatur aber meist zusammen mit Vitaminen erörtert werden und früher auch einen Vitamin-Status hatten, erfolgt deren Darstellung schon jetzt. Die Erläuterung weiterer Fettbegleitstoffe erfolgt im Abschnitt 2.4.
Viele Pseudo-Vitamine stufte man zunächst als Vitamine ein, später wurde ihnen dieser Status aber wieder aberkannt oder er ist umstritten.
Hierzu noch einige Anmerkungen:
- Für die vollständige Synthese eines „Pseudo-Vitamins“ ist ein gesunder Organismus notwendig. In Phasen der Krankheit oder bei anderweitigen Belastungen, beispielsweise erhöhtem psychischen Stress, und daraus resultierendem erhöhten Bedarf wird ein sogenanntes Pseudo-Vitamin kurzfristig oft zu einem „echten“ Vitamin mit der Notwendigkeit, den zusätzlichen Bedarf von außen zu decken.
- Ebenfalls ist oft ungeklärt, wie viel von einer Substanz tatsächlich benötigt wird, denn die Ansichten ändern sich häufiger.
- Es ist zu hinterfragen, warum der Körper eine Substanz selber herstellt, die bei einer durchschnittlichen Ernährungssituation dem Körper zugeführt wird. Das liegt entweder daran, dass der Körper an eine bestimmte Menge durch Nahrungsaufnahme gewohnt ist, welche aber nicht ausreicht oder dass es häufiger zu Schwankungen in der Nahrungsaufnahme kommt. In beiden Fällen handelt es sich nach unserer Definition bei der Substanz aber unbedingt um ein Vitamin.
- Eine ausreichende Aufnahme über die Nahrung ist sinnvoll, da eine vollständige Eigensynthese Ressourcen bindet oder den Organismus in einer anderen Weise belastet.
Auf die Vitaminstatus-Diskussion der Substanzen soll hier aber nicht weiter eingegangen werden. Allerdings ist es aus den o. g. Gründen ein Trugschluss zu glauben, es käme bei „Pseudo-Vitaminen“ nicht auf eine ausreichende Zufuhr von außen an.
Nachfolgend die beiden wichtigsten Vertreter, wie gewohnt im Zusammenhang mit ihren Funktionen im Nervensystem bei der Proteinbiosynthese und den funktionalen Prozessen.
Darüber hinaus sind noch erwähnenswert Phosphatidylserin (→ Abschnitt 2.4.2), Phosphatidylethanolamin und Phosphatidylglycerin, die ähnliche Rollen im Zentralnervensystem spielen.
Cholin/Phosphatidylcholin
Vor der Aberkennung als Vitamin gab es für Cholin die Bezeichnung B4, die heute aber manchmal noch verwendet wird. Es gibt Studien aus den USA, die einen täglichen Aufnahmebedarf von drei bis vier Gramm feststellten. Viele Wissenschaftler sind daher der abweichenden Meinung, dass der Organismus Cholin nicht ausreichend synthetisiert und eine zusätzliche Aufnahme notwendig ist. In diesem Falle müsste Cholin den Vitaminstatus aber wieder erhalten.
Über die Nahrung wird die Substanz so gut wie ausschließlich als Phosphatidylcholin aufgenommen, in der Leber resorbiert und steht dann als Cholin zur Verfügung. Zusätzlich wird körpereigenes Cholin in Leber und Nieren synthetisiert. Für die Synthese müssen genügend Aminosäuren, insbesondere Lysin und Methionin, zur Verfügung stehen.
Cholin übernimmt außerhalb des Nervensystems als Bestandteil der Gallensäure die Aufgabe der Fett-Emulgation und ist damit an der Fettverdauung beteiligt. Außerdem wird Cholin in den Körperzellen für die Membranen benötigt.
Cholin durchdringt die Blut-Hirn-Schranke und wird in den Hirnzellen entweder wieder zu Phosphatidylcholin synthetisiert oder dient als Grundsubstanz der Herstellung des Botenstoffs Acetylcholin.
- Funktionale Prozesse von Nerven- und Gliazellen:
1. Cholin ist die Grundlage der Synthese von Acetylcholin, einer der am häufigsten verwendeten Botenstoffe. Acetylcholin ist der wichtigste Neurotransmitter des peripheren Nervensystems, aber auch im Gehirn spielt Acetylcholin verschiedene Rollen, die noch nicht bis ins letzte Detail geklärt sind. So kontrolliert Acetylcholin zum Beispiel den Herzschlag oder den Blutdruck durch Aktivitäten in den dafür zuständigen Bereichen des Stammhirns. Weiter ist Acetylcholin für die Konzentrationsfähigkeit, Wahrnehmung, Entscheidungsfähigkeit, Lernvorgänge und das Erinnerungsvermögen zuständig.
Medikamente gegen die Alzheimer-Demenz setzen am Acetylcholin-Stoffwechsel an, in dem sie dessen Abbau blockieren. Die Konzentrationserhöhung des Acetylcholins führt dann zu einer Verzögerung des Fortschreitens der Erkrankung.
Nervenzellen, die Acetylcholin verwenden, nennt man „cholinerge Nerven“. Bei einer Unterversorgung mit Cholin sind cholinerge Nerven vom Absterben bedroht.
2. Cholin wird für den Aufbau der Zellmembranen im Zellinneren wieder zu Phosphatidylcholin synthetisiert, also der Form, in der es schon über die Nahrung zugeführt wurde. Diese Substanz ist zu 50% Bestandteil der äußeren Zellmembranenschicht im menschlichen Körper und daher für die Funktionsfähigkeit von Nerven- und Gliazellen wichtig.
- Weitere Besonderheiten im Zusammenhang mit dem Nervensystem:
Es besteht ein Zusammenhang zwischen der Menge des für das Nervensystem schädlichen Schlackenstoffs Homocystein und Cholin, da Cholin den Homocystein-Spiegel senkt.
Das Membran-Phosphatidylcholin sorgt darüber hinaus dafür, dass ein anderer Membranbestandteil, das Cholesterin, seine Viskosität behält und nicht verkrustet, denn das würde den Zelltod bedeuten.
Inositol (Myo-Inositol)/Phosphatidylinositol
Auch Inositol hatte – wie das Cholin – früher einen Status als B‑Vitamin, er ist aber heute aus den gleichen Gründen umstritten. Myo-Inositol ist die für den menschlichen Organismus hauptsächlich verwertbare Form des Inositols, woraus der Körper dann verschiedene Inositolverbindungen synthetisiert – beispielsweise Phosphatidylinositol, die in den Zellmembranen und der Muskulatur wirkende Substanz. Die Konzentration von Myo-Inositol ist im Gehirn besonders hoch. Andere Inositolformen, beispielsweise Scyllo-Inositol, sind auch im Gehirn in geringerer Konzentration vorhanden (etwa 10% des Myo-Inositol-Anteils).
- Transkription und Translation:
In Pflanzen- und Hefezellen ist die Beteiligung von Inositol an der Genexpression belegt. Inositol ist deswegen auch ein ausgezeichnetes Düngemittel für Pflanzen. Für den menschlichen Organismus und insbesondere die Proteinsynthese im Nervensystem sind keine Funktionen bekannt, jedoch besteht eine gewisse Wahrscheinlichkeit.
- Funktionale Prozesse von Nerven- und Gliazellen:
1. In der Hauptsache ist Phosphatidylinositol ein Bestandteil der Zellmembranen, wenn auch in wesentlich geringerem Umfang als Phosphatidylcholin. Hier ist es ausschließlich in der inneren Zellmembranschicht lokalisiert und für die Membranfunktionen von grundlegender Bedeutung.
2. Inositol-1,4,5-triphosphat, kurz IP3, hat vielfältige Auswirkungen, da es an der Weiterleitung von äußeren Signalen ins Zellinnere beteiligt ist, beispielsweise indem es an spezifische IP3-Rezeptoren innerer Zellmembranen andockt.
3. Im Nervensystem ist es an der Reizverarbeitung beteiligt, da es Teil des Enzyms Na1/K1-ATPase ist und damit für die reibungslose Impulsübertragung sorgt.
Hier gibt es Untersuchungen an Diabetes-Patienten: Deren hohe Blutzuckerkonzentration führt zu einer Myo-Inositol-Depletion, also einen Rückgang der Substanz bzw. höheren Verbrauch mit der Folge, dass das Na1/K1-ATPase-Enzym in seiner Funktion gestört ist. Dadurch ergeben sich Störungen in der Nervenreizübertragung durch energetische Erschöpfung, nämlich Amplitudenreduktionen und Minderungen der Nervenleitgeschwindigkeit, was die Entstehung Diabetes-bedingter Neuropathien begünstigt.
2.3.3 Docosahexaensäure (DHA) und Eicosapentaensäure (EPA)
Da auch die Fettsäuren DHA und EPA in der Literatur meist im Zusammenhang mit Vitaminen und anderen Mikronährstoffen besprochen werden, sollen sie auch in diesem Abschnitt kurz vorgestellt werden. Detailliertere Informationen zu Fettsäuren und über andere Fettsäurearten sind jedoch in ausführlicherer Form Themen des nachfolgenden Abschnittes 2.4 über Nahrungsfette.
DHA und EPA synthetisiert der Körper aus der n‑3‑Alpha‑Linolenfettsäure (→ Abschnitt 2.4), jedoch reichen die Mengen bei weitem nicht aus. Daher werden DHA und EPA als bedingt essentiell bezeichnet. Eine Aufnahme über die Ernährung ist daher notwendig. Beide Fettsäuren gelangen fast ausschließlich durch den Konsum von Fischen in den Körper.
DHA und EPA gehören zur Gruppe der mehrfach ungesättigten Fettsäuren, die leicht oxidieren und sich dabei zu schädlichen Transfettsäuren wandeln. Deshalb ist die parallele Versorgung mit antioxidativ wirkenden Mikronährstoffen (u. a. Vitamin C und E‑Vitamine) wichtig.
- Funktionale Prozesse von Nerven- und Gliazellen:
1. DHA hat einen Anteil an der Gehirnsubstanz von 15 Prozent, denn die fettreichen Hirnzellmembranen bestehen zu einem Viertel aus DHA. Sie sorgt dort für eine ausreichende Membranbeweglichkeit, so dass die Membran ihre Funktionen optimal ausführen kann.
2. Für Tätigkeit der myelinbildenden Gliazellen ist DHA unbedingt notwendig.
2. EPA ist an der Synthese der Serie-3-Eicosanoide beteiligt, die im Gehirn botenstoffähnliche Wirkungen haben und darüber hinaus dort auch entzündungshemmende Aktivitäten entfalten.
2.3.4 Mineralstoffe (Elektrolyte)
Mineralstoffe bzw. Elektrolyte sind – im Gegensatz zu Vitaminen – anorganische Mikronährstoffe. Damit gleichen sie den Spurenelementen, jedoch werden sie in einer höheren Konzentration benötigt und daher unterschieden. Die Grenze der Trennung liegt bei 50 mg pro kg Körpergewicht.
Wie die Vitamine müssen Mineralstoffe dem Körper von außen zugeführt werden, in der Regel über die Nahrung. Für das Nervensystem sind fünf Mineralstoffe von Bedeutung: Calcium, Kalium, Natrium, Magnesium und Phosphor.
Calcium
Calcium ist der am häufigsten im Körper vorkommende Mineralstoff, ein durchschnittlich schwerer männlicher Erwachsener enthält ca. 1 kg Calcium. Es findet sich zu 99% in Knochen und Zähnen. Dennoch ist der kleine Rest von einem Prozent für das Nervensystem bedeutend.
- Transkription:
Calcium ist zusammen mit dem cAMP-Reaktions-Element (CRE) an der Genexpression im Nervensystem beteiligt. Calcium sorgt für die Umwandlung des im Zellkern inaktiven CRE zum aktiven CREB (cAMP‑Reaktions‑Element‑Bindungsprotein), welches die Transkription mehrerer Gene von neuroaktiven Substanzen einleitet, und zwar Katecholamine (Adrenalin, Noradrenalin und Dopamin), Neuropeptide und Neurotrophine.
- Funktionale Prozesse von Nervenzellen:
Calcium ist – zusammen mit Kalium und Magnesium – an der Reizweiterleitung der Nerven beteiligt. Wenn ein Impuls die Synapse erreicht, strömen Calcium-Ionen durch Kanäle in die Nervenzelle. Die genauen Gründe und Auswirkungen dieses Vorgangs sind immer noch nicht vollständig geklärt.
Chlorid
Chlorid kommt nur in Verbindung mit anderen Mineralstoffen und Spurenelementen vor, wobei das nachfolgend beschriebene Natrium daran mit Natriumchlorid den größten Anteil hat. Chlorid und Natrium arbeiten auch im Nervensystem eng zusammen. Die Informationen zum Natrium gelten daher auch für Chlorid.
Kalium und Natrium
Kalium steht bezüglich seiner Konzentration im menschlichen Körper im Vergleich mit anderen Mineralstoffen an vierter Stelle (ca. 100 bis 150 Gramm). Im Nervensystem ist es, wie das Calcium, zusammen mit dem Natrium an der Reizweiterleitung beteiligt. Kalium verbindet sich mit zahlreichen Enzymen und übernimmt dabei viele Funktionen. In der Regel steht genügend Kalium in der Nahrung zur Verfügung.
Natrium ist im Organismus etwas weniger vorhanden als Kalium. Natrium wird überwiegend über das Salz in der Nahrung aufgenommen, in der Regel entsteht beim Menschen kein Natriummangel.
Kalium und Natrium sind nicht direkt an der Proteinbiosynthese beteiligt. Natrium hilft jedoch – wie einige B‑Vitamine – bei der Resorbierung von Aminosäuren aus der eiweißhaltigen Nahrung, der Vorstufe der Proteinsynthese.
- Funktionale Prozesse von Nervenzellen:
1. Kalium und Natrium bewerkstelligen als Gegenspieler gemeinsam die Weiterleitung von Nervenreizen. Dazu strömen kurzfristig Natrium-Ionen durch die Membran in die Nervenzelle, danach strömen Kalium-Ionen aus der Nervenzelle. Diese kurzfristige Ionenverschiebung stellt den Impuls dar. Dazu muss natürlich auch ein Zustand in Ruhe herrschen, der durch die Natrium-Kalium-Pumpe erzielt wird – Nervenzellmembranen pumpen ständig Natrium-Ionen aus der Zelle und Kalium-Ionen hinein.
2. Beide Substanzen sind ebenfalls an der Übertragung von Nervenreizen zwischen den Nervenzellen beteiligt.
Magnesium
Magnesium ist in einer relativ niedrigen Konzentration von nur ca. 25 Gramm im menschlichen Körper enthalten, davon etwa zur Hälfte im Knochengewebe. Mehr als 300 Enzyme benötigen Magnesium als Co-Faktor, wovon vor allem Energiestoffwechsel und die Proteinsynthese betroffen sind. Magnesium regelt die Durchlässigkeit der Zellmembranen und im Nervensystem auch die Reizweiterleitung.
- Transkription und Translation:
1. Magnesium ist Bestandteil der RNA-Polymerase, die im Verlauf der Transkription RNA-Nukleotide zu Basenketten verknüpft.
2. Magnesium spielt bei der Translation eine wichtige Rolle. Die beiden Teile der Ribosomen müssen sich vor Beginn des Translationsprozesses vereinen, was nur mit Hilfe von Magnesium möglich ist. Magnesium ist ebenfalls als Co-Faktor an der Beladung der tRNA mit Aminosäuren beteiligt, ohne die eine Translation überhaupt nicht möglich ist.
3. Magnesium bildet darüber hinaus die Sekundärstruktur von Nukleinsäuren.
- Funktionale Prozesse von Nerven- und Gliazellen:
1. Magnesium hat bei der Reizweiterleitung eine hemmende Funktion und damit eine beruhigende Wirkung auf übermäßig aktive Nervenzellen. An den präsynaptischen Endkolben der Nervenleitungen vermindert Magnesium die Transmitterausschüttung.
2. Magnesium ist für die Funktion des N-Methyl-D-Aspartat-Rezeptors zuständig, der langfristige Veränderungen der Nervenreizübertragung steuert.
3. Beispiele für die Funktionen des Magnesiums als Co-Faktor zahlreicher Vorgänge im Nervensystem sind die Enzyme Serinracemase, Calcium-Calmodulin-abhängige Proteinkinase II und die Proteinkinase C, welche verschiedene Prozesse an den Synapsen der Nervenzellen und in Gliazellen überwachen.
Phosphor
Phosphor – vor allem in Form der Phosphat-Verbindungen – ist das zweithäufigste Element in unserem Körper nach Calcium (ca. 700 Gramm) und Bestandteil vieler Enzyme. Es ist in fast jedem Lebensmittel enthalten, so dass Mangelversorgungen nicht zu erwarten sind.
Vor allem bei ungesunder Ernährungsweise (viel Fleisch, raffinierter Zucker und phosphathaltige Limonaden) erhält der Körper eher ein Überangebot an Phosphor. Auch Phosphor befindet sich zu 90% hauptsächlich in den Knochen und Zähnen.
- Transkription und Translation:
Phosphate sind Bestandteile von DNA und RNA und grundlegend für die Proteinsynthese im gesamten Körper – und damit auch im Nervensystem.
- Funktionale Prozesse von Nerven- und Gliazellen:
1. Als Bestandteil der Membranlipide, insbesondere bei den Myelin-Membranen der Gliazellen, ist Phosphor wichtig für das Nervensystem.
2. Phosphat verbindet sich mit Cholin und Inositol zu Phosphatidylcholin bzw. Phosphatidylinositol und wird in diesen Formen in den Hüllen der Nerven- und Gliazellen aktiv. Weitere Verbindungen sind Phosphatidylserin, Phosphatidylethanolamin und Phosphatidylglycerin, die im Gehirn ähnliche Funktionen haben.
2.3.5 Spurenelemente
Spurenelemente unterscheiden sich von den anorganischen Mineralstoffen nur durch ihren geringen Bedarf. Das drückt sich in der Konzentration pro kg Körpergewicht aus, die weniger als 50 mg beträgt.
Bor
(Text folgt)
Chrom
Das Funktionsspektrum von Chrom ist noch sehr unklar. Chrom wird vor allem mit dem Glukosestoffwechsel in Verbindung gebracht, da es ‑ wie auch das Vitamin B3 ‑ als Bestandteil des Glukosetoleranzfaktors den Kurvenverlauf des Zuckers im Blut glättet (→ Kapitel 4, Abschnitt 4.8.6).
- Transkription:
Die Konzentration von Chrom in den Zellkernen ist auffällig hoch, so dass Chrom mit der Zellteilung oder Transkription in Verbindung stehen könnte. Näheres ist darüber derzeit nicht bekannt.
- Weitere Besonderheiten im Zusammenhang mit dem Nervensystem:
Menschen, die einen chronisch niedrigen Blutzuckerspiegel oder einen ungünstigen Verlauf der Glukosekonzentrationskurve haben (Hypoglykämie-Syndrom) und dadurch zu Depressionen, Müdigkeit und Antriebsschwäche neigen, hilft Chrom durch Anhebung und Glättung der Blutzuckerkurve (→ Kapitel 4).
Eisen
Die bekanntesten Funktionen von Eisen sind der Transport und die Speicherung von Sauerstoff oder die Beteiligung am Energiestoffwechsel. Beides hat natürlich erhebliche Auswirkungen auf das Nervensystem, da gerade hier Energie- und Sauerstoffbedarf sehr hoch sind.
Ebenfalls sinkt bei Eisenmangel der Spiegel des Schilddrüsenhormons Thyroxin, verbunden mit einer Verminderung des Stoffwechsel-Grundumsatzes und erheblichen psychischen Befindlichkeitsstörungen.
Darüber hinaus hat Eisen aber auch noch eine Menge weiterer Aufgaben im Zentralnervensystem. Teilweise sind die Funktionen und Zusammenhänge nicht geklärt, jedoch kann aufgrund der Untersuchungen von Eisenmangelzuständen auf eine Mitwirkung von Eisen geschlossen werden.
- Funktionale Prozesse:
Eisenmangel führt zu einer Unterversorgung mit den Neurotransmittern Dopamin, Serotonin, GABA und Acetylcholin.
- Weitere Besonderheiten im Zusammenhang mit dem Nervensystem:
Zum Krankheitsbild des Eisenmangel-Syndroms ohne Anämie gehört auch die Depression. Bei einem Eisenmangel-Syndrom ohne Anämie liegt kein messbarer oder ein nur geringer Eisenmangel vor, Blutbildung und Sauerstoffversorgung sind nicht eingeschränkt. Dennoch verschwinden die Symptome nach Einnahme von Eisenpräparaten oder Eiseninfusionen.
Die Gründe dafür sind unklar, hängen aber wahrscheinlich mit den negativen Folgen einer Unterversorgung mit den o. g. Botenstoffen oder Problemen in der Energieversorgung zusammen.
Da der Organismus mit dem zur Verfügung stehenden Eisen zunächst einmal die überlebenswichtige Sauerstoffversorgung sicherstellt, könnten schon kleinere Mängel dazu führen, dass untergeordnete Funktionen im Zusammenhang mit den Neurotransmittern dabei auf der Strecke bleiben.
Jod
Die Bildung der Schilddrüsenhormone Thyroxin und Triiodthyronin ist nur mit Jod möglich und hier liegt auch die einzige Aufgabe des Spurenelements: Thyroxin enthält vier Jodatome, Triiodthyronin drei Jodatome. Beide Substanzen werden schon im Mutterleib dringend benötigt, da sie beim Fötus u. a. den Aufbau von Gehirn und Rückenmark steuern. Ihre Aufgaben setzen sie nach der Geburt fort.
Der Mangel an Thyroxin und Triiodthyronin kann mehrere Ursachen haben, zum Beispiel Fehlsteuerungen im Zwischenhirn durch eine gestörte Hypothalamus-Hypophysen-Achse, Veränderungen bzw. Erkrankungen der Schilddrüse (z. B. Minderung der Hormonproduktion durch „kalte Knoten“ in der Schilddrüse, Jodverwertungsstörungen) oder zu wenig Jod in der Nahrung sind mögliche Gründe.
- Transkription:
Beide jodhaltigen Schilddrüsenhormone regulieren die Genexpression in der Transkriptionsphase. Dadurch steuern sie dann die o. g. Entwicklung von Gehirn und Rückenmark bis ins Kleinkindalter.
- Funktionale Prozesse von Nerven- und Gliazellen:
Jodhaltige Schilddrüsenhormone wirken aktivierend u. a. auf das Gehirn, da sie den Grundumsatz des Organismus regeln. Ist die Konzentration von Thyroxin und Triiodthyronin aufgrund eines Jodmangels niedrig, führt das zur Verlangsamung der Stoffwechselvorgänge und oft zu einer depressiven Symptomatik.
Kobalt
Seine Bedeutung erhält Kobalt durch seine Eigenschaft als Bestandteil von Vitamin B12. Daher gelten die dort beschriebenen Zusammenhänge auch für Kobalt.
Kupfer
Kupfer hat mehrere Aufgaben als Co-Enzym: Es ist am Energiestoffwechsel beteiligt, hat seinen Anteil an der Blutbildung und am Aufbau des Bindegewebes (Kollagen- und Elastinbildung).
- Funktionale Prozesse von Nerven- und Gliazellen:
1. Kupfer wirkt durch seine Beteiligung an der Bildung von Adrenalin und Noradrenalin indirekt auf das Gehirn. Adrenalin und Noradrenalin werden mit Hilfe von Kupfer (daneben Vitamin C, B6, B12 und Folsäure) vorwiegend in der Nebenniere und im peripheren Nervensystem gebildet. Die im Gehirn benötigte Menge wird allerdings dort selbst synthetisiert, da beide Substanzen an der Blut-Hirn-Schranke nicht vorbeikommen. Adrenalinrezeptoren wurden vorwiegend in den der Formatio reticularis (→ Abschnitt 1.3.1) zugehörigen Nervenzellen des Gehirns gefunden, ihre Funktionen sind aber bis heute nicht geklärt.
2. Den Neurotransmitter Dopamin wandelt ein kupferhaltiges Enzym in Noradrenalin um und steuert dadurch u. a. euphorische Gefühle.
3. Kupfer ist in den Gliazellen an der Myelin-Synthese beteiligt und hält als Bestandteil eines Enzyms die Myelinschicht feucht.
Mangan
Mangan gehört zu den essentiellen Spurenelementen und reagiert mit mehr als 50 Enzymen. Der Mangan-Bedarf wird durch die Nahrungsaufnahme i. d. R. gedeckt. Allerdings sollte man dafür nicht allzu viel Alkohol, Zucker und Weißmehl zu sich nehmen.
Mangan arbeitet mit Vitamin B1 zusammen, das – wie oben beschrieben – einige Funktionen im Nervensystem erfüllt.
Mangan findet sich in Ribonukleotidreduktasen und ist dadurch bei der DNA-Synthese beteiligt.
In zu hohen Dosen ist Mangan sehr schädlich – vor allem für das Nervensystem; dort kann eine hohe Mangankonzentration beispielsweise zu sekundären Parkinson-Syndromen führen.
- Funktionale Prozesse von Nerven- und Gliazellen:
1. Mangan synthetisiert – zusammen mit anderen Substanzen – den Neurotransmitter Dopamin.
2. Im Gehirn findet man Mangan in bestimmten Bereichen als Bestandteil von Enzymen vor allem in den Gliazellen.
Molybdän
Viele Prozesse benötigen die Hilfe des Molybdäns, obwohl der menschliche Körper im Schnitt nur 10 mg dieses Spurenelements enthält. Es spielt als Co-Faktor in der Zusammenarbeit mit vielen Proteine eine Rolle, beispielsweise im Energiestoffwechsel oder beim Aufbau wichtiger bzw. Abbau schädlicher Substanzen. Im Zentralnervensystem ist keine unmittelbare Funktion bekannt.
Rubidium
Rubidium zählt zu den unbekannteren Mikronährstoffen, dessen Bedeutung für das Nervensystem sich nur langsam aufklärt. Im menschlichen Organismus kommt es in sehr kleinen Mengen im Gehirn vor.
- Funktionale Prozesse von Nerven- und Gliazellen:
Es wird vermutet, dass Rubidium an der Übertragung von Nervenreizen durch die Regelung der Botenstoffkonzentration beteiligt ist. Daher wird darüber diskutiert, Rubidium als komplementären Therapiewirkstoff bei der Behandlung der Depression einzusetzen. Allerdings nimmt jeder Mensch mit seiner Nahrung täglich ein Vielfaches des geschätzten Bedarfs von ca. 100 Mikrogramm pro Tag zu sich ‑ er ist zum Beispiel in besonders hoher Konzentration in Kaffee und Tee zu finden.
Selen
Selen ist Bestandteil vieler Enzyme und Proteine. Selenproteine werden in einer ungewöhnlichen Art translatiert: Selenocystein, eine durch Selen modifizierte Form der Aminosäure Cystein, wird auf die gleiche Weise wie die 20 natürlichen Aminosäuren mit Hilfe einer bestimmten Basenfolge auf der Boten-RNA in die Peptidkette integriert, obwohl sie anders strukturiert ist. Manche bezeichnen Selenocystein daher als „21. Aminosäure“. Auf jeden Fall ist es so, dass DNA und RNA über die 20 Aminosäuren hinaus weitere Codierungsmöglichkeiten haben.
Untersuchungen haben ergeben, dass die Selenversorgung in Deutschland eher an der unteren Grenze der empfohlenen Menge liegt, jedoch noch nicht von einer Mangelversorgung ausgegangen wird. Einige Gruppen von Menschen, zum Beispiel Veganer, Alkoholiker oder Magersüchtige, sind allerdings oft unzureichend mit Selen versorgt.
- Funktionale Prozesse von Nerven- und Gliazellen:
Selenhaltige Enzyme sind an der Aktivierung und Deaktivierung von Adrenalin und Noradrenalin beteiligt und beeinflussen damit Antrieb und Stimmungslage.
Es gibt Hinweise darauf, dass es bei Selenmangel zu einer Depression kommen kann, zumindest zeigten einige Studien, dass niedrige Selenwerte und Depression häufig gemeinsam auftraten. Die Gründe dafür sind noch nicht nachgewiesen, es könnte aber aus den o. g. Zusammenhängen resultieren.
- Weitere Besonderheiten im Zusammenhang mit dem Nervensystem:
1. Selen erfüllt – wie Vitamin C oder die E-Vitamine – vor allem antioxidative Funktionen, denn es wird für die Synthese antioxidativ wirkender Enzyme benötigt. Selen schützt dadurch auch Nerven- und Gliazellen.
2. Selen bewahrt den Organismus vor zu hohen Konzentrationen des Nervengifts Glutaminsäure.
Zink
Zink ist ein Co-Faktor vieler Enzyme und findet sich in bestimmten Hirnregionen in höherer Konzentration. Studien aus den USA belegen, dass sich eine gute Zinkversorgung positiv auf das Nervensystem auswirkt, zum Beispiel steigert es Gedächtnisleistung und Konzentrationsfähigkeit.
Forscher des Max-Planck-Instituts für Hirnforschung weisen in einer Studie ebenfalls zahlreiche Beziehungen zwischen Zink und dem zentralen Nervensystem nach. Es wird vermutet, dass Zink wie ein natürlicher Dopamin-Wiederaufnahmehemmer wirkt und so dafür sorgt, dass mehr des antriebssteigernden Dopamins für die Nervenreizübertragung zur Verfügung steht.
Frühere Studien kamen allerdings zu dem Ergebnis, dass Zink im Gehirn eher keine Rolle spielt.
- Transkription:
1. Zinkhaltige Enzyme und Proteine haben bei der Transkription zwei wichtige Funktionen. Zink ist zum einen Bestandteil der Zinkfingerproteine. Diese Proteingruppe zählt zu den Transkriptionsfaktoren, die für die Initiation der RNA‑Polymerasen zuständig sind.
2. Darüber hinaus ist Zink ebenfalls Bestandteil sowohl der RNA‑ als auch der DNA‑Polymerasen, der Thymidin‑Kinase, der reversen Transkriptase und der Ribonuklease und damit unentbehrlich für die Synthese der Nukleinsäuren.
3. Da Zink auch für die Synthese des Retinol‑Bindeproteins benötigt wird, sind die Funktionen des Retinols von Zink abhängig. Retinol ist im Rahmen der Transkription ebenfalls an der Genregulation beteiligt (siehe oben bei Vitamin‑A‑Gruppe). Damit erhöht sich die Bedeutung von Zink für die Transkription.
- Funktionale Prozesse von Nerven- und Gliazellen:
Zink wirkt verstärkend auf den inhibitorischen Neurotransmitter Glycin, der Nervenreize gezielt hemmt.
2.3.6 Essentielle Aminosäuren
20 proteinogene Aminosäuren sind die Grundlage für die Herstellung körpereigener Peptide. Acht davon werden ausschließlich über die Nahrung aufgenommen und können vom Körper nicht synthetisiert werden, und daher bezeichnet man sie als essentielle Aminosäuren. Die restlichen 12 Aminosäuren werden in der Regel im Körper in ausreichender Menge produziert, sie sind dem zufolge nicht-essentiell.
Alle proteinogenen Aminosäuren sind unentbehrlich für den Organismus. Einige davon haben bei der Synthese von Botenstoffen, in Gliazellen, für die Membranen der Hirnzellen oder für den Energiestoffwechsel eine etwas höhere Bedeutung, die in den folgenden Abschnitten beschrieben wird. Die Darstellungen beschränken sich sehr knapp auf die wichtigsten Zusammenhänge.
BCAAs (Verzweigtkettige Aminosäuren): Isoleucin, Leucin und Valin
Die Abkürzung BCAA ist die englische Bezeichnung für „Branched‑chain amino acid“. Zu den BCAAs gehören die drei essentiellen Aminosäuren Isoleucin, Leucin und Valin.
BCAAs werden insbesondere bei der Herstellung der Transmitter Acetylcholin, Adrenalin, Dopamin, Glutamat, Glutamin, Histamin, Noradrenalin und Serotonin benötigt.
Manche Neurotransmitter sind wiederum Vorstufen anderer Neurotransmitter. So ist beispielsweise Glutamat die Vorstufe der Gamma-Aminobuttersäure (GABA) und damit sind die BCAAs letztlich auch für die GABA-Synthese wichtig. Das Gleiche gilt für Melatonin, denn hier ist Serotonin die Vorstufe.
Isoleucin ist darüber an der Sauerstoffversorgung beteiligt, denn zur Bildung des roten Blutfarbstoffs Hämoglobin ist es unverzichtbar. Weiter sorgt Isoleucin für die Aufrechterhaltung der Mechanismen der Blutzuckerstabilisierung. Die ausreichende Versorgung mit Sauerstoff und Glukose ist für das Nervensystem von grundlegender Bedeutung. Leucin und Valin sind an der Steuerung der Insulin- und Somatrophin-Synthese beteiligt, Leucin darüber hinaus noch an der Steuerung des Cortisolspiegels.
Lysin
Lysin hat eine allgemeine Bedeutung, da es – wie jede der 20 Aminosäuren – für die Synthese zahlreicher Peptide benötigt wird, natürlich auch im Gehirn. Seine Aktivitätsschwerpunkte sind allerdings das Binde- und Muskelgewebe. Von einem weiteren Schwerpunkt des Lysins im zentralen Nervensystem ist nichts bekannt.
In bestimmten für Affekte zuständigen Bereiche des Gehirns gibt es 5-HT4-Rezeptoren, die bei Stress eine aktivierende Rolle spielen und an denen Lysin als Antagonist wirken kann. Das bedeutet: Lysin besetzt den Rezeptor ohne eine eigene biochemische Wirkung zu entfalten und verhindert gleichzeitig, dass eine solche entsteht.
Methionin
Methionin wird im Gehirn in S-Adenosyl-Methionin umgewandelt und dort aktiv. Was für die BCAAs Isoleucin, Leucin und Valin gilt, gilt auch für Methionin. Es hat bei der Herstellung von Acetylcholin, Adrenalin, Dopamin, Glutamat, Glutamin, Histamin, Noradrenalin und Serotonin eine besondere Bedeutung und damit auch bei der Gamma-Aminobuttersäure (GABA), für die Glutamat eine Vorstufe ist.
Ebenfalls ist Methionin bei der Synthese des Pseudo-Vitamins Phosphatidylcholin (siehe oben) maßgeblich beteiligt. Phosphatidylcholin hat eine hohe Bedeutung für die Stabilität der Nerven- und Gliazellwände.
Methionin sorgt für die Synthese der nicht-essentiellen Aminosäure Cystein. Cystein ist für das Nervensystem wichtig, da es einige Aufgaben als Radikalfänger direkt und indirekt übernimmt (siehe nachfolgende Beschreibung unten).
Phenylalanin
Die Aminosäure entfaltet im Nervensystem eine hohe Aktivität, unter anderem auch wegen ihrer Bedeutung als Vorstufe der nicht‑essentiellen Aminosäure Tyrosin (siehe Beschreibung unten).
Phenylalanin ist an der Synthese der Neurotransmitter Adrenalin, Dopamin, Levodopa, Noradrenalin, Phenethylamin und Tyramin beteiligt.
Ebenfalls hat Phenylalanin bei der Synthese des Schilddrüsenhormons Thyroxin eine Funktion. Die Steuerung des Körpergrundumsatzes, welche die Schilddrüse übernimmt, hat auf die Psyche eine große Auswirkung (→ Erläuterungen des Spurenelements Jod im Abschnitt 2.3.5).
Threonin
Threonin kann in die nicht-essentielle Aminosäure Glycin umgewandelt werden und hat nur deshalb im Nervensystem eine höhere Bedeutung (→ Beschreibung von Glycin im Abschnitt 2.3.7).
Tryptophan
Tryptophan ist die Grundlage für die Synthese des wichtigen Neurotransmitters Serotonin, zu dem es in wenigen Schritten über 5-Hydroxytryptophan umgewandelt wird. Serotonin ist für die Steuerung von Stimmungslage und Affekten von großer Bedeutung.
Bezüglich der Neurotransmitter Acetylcholin, Adrenalin, Dopamin, Glutamat, Glutamin, Histamin, Noradrenalin und der Gamma-Aminobuttersäure (GABA) gilt für Tryptophan das Gleiche wie für die BCCAs und Methionin.
Im Gehirn spielt Tryptophan auch in der Epiphyse eine große Rolle, denn das wichtige Epiphysen-Hormon Melatonin wird aus Serotonin gebildet.
2.3.7 Halb-essentielle und nicht-essentielle Aminosäuren
Der Unterschied zwischen halb- und nicht-essentiellen Aminosäuren wird wichtig, wenn der Körper in einer besonderen Situation ist, beispielsweise bei Stress, Krankheit und Rekonvaleszenz oder in der Wachstumsphase. Dann reichen die körpereigenen Mengen der Aminosäuren Alanin, Arginin und Histidin nicht immer aus, so dass sie mit der Ernährung zugeführt werden müssen. Die normalerweise nicht-essentiellen Aminosäuren werden somit essentiell. Manchmal werden die Aminosäuren Asparagin, Cystein und Tyrosin ebenfalls den halb-essentiellen Aminosäuren zugeordnet.
Alanin
Vor allem für die Regulierung des Blutzuckerspiegels ist Alanin entscheidend, da es eine Vorstufe der Glukose im Zusammenhang mit der Gluconeogenese ist (→ Abschnitte 4.8.4 ff.). Somit ist Alanin auch für den Verlauf der Blutzuckerkurve mitverantwortlich und hat damit für ein funktionierendes Nervensystem eine besondere Bedeutung.
Obwohl es bei Stress aufgrund eines erhöhten Bedarfs zu einer Alaninmangelversorgung kommen kann, wird Alanin nicht immer zu den halb-essentiellen Aminosäuren gezählt.
Arginin
Auch Arginin ist – wie Alanin – von allgemeiner Bedeutung und erfüllt seine Aufgaben vor allem im Blutkreislauf und in den Gefäßen. So sorgt die Aminosäure unter anderem als Botenstoff für eine Gefäßerweiterung. Das kommt natürlich auch den Gefäßen des Gehirns zugute und trägt unter anderem zu einer Minderung des Schlaganfallrisikos bei. Durch Gefäßveränderungen im Gehirn wird auch auf unterschiedliche Blutbedarfe reagiert, zum Beispiel wenn Hirnareale besonders aktiv sind.
Darüber hinaus ist Arginin eine Vorstufe von Stickstoffmonoxid, ein für die Nervenzellen relevanter Botenstoff und im Gehirn in hoher Menge nachweisbar. Es spielt bei der Entwicklung und Veränderung von Neuronen eine große Rolle. Lern- und Gedächtnisprozesse werden von Arginin beeinflusst. Leider fehlen noch detailliertere Informationen über diese Vorgänge.
Asparagin und Asparaginsäure
Bei den beiden Aminosäuren handelt es sich um verwandte Substanzen, so dass sie hier der Einfachheit halber gemeinsam beschrieben werden.
Der als Asparagin-Asparaginsäure-Kreislauf bezeichnete Stoffwechselzyklus bedeutet, dass beide Substanzen ineinander umwandelbar sind. Aspargin entsteht im Körper aus Asparaginsäure und ATP. Umgekehrt kann aus Asparaginsäure wieder Asparagin werden, wobei das schädliche Ammoniak entsteht.
Asparagin ist ein Ausgangsstoff verschiedener Neurotransmitter und Bestandteile vieler Proteine, die im zentralen Nervensystem eine Rolle spielen. Die Asparaginsäure (= L-Aspartat) übernimmt dagegen direkt die Funktionen eines Neurotransmitter und wirkt, ähnlich wie die Glutaminsäure, stimulierend. Asparaginsäure bindet an die NMDA-Rezeptoren des Gehirns.
Für die Synthese der DNA und RNA ist die Asparaginsäure grundlegend.
Cystein
Es gilt: Kein Protein ohne Cystein, so dass die Aminosäure von großer allgemeiner Bedeutung ist.
Cystein hat eine wichtige Funktion für den Zellschutz, da es – zusammen mit Glycin und Glutamin – an der Synthese des Antioxidans Glutathion beteiligt ist.
Aus Cystein (zusammen mit Methionin und Vitamin B6) wird Taurin gebildet. Taurin hat im Nervensystem vor allem schützende Funktionen, da es ebenfalls antioxidativ wirkt und sowohl die Membranen der Nerven- und Gliazellen stabilisiert als auch die im Gehirn wichtigen essentiellen Fettsäuren vor Oxidation schützt.
Glutamin und Glutaminsäure
Auch bei diesen beiden Aminosäuren handelt es sich um verwandte Substanzen, so dass sie hier der Einfachheit halber gemeinsam beschrieben werden. Sie haben einen gegensätzlichen Charakter und sind im Gehirn von entscheidender Bedeutung.
Glutamin wird in der Regel aus der in der Nahrung häufiger vorkommenden Glutaminsäure synthetisiert. Glutamin ist die Vorstufe der Neurotransmitter Glutamat und Gamma‑Aminobuttersäure (GABA). GABA ist der wichtigste inhibitorische Neurotransmitter, wirkt also beruhigend.
Die im Nervensystem direkt synthetisierte Glutaminsäure, also der Teil, der nicht über die Nahrung aufgenommen wird, ist der wichtigste erregende Neurotransmitter. Glutaminsäure und GABA sind damit Gegenspieler.
Darüber hinaus ist die Eigenschaft des Glutamins als allgemeiner Energielieferant für das zentrale Nervensystem ebenfalls sehr wichtig.
Glycin
Für den Energiehaushalt einer Zelle ist Glycin doppelt wichtig. Es ist sowohl für den Zuckerstoffwechsel, das heißt für die Energieproduktion unverzichtbar, als auch Teil des roten Blutfarbstoff Hämoglobin, das für die Sauerstoffversorgung wichtigste Protein.
Darüber hinaus ist Glycin ein inhibitorischer Neurotransmitter im Gehirn und hat daher eine beruhigende Funktion.
Histidin
Histidin ist für die Synthese des roten Blutfarbstoffs Hämoglobin entscheidend und damit auch für die Sauerstoffversorgung der Hirnzellen.
Bei der Synthese der Myelinzellen, den nervenzellenumhüllenden Gliazellen, ist Histidin beteiligt und das ist auch die entscheidende Aufgabe des Histidins im Gehirn.
Viele weitere Erkenntnisse über besondere Funktionen des Histidins im Stoffwechsel des Zentralnervensystems gibt es bisher nicht. Einige Quellen verweisen auf Studien, die über bestimmte Zusammenhänge zwischen Histidin und Verhaltensstörungen berichten, aber leider sind deren Ergebnisse relativ spärlich dokumentiert, so dass darüber nicht weiter spekuliert werden soll.
Prolin
Über die Aminosäure Prolin und ihre Beziehungen zum Nervensystem liegt so gut wie nichts vor. Sie hat natürlich eine wichtige allgemeine Bedeutung, wie alle Aminosäuren.
Einige Funktionen hat Prolin im Bewegungsapparat, da es dort in allen Gewebearten reichlich vorkommt, nämlich im Bindegewebe, in Knochen und Knorpel und in den Kollagenfasern.
Serin
Einige der Prozesse mit allgemeiner Bedeutung, an denen besonders Serin beteiligt ist, sind auch im Nervensystem entscheidend. Dazu zählen der Kohlenhydratstoffwechsel und der Stoffaustausch durch die Zellmembranen, Letzteres aufgrund der Beteiligung von Serin an der Phosphatlipidsynthese. Die Membranen der Nervenzellen sind vor allem auf Phosphatidylserin angewiesen, das auf Grundlage von Serin hergestellt wird. (→ Abschnitt 2.4.2).
Serin und Glycin können jeweils ineinander umgewandelt werden, wodurch sich die Bedeutung des Serins für die Energieversorgung erklärt.
Cholin ist eine Vorstufe des für Nerven- und Gliazellen wichtigen Phosphatidylcholins. Cholin benötigt Serin zu seiner Synthese. Phosphatidylcholin ist ein weiterer wichtiger Bestandteil von Zellmembranen (→ Abschnitte 2.3.2 und 2.4.2).
Cholin ist aber auch die Vorstufe des Botenstoffs Acetylcholin, der hier schon öfter erwähnt wurde. Acetylcholin ist vor allem ein erregender Botenstoff, kann aber auch hemmend agieren. Dieser Zusammenhang steigert die Bedeutung des Serins für das Nervensystem erheblich.
D-Serin ist ein weiterer Botenstoff, der mit Serin in Zusammenhang steht. D-Serin wird als Botenstoff von bestimmten Gliazellen, den Astrozyten, aber auch in Nervenzellen ausgeschüttet und beeinflusst den Informationsaustausch zwischen den Nervenzellen. D-Serin wird mittels des Enzyms Serin-Razemase aus Serin hergestellt. D-Serin bindet an NMDA-Rezeptoren und verstärkt dadurch die Wirkung des Botenstoffs Glutamat.
Tyrosin
Die hohe Bedeutung der Aminosäure Tyrosin ergibt sich aufgrund nachfolgender Beschreibung. Die Leber wandelt Phenylalanin in Tyrosin um.
Tyrosin ist eine Vorstufe der Neurotransmitter Adrenalin, Dopamin, L-Dopa und Noradrenalin. Ebenfalls ist es an der Synthese der für das Gehirn wichtigen Schilddrüsenhormone T3 und T4 beteiligt.
Fast alle signalübertragenden Proteine benötigen zur Herstellung diese Aminosäure. Tyrosin wirkt gleichfalls als erregender Botenstoff.
2.4 Nahrungsfette und Fettbegleitstoffe ▲
Im Abschnitt 2.3.2 wurden Docosahexaensäure (DHA), Eicosapentaensäure (EPA) und die beiden wichtigsten Phospholipide Phosphatidylcholin und Phosphatidylinositol schon beschrieben, die aufgrund ihrer Eigenschaften zwar zu den Fetten bzw. Fettbegleitstoffen gehören, jedoch in den meisten Darstellungen den Mikronährstoffen als vitaminähnliche Substanzen zugeordnet werden. So erhielten EPA und DHA früher sogar einmal die Bezeichung Vitamin F und die beiden Phospholipide wurden längere Zeit zu den B‑Vitaminen gezählt. Die vier fettlöslichen Vitamine A, D, E und K, auch schon in Abschnitt 2.3.1 erörtert, sind strenggenommen ebenfalls Fettbegleitstoffe.
Die Darstellung der Systematik der Fette ist häufig verwirrend, denn das Wort „Fett“ wird fälschlicherweise meist stellvertretend für sämtliche Fettarten und fettähnliche Substanzen verwendet. Eine differenzierte Betrachtung der verschiedenen Substanzen und Stoffwechselvorgänge kann hier für mehr Klarheit sorgen.
Fett ist meist eine Sammelbezeichung für Glyceride, Fettsäuren, fettähnliche Stoffe (Lipoïde) und Cholesterin, was wissenschaftlich nicht korrekt ist. Der exakte Obergegriff für alle ist Lipide.
Hier sollen die beiden Gruppen der Nahrungsfette (bzw. vereinfachend Fette) und der Fettbegleitstoffe unterschieden werden. Wie immer wird auf die Erklärung von Details verzichtet, die hier nicht von Interesse sind. Die Erörterung ihrer Rollen im Stoffwechsel erfolgt immer im Zusammenhang mit dem Zentralnervensystem.
2.4.1 Nahrungsfett/Fett
Das Nahrungsfett besteht hauptsächlich aus Glyceriden. Glyceride sind Verbindungen von Glycerin mit Fettsäuren. Die Fettsäuren machen dabei den eigentlichen Fettanteil des Moleküls aus, Glycerin gehört dagegen zur Gruppe der Alkohole.
Ebenso sind auch ungebundene bzw. freie Fettsäuren in geringer Zahl Bestandteile des Nahrungsfetts.
Darüber hinaus können bestimmte Fettsäurearten aus anderen Fettsäuren synthetisiert werden, diese zählen hier der Einfachheit halber aber auch zu den Nahrungsfetten, denn alle Fettsäuren haben letztlich ihren Ursprung in der Nahrung.
Man unterscheidet Mono-, Di- und Triglyceride, je nachdem, ob sich eine, zwei oder drei Fettsäuren mit einem Glycerin-Molekül verbinden. Glyceride werden auch als einfache Fette oder Neutralfette bezeichnet.
Triglyceride - korrekte Bezeichnung: Triacylglycerine - machen mit ca. 90% den größten Teil des Nahrungsfetts aus. Die beiden anderen Glyceride sind nur in geringer Menge in der Nahrung enthalten.
Es gibt verschiedene Fettsäuren-Klassifizierungen, für die hier zu erörternden Themen ist zu unterscheiden zwischen...
- gesättigten Fettsäuren,
- einfach ungesättigten Fettsäuren und
- mehrfach ungesättigten Fettsäuren.
Die Bezeichnungen ergeben sich aus ihren unterschiedlichen chemischen Strukturen, was hier nicht von Bedeutung ist. Die drei Gruppen verbinden jedoch auch gemeinsame Eigenschaften und Funktionen miteinander.
Gesättigte und einfach ungesättigte Fettsäuren kann der Körper selbst produzieren, während mehrfach ungesättigte Fettsäuren mit der Nahrung zugeführt werden müssen, da er sie entweder nur teilweise oder gar nicht synthetisiert. Sie werden aus diesem Grund auch bedingt essentielle Fettsäuren oder essentielle Fettsäuren genannt. Die Bezeichung „bedingt essentiell“ wird aber eher selten verwendet.
Sämtliche Fettsäuren können der Deckung des Energiebedarfs, der Energiespeicherung und als Baustoffe der Zellmembranen dienen, viele ein- oder mehrfach ungesättigte Fettsäuren haben darüber hinaus noch wichtige physiologische Funktionen. So dienen Fette der Herstellung wichtiger Hormone und ermöglichen es der Zelle, fettlösliche Vitamine aufzunehmen.
Wichtig ist, dass die Energieversorgung durch Fette in Nervenzellen keine Rolle spielt, denn dort wird Energie ausschließlich durch den Abbau von Glukose gewonnen. Eine einzige Ausnahme ist die Notversorgung des Gehirns durch Ketonkörper bei einem niedrigen Glukosespiegel, zum Beispiel im Rahmen einer Hungerkur oder kohlenhydratfreien bzw. ‑armen Ernährung. Ketonkörper werden durch den Abbau von Fettsäuren synthetisiert. Diese Form der Energieversorgung ist eine absolute Ausnahme und spielt hier keine Rolle. Hier sind daher ausschließlich die Funktionen von Fettsäuren interessant, die nicht die Energieversorgung betreffen.
Gesättigte Fettsäuren
Gesättigte Fettsäuren gelangen überwiegend durch den Konsum tierischen Fettes in den Körper. Aber auch in pflanzlichen Lebensmittel sind sie enthalten, Kokosöl besteht beispielsweise überwiegend aus den gesättigten Fetten Laurin‑, Myristin‑, Palmitin‑, Capryl‑, Caprin‑ und Stearinsäure, den Rest bilden mit nur 6 ‑ 13% die einfach ungesättigte Ölsäure und die mehrfach ungesättigte Linolsäure.
Gesättigte Fettsäuren dienen aufgrund ihres hohen Energiegehalts vor allem der Energieversorgung. Aber sie sind ebenfalls wichtige Baustoffe für die Zellmembranen, ihre zweite Funktion ist daher strukturelle Natur. Der Einbau gesättigter Fettsäuren in Membranen ist unbedingt notwendig, denn die stabilisierenden Eigenschaften gesättigter Fettsäuren sind wichtig. Bei einer zu hohen Zufuhr gesättigter Fettsäuren auf Kosten der ungesättigten gelten sie als schädlich, u. a. weil die Zellmembranen starrer werden. Es ist alles eine Frage der richtigen Mengenverhältnisse zwischen gesättigten und ungesättigten Fettsäuren.
Ein zu hoher Konsum gesättigter Fettsäuren soll bestimmte, negativ assoziierte Blutfettwerte erhöhen, die für Herz- und Kreislaufkrankungen mitverantwortlich gemacht werden. So sollen sie zu Gefäßschädigungen führen, was auch die Arterien, Venen und Kapillaren des Gehirns belasten würde. Diese These wird unter Fachleuten jedoch kontrovers diskutiert, da ein Beweis des unterstellten kausalen Zusammenhangs noch nicht erbracht ist.
Gesättigte Fettsäuren sind nicht in der Lage, mit anderen Substanzen zu interagieren und können dadurch nach dem derzeitigen Stand des Wissens eigentlich keine weiteren biologisch-physiologischen Funktionen ausführen.
Es mehren sich aber die Hinweise, dass auch sie derartige Aufgaben erfüllen, beispielsweise für die Genexpression, bei der Verhinderung der Entstehung maligner Zellen oder bei der Hormonsynthese (Quellen: O. Hirschfeld-Kroll 2005, Medizinische Fakultät der Eberhard-Karls-Universität, Tübingen; European Food Information Council, www.eufic.org). Bei folgenden für den Menschen wichtigen gesättigten Fettsäuren werden biologische Funktionen diskutiert, jedoch ist der Kenntnisstand darüber noch sehr lückenhaft:
- Buttersäure - Regulation der Proteinbiosynthese, Abwehr maligner Krebszellen
- Laurinsäure - Beteiligung an der Synthese von mehrfach ungesättigten Fettsäuren
- Myristinsäure - Funktionen bei der Zellkommunikation, Immunfunktion, Regulation der Verfügbarkeit von mehrfach ungesättigten Fettsäuren
- Palmitinsäure - Regulation der Hormonsynthese, Funktionen bei der Zellkommunikation, Immunfunktion
Einfach ungesättigte Fettsäuren
Neben ihrer Energieversorgungsfunktion übernehmen einfach ungesättige Fettsäuren ebenfalls eine besondere Rolle beim Aufbau von Zellmembranen, welche gesättigte Fettsäuren nicht leisten können. Membranen werden von ihnen flexibel und beweglich gehalten, wovon die Membranstruktur und -funktion insgesamt sowie die in die Zellwände eingebauten Proteine profitieren, da sie nur so in der Lage sind, ihre Funktionen optimal zu erfüllen, beispielsweise als Rezeptoren: Das Ein- und Ausschleusen von Stoffen oder deren Blockade wird durch flexible Membranen erleichtert.
Darüber hinaus haben einfach ungesättigte Fettsäuren ‑ im Gegensatz zu den gesättigten ‑ auf „schlechte“ Blutfette einen positiven Einfluss, da sie für eine Stabilisierung der Werte oder diese sogar vermindern.
Die für den Menschen wichtigste Verterterin ist die Ölsäure, die in einigen Pflanzenölen (Rapsöl, Olivenöl) einen besonders hohen Anteil hat. Daneben spielen noch die Gadoleinsäure und die Nervonsäure eine große Rolle.
Das Interesse an der nicht essentiellen Nervonsäure ist seit einiger Zeit gestiegen. Sie soll über die energetischen und strukturellen Grundfunktionen hinaus ‑ Nomen est Omen ‑ besondere biologische Funktionen beim Aufbau und der Tätigkeit des Zentralnervensystems haben:
- Überproportionale Nutzung der Nervonsäure als Baustein der Nervenzellmembranen
- Beteiligung an der Myelinsynthese
- Modulierung der Nervenreizübertragung
- Beteiligung am Wachstum von Nervenzellen
- Beteiligung an den Verschaltungsvorgängen von Nervenzellen
- Verhinderung von Mechanismen, die zur Neurodegeneration beitragen
Bei Patienten mit Multipler Sklerose und dem Addison-Schilder-Syndrom wurde festgestellt, dass Nervonsäure in den Myelinzellen fehlt. Hier ist noch einiges an Forschungsarbeit notwendig, um die tatsächliche Bedeutung der Nervonsäure besser beurteilen zu können.
Mehrfach ungesättigte Fettsäuren
Die bedingt oder absolut essentiellen mehrfach ungesättigten Fettsäuren erfüllen neben der Energieversorgung ebenfalls eine strukturelle Aufgabe als Bausteine für Zellmembranen. Hier sorgen einige von ihnen gemeinsam mit den einfach ungesättigten Fettsäuren für eine ausreichende Membranflexibilität.
Eine weitere allgemeine Eigenschaft von ihnen ist die Senkung der „schlechten“ LDL‑ und die parallele Steigerung der „guten“ HDL‑Blutfette. Damit sind sie sogar den einfach ungesättigten Fettsäuren überlegen.
Mehrfach ungesättigte Fettsäuren sind größtenteils pflanzlichen Ursprungs. Auch die in Fischen vorkommenden n‑3‑Fettsäuren DHA und EPA entstammen Algen. Algen sind Teil der Nahrung von Fischen und Krebsen, wodurch deren Fressfeinde, beispielsweise Wildlachse, DHA und EPA ebenfalls anreichern.
Diese Fettsäuren übernehmen aufgrund ihrer Fähigkeit, Verbindungen mit anderen Substanzen einzugehen, noch eine Vielzahl weiterer biologischer Funktionen, die relativ gut erforscht sind:
- Alpha-Linolensäure (ALA, gehört zu den n-3-Fettsäuren)
Ein geringer Teil der essentiellen dreifach ungesättigten Alpha-Linolensäure synthetisiert DHA und EPA. Daher treffen die bei EPA und DHA erwähnten positiven Einflüsse auf das Zentralnervensystem indirekt auch auf die Alpha‑Linolensäure zu. Eine wichtige Synthese-Voraussetzung ist die Anwesenheit des Enzyms Delta‑6‑Desaturase.
Bei der Bewertung der ALA ist zu berücksichtigen, dass DHA und EPA auch über die Nahrung in den Körper gelangen sollten, da man sich nicht alleine auf deren Synthese durch die ALA verlassen kann.
Eine weitere Eigenschaft der ALA ist ihre Unterdrückung der Synthese der Arachidon‑Fettsäure. Dies wäre positiv, denn die Arachidonsäure, deren Beschreibung weiter unten noch folgt, steht im Verdacht negativer, entzündungsverstärkender Wirkungen.
- Docosahexaensäure/DHA und Eicosapentaensäure/EPA
(→ Abschnitt 2.3.3)
- Linolsäure (gehört zu den n-6-Fettsäuren)
Die essentielle Linolsäure ist zweifach ungesättigt und dient als Vorstufe der Synthese anderer mehrfach ungesättigter Fettsäuren aus der n‑6‑Gruppe, dazu gehören Gamma‑Linolensäure, Dihomogamma‑Linolensäure und die Arachidonsäure. Somit ist sie indirekt auch mit deren Eigenschaften in Verbindung zu bringen.
Auch Linolsäure benötigt zu dieser Synthese die Delta-6-Desaturase, so dass ein Mangel daran ihren physiologischen Wert mindert.
- Gamma-Linolensäure
(GLA, gehört zu den n-6-Fettsäuren)
Die Gamma-Linolensäure wird im Körper durch die Umwandlung der Linolsäure synthetisiert. Auch durch die Nahrung kann sie in den Körper gelangen, ist jedoch nur in wenigen pflanzlichen Ölen enthalten, die bekanntesten sind das Nachtkerzenöl und das Borretschöl.
Die GLA ist die Grundsubstanz der Dihomogamma-Linolensäure (DGLA).
Diese Fettsäure ist essentiell für das Gehirn und die Reizverarbeitung. Sie ist in den Nervenzellmembranen auffällig hoch konzentriert und steht dort bei Bedarf zur weiteren Umwandlung in DGLA zur Verfügung.
- Dihomogamma-Linolensäure (DGLA, gehört zu den n‑6‑Fettsäuren)
Die Dihomogamma-Linolensäure wird auch als Eicosatriensäure (ETA) bezeichnet. Sie dient der Synthese von Serie-1-Eicosanoiden mit entzündungshemmenden Funktionen. Aber auch für die Arachidonsäure ist DGLA die Vorstufe.
- Arachidonsäure (AA, gehört zu den n-6-Fettsäuren)
Nur tierische Lebewesen können Arachidonsäure aus DGLA synthetisieren, was der Grund dafür ist, dass nur tierische Lipide Arachidonsäure enthalten. Sie ist die einzige Fettsäure der n‑6‑Gruppe, auf die diese Eigenschaft zutrifft.
Die Arachidonsäure wird in Serie-2-Eicosanoide umgewandelt, die mit vielen unterschiedlichen Funktionen verbunden sind, was ihre Bewertung erschwert. Einerseits werden ihr entzündungsfördernde Eigenschaften nachgesagt, aber es gibt ebenfalls Hinweise auf entzündungshemmende Funktionen. Auch ist zu berücksichtigen, dass Entzündungsprozesse im Körper notwendig sind, denn sie dienen der Heilung von Verletzungen und sind nicht per se negativ. Von daher gesehen wäre auch die entzündungsfördernde Eigenschaft der Arachidonsäure positiv zu bewerten.
Zur Gruppe der Serie-2-Eicosanoide gehören Endocannabinoide, die im Nervensystem eine Rolle spielen, wissenschaftlich aber noch relativ wenig erforscht sind.
In der Pädiatrie wurden bei ADHS-Patienten geringe Arachidonsäurekonzentrationen festgestellt. Das stimmt mit der Erkenntnis überein, dass Arachidonsäure das Verhalten beeinflusst.
Aufgrund der drei genannten Charakteristika - essentiell, wichtig für biologische Funktionen und günstiger Einfluss auf die Blutfette - gelten die mehrfach ungesättigten Fettsäuren als die wichtigsten und qualitativ hochwertigsten Nahrungsfette.
2.4.2 Fettbegleitstoffe
Unter Fettbegleitstoffen werden fettähnliche und einige weitere Substanzen verstanden, die wie Fette in Wasser unlöslich sind und meist zusammen mit dem Nahrungsfett aufgenommen werden.
Fettähnliche Fettbegleitstoffe, auch Lipoïde genannt, enthalten Fettsäuren. Auf die anderen Begleitstoffe trifft das nicht zu, zu ihnen zählen Sterine und fettlösliche Vitamine.
Folgende Fettbegleitstoffe spielen im Zusammenhang mit dem Nervensystem eine besondere Rolle:
- Fettähnliche Stoffe (Lipoïde), insbesondere Phospholipide
- Phosphatidylcholin
- Phosphatidylinositol
- Phosphatidylserin
- Sterine
- Cholesterin
- Fettlösliche Vitamine
- Vitamin-A-Gruppe, insbesondere Retinol
- Vitamin-D-Gruppe, insbesondere Calciol
- Tocopherole, Tocotrienole (Vitamin-E-Gruppe)
- Vitamin-K-Gruppe
- Carotinoide, zum Beispiel beta-Carotin oder Lykopin
Die beiden wichtigsten Vertreter der Phospholipide, Phosphatidylcholin und ‑inositol, und die fettlöslichen Vitamine wurden als Mikronährstoffe schon erörtert (→ Abschnitt 2.3.2), so dass nun nur noch Phosphatidylserin und Cholesterin vorgestellt werden.
Phosphatidylserin
Phosphatidylserin ist ‑ wie die anderen beiden Phospholipide ‑ ein wichtiger Teil von Zellmembranen und dort auf den dem Zytoplasma zugewandten Membraninnenseiten lokalisiert.
Die Hauptaufgabe ist die Aufrechterhaltung der Membranflexibilität. Dabei hat Phosphatidylserin eine besondere Affinität zu den Membranproteinen und sorgt dafür, dass diese optimal in die Membranstruktur integriert werden und ihre Funktionen noch besser erfüllen. Phosphatidylserin-Moleküle befinden sich nämlich auffällig verstärkt in räumlicher Nähe zu ihnen.
Membanproteine sind u. a. für alle Schaltfunktionen der Zelle verantwortlich. Das betrifft die gesamte Reizverarbeitung der Nervenzellen: die Reizübertragung an den Synapsen und die Reizweiterleitung an den Axonen mit deren Myelinscheiden. Es wird vermutet, dass Phosphatidylserin nicht nur passiv, sondern auch aktiv in Zelloberflächenprozesse involviert ist.
Studien deuten darauf hin, dass Phosphatidylserin auch als Antioxdans Nervenzellen vor Toxinen schützt. Das könnte direkt erfolgen aber auch eine indirekte Folge ihrer Membranfunktionsverbesserung sein, denn durch sie wehren sich die Membranen besser gegen schädliche Eindringlinge (Quelle: Geiss, Hamm, Waag, Zirkelbach 1999, Wissenschaftliches Dossier zu Phosphatidylserin, ISME GmbH, Mörfelden-Walldorf).
Cholesterin
Der Körper eines Erwachsenen enthält im Durchschnitt 150 Gramm Cholesterin. Damit kommt es häufiger vor als wichtige Mineralstoffe. Zum Vergleich: Kalium steht dort mit etwa 125 Gramm an vierter Stelle. Ein Gehirn besteht zu ca. 18% aus Cholesterin, was dessen Bedeutung unterstreicht.
Cholesterin ist ein polyzyklischer Alkohol und kommt ausschließlich in tierischen Lebensmitteln vor. Pflanzen enthalten kein Cholesterin, jedoch haben sie eine vergleichbare Substanz, das Phytosterin. Phytosterin ist für Menschen so gut wie bedeutungslos. Auch sind die in den Pflanzen enthaltenen Phytosterinmengen - im Vergleich mit Cholesterin - sehr gering.
Der Körper bildet Cholesterin jedoch hauptsächlich in der Leber selber und verfügt über einen effektiven Regelmechanismus. Wird Cholesterin über die Nahrung aufgenommen, kompensiert er das zu einem großen Teil durch Drosselung der Eigenproduktion. Bezüglich des Anteils selbstproduzierten Cholesterins gibt es jedoch verschiedene Meinungen. In der Literatur findet man häufig den Hinweis, dass der Körper ca. 70% des Cholesterinbedarfs selbst produziert. Verschiedene Untersuchungen deuten im Gegensatz dazu darauf hin, dass der Cholesteringehalt des Blutes zu 98% durch körpereigene Mechanismen gesteuert wird und nur 2% nahrungsabhängig ist. Über dieses Thema wird unter Fachleuten heftig gestritten, denn eine überwiegende endogene Regelung des Cholesterinspiegels bedeutet, dass die Menge des aufgenommenen Nahrungscholesterins keine größeren Auswirkungen hätte. Je geringer der Anteil des Regelungsmechanismus jedoch ist, desto wichtiger wäre die Aufnahme von genügend Nahrungscholesterin, das damit quasi einen semi-essentiellen Status bekäme.
Es wird dennoch empfohlen, die täglich mit der Nahrung aufgenommene Menge an Cholesterin auf ca. 300 mg zu begrenzen. Ein hoher Colesterinspiegel im Blut wird mit Erkrankungen des Herz-Kreislauf-Systems in Zusammenhang gebracht, denn es soll sich in den für Gefäßverengungen verantwortlichen Plaques ansammeln, was zu verschiedenen Erkrankungen führen kann. Durchblutungsstörungen des Gehirns bzw. TIA und die Gefahr eines Apoplex oder weitere neurologische Störungen wären dann die für das Zentralnervensystem möglichen Folgen.
Der Kausalzusammenhang zwischen hohen Cholesterinwerten und Herz-Kreislauf-Erkrankungen ist jedoch bis heute nicht belegt. Dementsprechend kontrovers werden die Diskussionen unter Medizinern geführt. Darin eingeschlossen ist auch die Diskussion um Notwendigkeit und Nebenwirkungen der Einnahme cholesterinsenkender Medikamente.
Über die Nützlichkeit oder Gefahr des Cholesterins scheint man sich also generell uneins zu sein. Wesentlich klarer belegt sind hingegen die Aufgaben des Cholesterins und seine Unverzichtbarkeit im menschlichen Körper. Cholesterin wird benötigt als...
- Bestandteil aller Zellmembranen,
- Vorstufe der Geschlechtshormone DHEA, Östrogen, Progesteron und Testosteron,
- Vorstufe der Nebennierenhormone Aldosteron und Cortisol und als
- Faktor bei der Synthese von Vitamin D.
Cholesterin sorgt für eine gute Zellmembranstabilität bzw. ‑steifheit und ist mitverantwortlich dafür, dass die Zelle das Ein- und Ausschleusen von Substanzen optimal durchführen kann. Cholesterin arbeitet hier mit den membranrelevanten Fettsäuren bzw. Fettbegleitstoffen eng zusammen.
Fehlversorgungen mit Cholesterin werden als Hyper- bzw. Hypocholesterinämie bezeichnet.
Die primäre oder sekundäre Hypercholesterinämie, eine durch überhöhte Blutcholesterinwerte gekennzeichnete Lipidstoffwechselstörung, ist heute hinsichtlich Diagnose und Folgen umstritten, wie die oben beschriebenen Kontroversen schon vermuten lassen.
Die üblichen Grenzwerte für das Gesamtcholesterin liegen bei gesunden Erwachsenen bei 200 bis 230 mg/dl für das Gesamtcholesterin, während der Wert des „schlechten“ LDL-Cholesterins nicht über 160 mg/dl steigen sollte. Das „gute“ HDL soll bei Männern bzw. Frauen nicht unter 40 bzw. 50 mg/dl sinken. Jenseits dieser Mengen für das LDL- bzw. Gesamtcholesterin wird die Erkrankung diagnostiziert. Für Risikopatienten gelten allerdings niedrigere Werte. Es gibt viele Wissenschaftler, die diese Einteilung als willkürlich und nicht zutreffend betrachten und wesentlich höhere Cholesterinwerte als unbedenklich betrachten.
Bei 70% der Personen mit entsprechenden Werteabweichungen liegen Ernährungsfehler oder bestimmte Erkrankungen vor, beispielsweise Diabetes mellitus oder Adipositas, was aber nicht automatisch auf einen Kausalzusammenhang hinweist. Das Metabolische Syndrom, eine Sammelbezeichnung für eine häufig vorkommende Kombination bestimmter Erkrankungen, beinhaltet auch die Hypercholesterinämie, insbesondere ein ungünstiges Verhältnis der „guten“ HDL-Blufette zu den „schlechten“ LDL-Blutfetten. In diesen Fällen liegt eine sekundäre Hypercholesterinämie vor.
Eine primäre Hypercholesterinämie aufgrund eines ererbten Gendefekts oder anderer endogener Faktoren wird bei ca. 30% der Personen mit Wertabweichungen diagnostiziert.
Eine Hypocholesterinämie mit zu niedrigen Werten liegt demnach vor bei einem HDL-Blutwert von unter 40 (gesunde Männer) bzw. 50 mg/dl (gesunde Frauen). Bezüglich des LDL-Blutwertes sind die Angaben nicht so eindeutig, manchmal findet man 130 mg/dl als Untergrenze.
2.5 Integration der vier Zellprozessbereiche ▲
Die Beschreibung einzelner Zellvorgänge, Zellbestandteile oder sonstiger Substanzen ergibt noch kein Gesamtmodell. Das wird jedoch benötigt, um Ursache-Wirkungs-Zusammenhänge zu identifizieren. Ein geeignetes Zellmodell wird nun Schritt für Schritt erarbeitet.
Von den vier grundlegenden Prozessgruppen Kern-/Zellteilung, Proteinbiosynthese, Energieversorgung und Funktionalprozesse (→ Abschnitt 2.1) soll mit den für die Darstellung relativ unkomplizierten Bereichen begonnen werden: der Gruppe der zahlreichen funktionalen Prozesse und der Gruppe der Energieversorgungsprozesse. Funktionalprozesse sind für die zelltypischen Funktionen verantwortlich, Energieversorgungsprozesse stellen die nötige Energie bereit, damit alle Zellvorgänge überhaupt geschehen können (→ Abbildung 6 oben).
Voraussetzung ist das Vorhandensein bestimmter Peptide, beispielsweise Enzyme und Proteine, die durch die beiden Proteinbiosyntheseteilprozesse Transkription und Translation entstehen. Sie haben in der Darstellung daher ihren Platz überhalb der Peptide für die Energieversorgung und der Peptide für funktionale Prozesse (→ Abbildung 8 unten). Die Proteinbiosynthese stellt damit als wichtige Komponente aller nachfolgender Vorgänge den Hauptprozess einer Zelle dar.
Auf diese Weise entstehen zwei Prozessebenen: eine obere Prozessebene mit den beiden Teilen des Hauptprozesses ‑ Transkription und Translation ‑ als Enstehungsort sämtlicher Peptide und eine untere Prozessebene, die durch Peptide und die mit ihnen verbundenen Folgeprozessen charakterisiert ist.
ABBILDUNG 8: TRANSKRIPTION, TRANSLATION, PEPTIDE FÜR FUNKTIONAL- UND ENERGIEPROZESSE
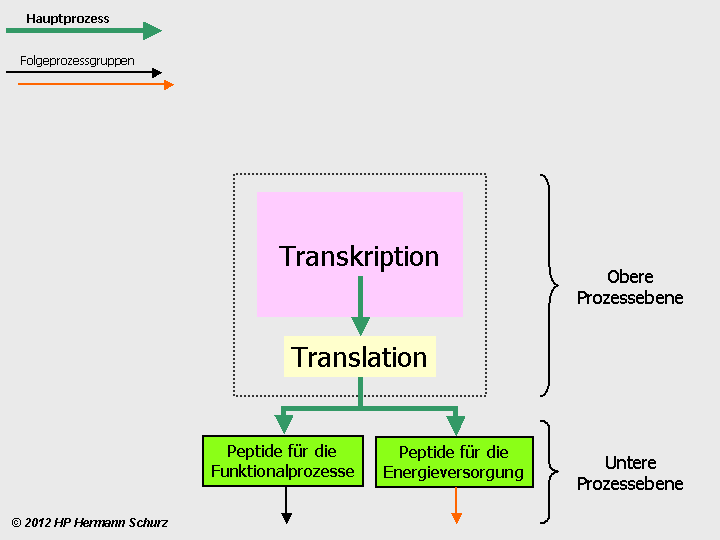
Abbildung 8: Die Proteinbiosynthese, bestehend aus Transkription und Translation, ist ein Prozess, der die Synthese der zahlreichen Peptide, beispielsweise Enzyme und Proteine, für die Funktionalprozesse und Energieversorgung bewerkstelligt. Daraus resultieren zwei Prozessebenen, die mit einem durchgehenden grünen Prozesspfeil verbunden sind. Transkription und Translation bilden den Hauptrozess auf der oberen Ebene, weil sie sowohl Teil der Funktional- als auch Teil der Energieversorgungsaktivitäten sind. Die aus den Peptiden resultierenden Prozesse werden von zwei dünnen Prozesspfeilen (schwarz bzw. orange) symbolisiert.
Etwas komplizierter wird es, Kern- und Zellteilung in die Zeichnung einzufügen. Kern- und Zellteilung finden ‑ im Gegensatz zu den anderen Prozessen ‑ nur einmalig statt und haben die „Geburt“ zweier Tochterzellen zur Folge. Man kann sie auch als das Ende oder den „Tod“ der Mutterzelle betrachten. Obwohl zwischen Mutter- und Tochterzelle zu differenzieren ist, müssen sie in eine einzige Modelldarstellung integriert werden.
Da Kern- und Zellteilung durch Enzyme bzw. Proteine gesteuert werden, deren Existenz wiederum der Proteinbiosynthese zu verdanken ist, erhalten die dafür nötigen Peptide ihren Platz ebenfalls auf der unteren Prozessebene (→ Abbildung 9).
Die Proteinbiosyntheseprozesse beider Tochterzellen bedienen sich nun den neu entstandenen DNA-Vorlagen, aus denen sie die Boten‑RNA synthetisieren (Transkription). Der die Kern- und Zellteilung darstellende braune Folgeprozesspfeil auf der unteren Prozessebene der Mutterzelle endet daher im Transkriptionsprozess der Tochterzelle(n).
Nun sind Mutter- und Tochterzellen in einer einzigen Modelldarstellung integriert und auf der rechten Seite der Zeichnung wird ein erster Prozesskreislauf sichtbar, nämlich zwischen der unteren Prozessebene einer Mutterzelle und der oberen Prozessebene ihrer Tochterzelle(n).
ABBILDUNG 9: DIE BERÜCKSICHTIGUNG VON KERN- UND ZELLTEILUNG
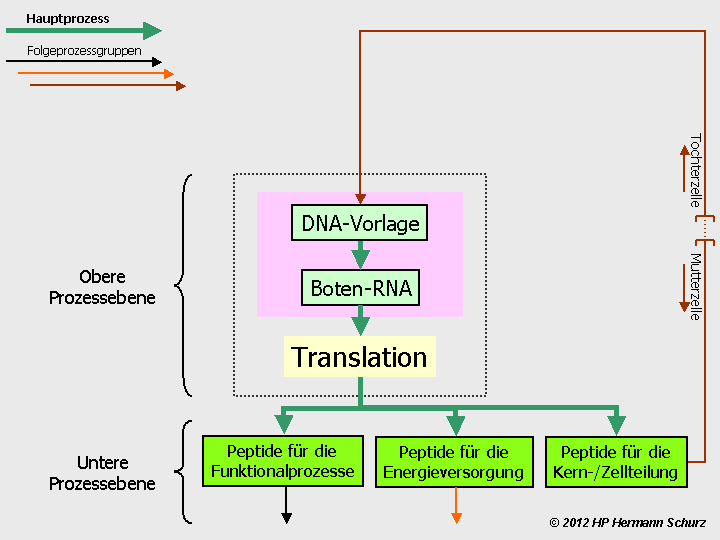
Abbildung 9: Auch die Enzyme und Proteine für die Kern- und Zellteilungsaktivitäten gehören zur unteren Prozessebene, denn sie resultieren ebenfalls aus der vorangehenden Proteinbiosynthese. Daran ändert auch nichts der Umstand, dass ihre Arbeit die Voraussetzung dafür ist, dass Tochterzellen überhaupt entstehen und auf diese Weise ihre wichtigen DNA-Vorlagen für die Transkription bekommen. Zwischen beiden Ebenen entsteht im Modell ein erster Prozesskreislauf.
Im Modell ist die DNA auf ihre Rolle als Lieferant des „Datenmaterials“ für die Transkription beschränkt. Sie hat damit den Charakter eines codierten Zwischenprodukts der Proteinsynthese und wird - wie alle codierten Zwischenprodukte - in einem umrahmten hellgrünen Kasten dargestellt, während Enzyme und Proteine als Endprodukte der Proteinbiosynthese in einem grünen Kasten erscheinen.
Abbildung 9 beinhaltet schon alle vier Prozessgruppen, aber die Darstellung der Proteinbiosynthese reicht noch nicht aus, denn sie wird ebenfalls von Peptiden gesteuert, die mittels Transkription und Translation „von ihr selber“ produziert werden, zum Beispiel Polymerasen, zahlreiche Transkriptionsfaktoren oder Ribosomen. Auf diesen Zusammenhang wurde schon in Animation 8 hingewiesen. Die Proteinbiosynthese produziert also ihre eigenen Werkzeuge. Wo sollen sich diese Werkzeuge in der Darstellung befinden?
Die Peptide zur Durchführung der Proteinbiosynthese müssen natürlich auch Teil der unteren Prozessebene sein, sie werden durch das grüne Rechteck links unten symbolisiert.
Die Aktivitäten der Peptide sind dann aber wieder Bestandteil des Hauptprozesses der oberen Prozessebene, denn sie machen ja einen großen Teil der Proteinbiosynthese aus. Die beiden dünnen grünen Prozesspfeile verdeutlichen dies, indem sie zurück auf Transkription und Translation verweisen. So ergibt sich ein zweiter Prozesskreislauf im linken Teil der Zeichnung.
ABBILDUNG 10: DIE KORREKTE DARSTELLUNG DER PROTEINBIOSYNTHESE
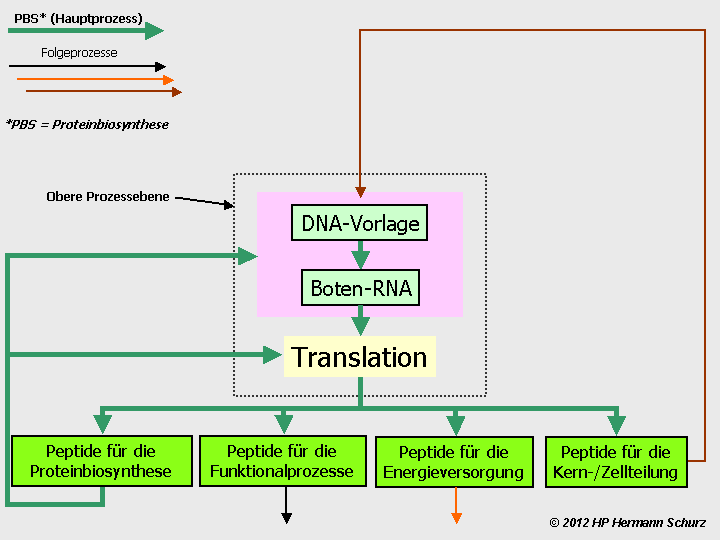
Abbildung 10: Auch die Peptide zur Durchführung der Proteinbiosynthese sind Ergebnisse von Transkription und Translation. Die Proteinbiosynthese ist damit ihr eigener Werkzeuglieferant, was durch die beiden linken grünen Prozesspfeile zum Ausdruck kommt. Ein zweiter Prozesskreislauf ist entstanden (→ Animation 8).
In Abbildung 10 fehlen noch nicht-codierende Ribonukleinsäuren (zum Beispiel micro‑RNA oder Primer‑RNA). Sie werden ebenfalls im Zellkern transkribiert, die entstandenen micro-RNA bzw. miRNA modulieren die Proteinbiosynthese, sind aber nicht Bestandteile der späteren Peptide, ihrer Zwischenprodukte und dienen auch nicht als Vorlagen zur Synthese. Primer‑RNA sind wichtig für den Start der DNA-Teilung (Replikation) als Voraussetzung für die Kernteilung.
Die ncRNA-Synthese kann im Modell daher nicht Bestandteil des Hauptprozesses sein, sie erfolgt in einem von diesem abzugrenzenden Parallelprozess und findet direkt an der DNA-Vorlage statt. Daher ist auch sie Teil der oberen Zellprozessebene.
Die proteinsynthesemodulierenden Aktivitäten der ncRNA gehören jedoch nichtsdestotrotz zum Hauptprozess der Proteinbiosynthese, Primer-Aktivitäten gehören zur Kernteilung. Die verschiedenen ncRNA ist am besten mit dem Begriff Steuerungsfaktoren beschrieben
Die in Abschnitt 2.3.5 erwähnten zirkulären Ribonukleinsäuren, die erst Anfang 2013 entdeckt wurden, müssen im Modell nicht berücksichtigt werden, da sie an den Verhältnissen nichts Grundsätzliches ändern. Man muss davon ausgehen, dass in Zukunft noch weitere ncRNA-Formen dazukommen, deren Aufgaben und Wirkungsweisen den schon bekannten Formen ähneln, so dass die Berücksichtigung einzelner Sorten in diesem hochaggregierten Modell nicht notwendig ist.
Abbildung 11 berücksichtigt die ncRNA-Synthese und deren Funktionen bei Proteinsynthese und DNA-Replikation bzw. Kernteilung. Die Farbe Rot veranschaulicht, dass der dazu notwendige Syntheseprozess vom codierenden Hauptprozess mit seinen diversen Zwischen- und Endprodukten zu unterscheiden ist.
ABBILDUNG 11: DIE INTEGRATION NICHT-CODIERENDER RIBONUKLEINSÄUREN
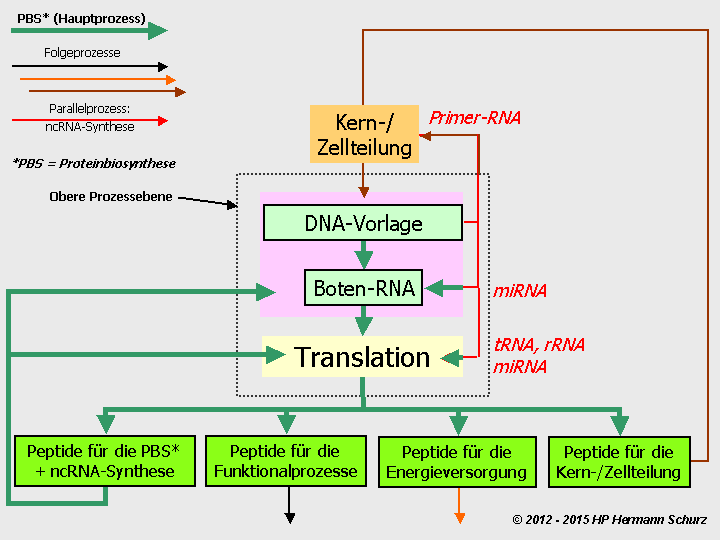
Abbildung 11: Die genregulierenden nicht-codierenden Ribonukleinsäuren, im wesentlichen miRNA, beeinflussen Transkription und Translation. Ihre Aktivitäten werden daher dem Hauptprozess zugerechnet. Ihre Synthese jedoch bildet einen eigenständigen Parallelprozess. Zu den nicht-codierenden Ribonukleinsäuren gehören auch tRNA und rRNA, die Hilfsfunktionen bei der Translation übernehmen, und die Primer-RNA zur DNA-Replikation.
Die folgende Abbildung ist eine detailliertere Darstellung mit 12 Prozessschritten. Die im Text oben beispielhaft erwähnten Enzyme und Proteine (→ Abschnitt 2.2.1 bis 2.2.7) sind diesen zugeordnet:
- PS 1 durch Aktivatoren, Helikasen, Repressor-Proteine, RITS-Proteine, RNA-Polymerase II, Histone oder Transkriptionsfaktoren.
- PS 2 durch RNA-Polymerasen I, II oder III.
- PS 3 durch TBP oder TREX.
- PS 4 durch Cleavage-Faktoren, PolyA-Polymerasen und Spleißosome.
- PS 5 durch Dicer-Enzyme oder Exportin 5
- PS 6 durch Argonautenproteine oder RISC-Proteine.
- PS 7 durch Argonautenproteine, EF-G, EF-Ts, EF-Tu, eRF1 bis eRF3, iF1 bis iF11, Peptidyltransferasen, Ribosomen oder RISC-Proteine.
- PS 8 durch Chaperone, Chaperonine (Chaperonzylinder) und Transportproteine.
- PS 9 durch Diversifizierungsenzyme, Motor- und Transportproteine (z. B. SRP oder MPP) oder Zellorganellen (z. B. Endoplasmatisches Retikulum).
- PS 10 durch DNA-Polymerasen alpha, Helikasen, Histone, Primasen und Topiosomerasen.
- PS 11 durch DNA-Polymerasen alpha, beta und delta, DNA-Ligasen, Helikasen, Histone, Primasen, RNase H, Topiosomerasen und Tus.
- PS 12 durch Membranproteine und Motorproteine.
ABBILDUNG 12: INTEGRIERTE DARSTELLUNG ALLER VIER ZELLPROZESSBEREICHE
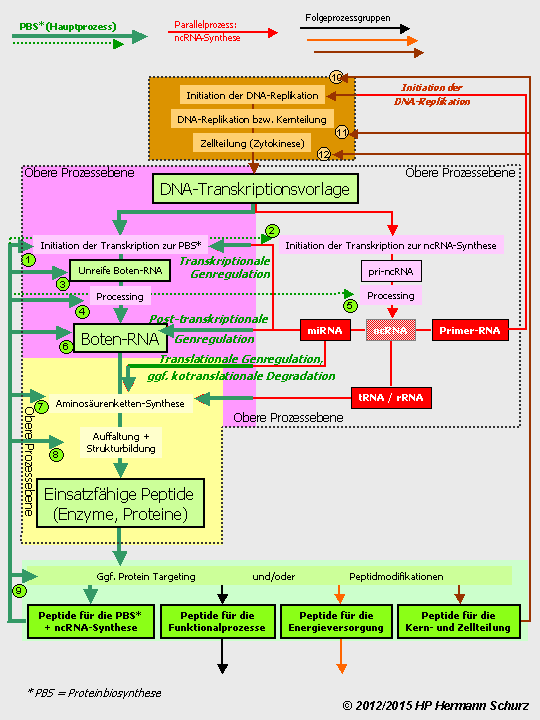
Abbildung 12: Die im Text beispielhaft genannten Peptide für Proteinsynthese, Kern- und Zellteilung sind den verschiedenen Prozessschritten 1 bis 9 (Proteinsynthese) und 10 bis 12 (Kern- und Zellteilung) zugeordnet. Theoretisch können miRNA auch beim Processing eine direkte Rolle spielen, jedoch sind derartige Prozesse noch nicht nachgewiesen. Eine indirekte Rolle spielen sie sowieso, da auch die zum Processing notwendigen Peptide oder ein Teil davon wahrscheinlich im Syntheseprozess durch miRNA reguliert werden.
Die Auswahl umfasst sowohl Peptide, die den Syntheseprozess mechanistisch durchführen als auch solche, die für die Genregulation notwendig sind und dabei alleine agieren oder mit ncRNA kooperieren. Der Kreislauf innerhalb der Proteinbiosynthese wird durch die grünen Prozesspfeile 1, 3, 4, 6, 7 und 8 links verdeutlicht. Auf Peptide, die für die Synthese der ncRNA benötigt werden, verweisen die beiden Grün gestrichelten Pfeile 2 und 5.
Zur Ausführung der Prozessschritte 10 bis 12 sind die Steuerungspeptide von Kern‑ und Zellteilung und Primer‑RNA notwendig. Aus Gründen einer besseren Darstellbarkeit sind sie in Abbildung 12 nach oben gerückt, bleiben jedoch weiterhin Teile der unteren Prozessebene.
Micro-RNA/miRNA regulieren die Proteinbiosynthese potentiell transkriptional, post‑transkriptional, translational oder kotranslational, wahrscheinlich hauptsächlich zusammen mit bestimmten Enzymen oder Proteinen.
2.6 Vollständiges Zellprozessmodell ▲
Das bis hier beschriebene Zellprozessmodell (→ Abbildung 12) ist noch unvollständig und muss um folgenden Substanzen ergänzt werden, von denen Aminosäuren, Mikronährstoffe und Lipide bzw. Lipoïde schon ausführlicher dargestellt wurden:
- Aminosäuren,
- die ursprüngliche Erbinformation der Eltern,
- Kohlenhydrate bzw. Glukose,
- Mikronährstoffe,
- Nahrungsfette und Fettbegleitstoffe (Lipide und Lipoïde),
- molekularer Sauerstoff (O2) und
- Wasser (H2O).
Da die Substanzen den Proteinbiosyntheseprozess ermöglichen, ohne dieser Prozesskette direkt zuzugehören, handelt es sich um Faktoren. Sechs davon werden von Nahrung oder Atmung zugeführt, die ursprüngliche Erbinformation bildet hier eine Ausnahme.
Erbinformation ≠ Zell-DNA
Die Unterscheidung zwischen prozesszugehöriger Zell-DNA und nicht-prozesszugehöriger ursprünglicher Erbinformation ist wichtig. Deren Unterschiede werden deutlich, wenn sie aus zwei Blickwinkeln betrachtet werden.
1. Funktion:
Die Zell-DNA ist Teil des Proteinbiosyntheseprozesses. Sie liefert die grundlegenden Informationen für die Transkription von Boten-RNA oder nicht-codierenden Ribonukleinsäuren und ist die erste Station auf dem Weg zum Peptid.
Die Erbinformation hat demgegenüber die Aufgabe, väterliche und mütterliche Erbinformationen als Grundlagen für Bau und Betrieb eines vollständigen Organismus bereitzustellen; sie ist Teil des Zellprozessmodells, gehört aber weder zur oberen noch zur unteren Prozessebene.
2. Entstehung:
Die ursprüngliche Erbinformation entsteht, wenn eine männliche und weibliche Keimzelle zur Zygote verschmelzen.
Zell-DNA geht aus der ursprünglichen Erbinformation hervor und entsteht mit der ersten Teilung der Zygote in zwei Morula-Zellen. Die beiden Chromosomensätze der neuen Zellen sind nur noch eine Kopie des ursprünglichen Erbinformationsmaterials und zur Grundlage der Proteinbiosynthese geworden.
Die ursprüngliche Erbinformation ist als ein aus der Vergangenheit stammender Faktor stoffwechselinaktiv, demgegenüber ist Zell‑DNA stoffwechselaktiv ‑ genauso wie die restlichen Faktoren ncRNA, Aminosäuren, Kohlenhydrate/Glukose, Mikronährstoffe, Fette/Fettbegleitstoffe, Sauerstoff und Wasser.
Der Faktor Sauerstoff
Sauerstoff ist für die Energiegewinnung in sämtlichen Zellen unentbehrlich. Funktionen und Gefahren des Sauerstoffs ‑ insbesondere im Zentralnervensystem und im Zusammenhang mit Affektiven Störungen ‑ werden im Abschnitt 9 von Kapitel 4 noch ausführlicher dargestellt.
Der Faktor Wasser
Als weiterer Faktor ist Wasser unverzichtbar, das bei den Zellaktivitäten größtenteils eine allgemeine Rolle spielt und wichtige Grundaufgaben erfüllt. Ohne Wasse ist kein Leben denkbar.
- Wasser als Körperbestandteil: Der menschliche Körper besteht zu ca. 70% aus Wasser. Es ist in allen Körperzellen und Körperflüssigkeiten vorhanden.
- Wasser als Lösungsmittel: Fast alle Substanzen in den Zellen, außer den wenigen fettlöslichen, sind in Wasser gelöst. Wasser ist damit die Grundlage sämtlicher Stoffwechselprozesse.
- Wasser zum Druckausgleich: Wasser ist hauptsächlich für die Steuerung des osmotischen Drucks zwischen dem Zellinneren und -äußeren verantwortlich.
- Wasser als Transportmittel: Mit Hilfe des Wassers werden alle Nährstoffe und Körpersubstanzen im Blut und der Lymphflüssigkeit zu den Organen transportiert. Blutplasma besteht zu 90 ‑ 95% aus Wasser.
- Wasser für die Verdauung: Nur mit Hilfe von Verdauungssekreten, die größtenteils aus Wasser bestehen, kann die Nahrung aufgespalten und ihre Bestandteile in den Körper aufgenommen werden.
- Wasser zur Körpertemperaturregelung: Wasser dient der Kühlung. Bei hohen Temperaturen verdunstet das Körperwasser über die Haut durch schwitzen, wobei überflüssige Wärme entzogen wird.
Der Faktor Kohlenhydrate bzw. Glukose
Die Bedeutung der Kohlenhydrate wurde beim Abschnitt über Energiegewinnung und Zellatmung kurz erörtert.
Eine ausführliche Darstellung der Problematiken dieses Faktors enthält Abschnitt 4.8, denn diese liegen in der Art und Weise der Glukoseaufnahme in eine Zelle, so dass an dieser Stelle darauf verzichtet werden kann.
Das komplette Zellprozessmodell
Nun liegen alle Bestandteile zur Konstruktion eines vollständigen Zellprozessmodells vor (→ Abbildung 13). Es setzt sich aus mehreren Teile zusammen:
- Proteinbiosyntheseprozess einschließlich seiner verschiedenen codierten Zwischen‑ und Endprodukte,
- der Zellteilung als Vorstufe zur Proteinbiosynthese,
- den Energieversorgungsprozessen,
- den speziellen Zellfunktionsprozessen und
- acht Faktoren.
Energieversorgungprozesse und Zellfunktionsprozesse werden graphisch durch Prozesspfeile repräsentiert. Die orangen Energieversorgungsprozesspfeile sind mit sämtlichen Prozessen verknüpft.
ABBILDUNG 13: VOLLSTÄNDIGES ZELLPROZESSMODELL
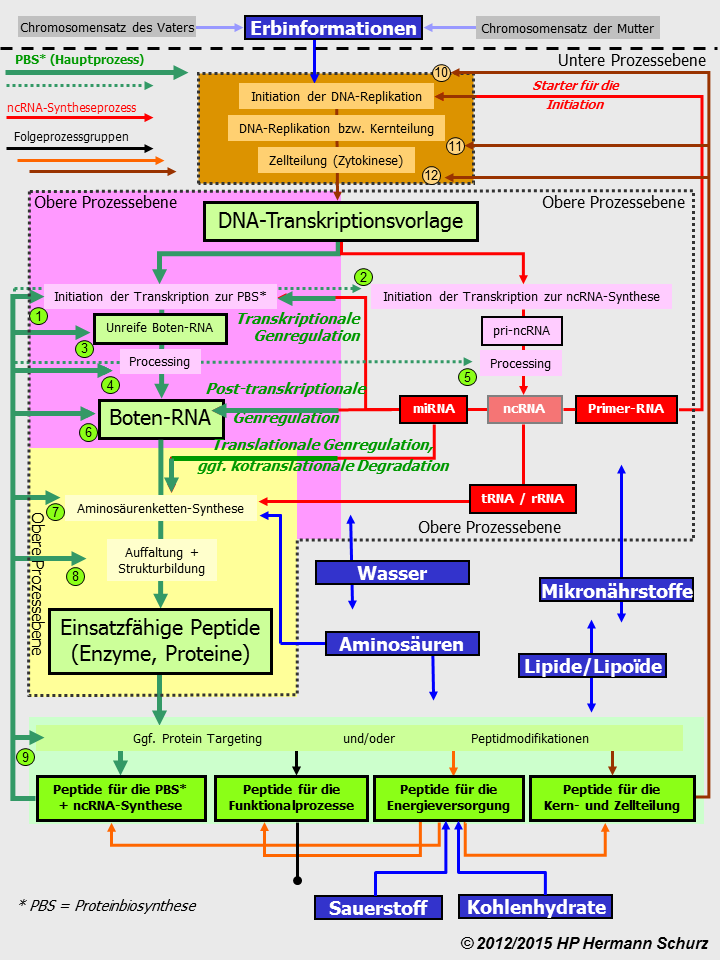
Abbildung 13: Das Zellprozessmodell integriert vier grundlegende Zellprozessbereiche (Proteinbiosynthese auf der oberen Prozessebene bzw. Funktionalprozesse, Energieversorgungsprozesse und Kern-/Zellteilung auf der unteren Prozessebene). Sechs der acht zur Prozessdurchführung notwendigen Faktoren (Aminosäuren, Erbinformationen, Mikronährstoffe, Lipide/Lipoïde, nicht-codierende Ribonukleinsäuren bzw. ncRNA und Wasser) erfüllen ihre Aufgaben auf der oberen und/oder unteren Prozessebene. Sauerstoff und Kohlenhydrate sind im Wesentlichen für die Herstellung von Energie auf der unteren Prozessebene zuständig. Die Resultate des gesamten Proteinbiosyntheseprozesses sind Peptide in Form von Enzymen und Proteinen als Voraussetzung für sämtliche Zellprozesse. Sieben der acht Faktoren werden von außen über Atmung, Nahrung oder Keimzellenverschmelzung zugeführt, ncRNA als einzige Ausnahme ausschließlich in Zellen synthetisiert. Daher werden ncRNA in Rot (statt Blau) dargestellt. Die auf Energieversorgungspeptiden beruhenden Energieversorgungsprozesse werden durch die orangen Prozesspfeile repräsentiert, die mit sämtlichen Zellprozessen verknüpft sind. Alle Funktionalprozesse sind hier als schwarze Linie dargestellt, die sich bei der Anwesenheit aller Peptide und notwendiger Faktoren automatisch entfalten.
Das vollständige Zellprozessmodell ist durch folgende grundsätzliche Aussagen, Terminologien und Substanzen charakterisiert:
- Es gibt eine obere Zellprozessebene, zu der die Proteinbiosynthese als Hauptprozess und die Transkription unterschiedlicher tRNA- und rRNA-Moleküle, Primer-RNA und genregulierender nicht-codierender RNA (ncRNA) als Nebenprozess gehören.
- Zell-DNA und Boten-RNA (mRNA) sind Informationsüberträgersubstanzen innerhalb der Proteinbiosynthese und damit ebenfalls Teil der oberen Zellprozessebene.
- Zur unteren Zellprozessebene gehören demgegenüber sämtliche durch die Proteinbiosynthese hergestellten Peptide (Enzyme und Proteine) sowie die durch diese Peptide initiierten Folgeprozesse (mit Ausnahme des Proteinbiosyntheseprozesses), also Funktionalprozesse, Energieversorgungsprozesse und die Prozesse von Kern- bzw. Zellteilung.
Die Vorgänge auf der unteren Ebene werden als Folgeprozesse bezeichnet, da sie aus dem Hauptprozess auf der oberen Ebene resultieren.
- Zwei Prozesskreisläufe verbinden untere und obere Zellprozessebene. Ein Kreislauf entsteht zwischen Kern-/Zellteilung (untere Ebene) und Transkription (obere Ebene), ein zweiter zwischen den proteinsyntheserelevanten Peptiden (untere Ebene) und dem Proteinbiosyntheseprozess (obere Ebene).
- Die ncRNA-Moleküle werden aufgrund ihrer funktionalen Charakteristik als Faktoren definiert. Faktoren sind Zellsubstanzen, die zur Durchführung von Zellprozessen notwendig sind, aber weder Informationsübertragungsfunktionen innerhalb der Proteinbiosynthese haben (Zell-DNA, Boten-RNA) noch das Ergebnis der Proteinbiosynthese sind (Peptide).
- Weitere sieben Substanzen werden aufgrund ihrer funktionalen Charakteristik ebenfalls als Faktoren bezeichnet. Dabei übernimmt die ursprüngliche Erbinformation die Rolle als ein grundlegender exogener Basisinformationsträger, Aminosäuren, Mikronährstoffe und Lipide/Lipoïde bilden die Gruppe der Baustoffe, während Kohlenhydrate, Sauerstoff und Wasser als Hilfsstoffe bezeichnet werden. Die ursprüngliche Erbinformation als Faktor ist von der Zell-DNA zu unterscheiden; letztere hat als Teil der Proteinbiosynthese lediglich eine endogene Informationsübertragungs- und keine Faktorfunktion.
- Die Energieversorgung ist mit sämtlichen Prozessen verknüpft, da sie in alle Prozesse involviert ist.
Zum nächsten Kapitel 3 - Zellschwachstellenanalyse - bitte hier klicken: ►